Структура стандартов на медицинскую технику представляет собой систему нормативных документов, определяющих требования к качеству, безопасности и производству медицинских устройств. Они являются основой для разработки, сертификации и эксплуатации медицинской техники, обеспечивая ее надежность и эффективность.
В последующих разделах статьи мы рассмотрим основные категории стандартов на медицинскую технику, процесс их разработки и утверждения, а также влияние стандартов на безопасность и качество медицинских устройств. Узнаем, какие требования должны соответствовать медицинские изделия, чтобы быть допущенными к массовому использованию, и какие меры предпринимаются для контроля и надзора за их соответствием стандартам.
- Стандарты на медицинскую технику представляют собой определенные требования и нормы к качеству, безопасности и эффективности медицинских устройств.
- Структура стандартов на медицинскую технику включает в себя общие принципы, технические характеристики, требования к маркировке и инструкциям по эксплуатации.
- Стандарты разрабатываются специализированными организациями и утверждаются национальными и международными органами по стандартизации.
- Соблюдение стандартов обеспечивает соответствие медицинской техники международным требованиям, обеспечивает безопасность пациентов и персонала, а также облегчает процессы сертификации и регистрации медицинских устройств.
- Эффективное применение стандартов на медицинскую технику способствует повышению качества медицинской помощи и улучшению условий работы медицинского персонала.
Структура стандартов для медицинской техники
Начиная с 16 июня 2018 года, действует приказ о определении стандарта медицинской помощи. Согласно пункту 1 статьи 37 Федерального закона от 21.11.2011 № 323-ФЗ, медицинская помощь организуется и оказывается в соответствии с порядками, обязательными для исполнения всеми медицинскими организациями на территории России, а также на основе стандартов медицинской помощи за исключением медицинской помощи, оказываемой в рамках клинической апробации.
В стандарте медицинской помощи содержатся необходимые требования к медицинской технике, которую необходимо соответствующим образом поддерживать и обслуживать, чтобы гарантировать качество предоставляемой услуги.
Все медицинские учреждения, занимающиеся осуществлением медицинской помощи, должны следовать стандартам, установленным Федеральным законом № 323-ФЗ, в соответствии с номенклатурой медицинских услуг. Эти стандарты включают в себя усредненные показатели частоты и кратности предоставления медицинских услуг, зарегистрированных на территории Российской Федерации лекарственных препаратов (с указанием средних доз), медицинских изделий, компонентов крови и видов лечебного питания, включая специализированные продукты. Порядок разработки указанных стандартов определяется уполномоченным федеральным органом исполнительной власти в соответствии с инструкцией по применению лекарственного препарата и фармакотерапевтической группой, рекомендованными Всемирной организацией здравоохранения.
6) Другие подходы к оказанию медицинской помощи в зависимости от характера заболевания (состояния).
Структура стандарта медицинской помощи является объектом регулирования в соответствии с приказом об оказании медицинской помощи. Этот стандарт включает основные и паспортные разделы.
Паспортный раздел стандарта медицинской помощи содержит следующую информацию:
1) возрастные особенности пациента;
2) положение о медицинской помощи;
3) вид медицинской помощи;
4) правила описание медицинской помощи;
5) метод предоставления медицинской помощи;
6) текущий этап лечения заболевания (состояния);
7) стадию и/или тяжесть заболевания (состояния);
8) осложнения (если есть);
9) продолжительность лечения на основе лечения (количество дней);
10) нозологические единицы, указанные в соответствии с Международной статистической классификации болезней и проблем, связанных со здоровьем.
Стандарт медицинской помощи определяет частоту и кратность применения следующих медицинских услуг:
1) медицинских услуг;
2) зарегистрированных в Российской Федерации лекарственных препаратов для медицинского применения (с указанием средних доз) в соответствии с инструкцией по применению их и фармакотерапевтической группой по анатомо-терапевтическо-химической классификации, рекомендованной Всемирной организацией здравоохранения;
3) медицинских изделий, которые могут быть имплантированы в организм человека;
4) компонентов крови;
5) видов лечебного питания, включая специализированные продукты лечебного питания;
6) иных методов, основанных на особенностях заболевания (состояния).
Процесс разработки стандартов устанавливается порядком.
Предложения по созданию стандарта медицинской помощи в Министерство здравоохранения Российской Федерации могут быть представлены:
а) главными экспертами Министерства;
б) представителями государственных органов субъектов Российской Федерации, занятых в сфере охраны здоровья;
в) Федеральным фондом обязательного медицинского страхования;
г) департаментами Министерства.
Предложения по разработке стандарта медицинской помощи должны быть представлены в письменном виде или в форме электронного документа с электронной подписью, и должны содержать следующую информацию:
В составе информации об обслуживании пациентов:
— название заболевания, его стадия и тяжесть по международной статистической классификации болезней и проблем со здоровьем, а также перечень осложнений в случае их наличия;
— возрастную категорию пациента;
— условия оказания медицинской помощи и ее форму;
— рекомендации по включению медицинских услуг и лекарственных препаратов;
— рекомендации по включению медицинских изделий, компонентов крови, имплантируемых в организм человека, видов лечебного питания, включая специализированные продукты лечебного питания;
— другие особенности заболевания или состояния.
Для внедрения медицинских услуг, лекарственных препаратов, медицинских изделий, компонентов крови, лечебного питания, а также специализированных продуктов лечебного питания в проект стандартов медицинской помощи необходимо учитывать их наличие в клинических рекомендациях (протоколах лечения), касающихся вопросов предоставления медицинской помощи.
Федеральное государственное бюджетное учреждение, подведомственное Министерству, в соответствии с уставом организует и методически обеспечивает создание стандартов медицинской помощи.
Организационное и методическое обеспечение включает в себя:
Одна из задач — размещение стандартов медицинской помощи на информационной платформе.
Другая важная задача — проведение медико-экономической оценки здоровоохранительных стандартов.
Проведение экспертизы задано в нескольких направлениях:
а) проверка соответствия медицинских услуг номенклатуре медицинской помощи и правильность усредненных показателей частоты и кратности предоставления медицинских услуг;
б) установление регистрации лекарственных препаратов на основе сведений, находящихся в государственном реестре лекарственных средств;
в) оценка соответствия указаний фармакотерапевтической группы анатомо-терапевтическо-химической классификации, рекомендованной Всемирной организацией по здравоохранению.
Г) Медицинские препараты должны соответствовать инструкции по применению и клиническим рекомендациям, а также правильно и точно отражать частоту их использования.
Д) Медицинские изделия, имплантируемые в человеческий организм, должны соответствовать утвержденному перечню медицинских изделий.
Е) Дозировка компонентов крови должна соответствовать клиническим рекомендациям и частоте применения, а данные о частоте использования должны быть точными.
Ж) Специализированные продукты лечебного питания должны быть зарегистрированы государством.
Оценка проекта стандарта медицинской помощи осуществляется департаментами Министерства согласно их компетенции.
В течение 15 дней с момента публикации проекта стандарта медицинской помощи в информационной системе, Департаментом лекарственного обеспечения и регулирования обращения медицинских изделий и Департаментом государственного регулирования обращения лекарственных средств будут проведены проверки на предмет следующих пунктов:
— Наличие государственной регистрации лекарственного препарата на основании сведений, содержащихся в государственном реестре лекарственных средств;
— Соответствия указания фармакотерапевтической группы анатомо-терапевтическо-химической классификации, которую рекомендует Всемирная организация здравоохранения;
— Соответствия средних доз лекарственных препаратов инструкции по применению и клиническим рекомендациям, а также корректности усредненных показателей частоты предоставления лекарственных препаратов.
г) Проверка соответствия медицинских изделий, которые будут имплантированы в организм человека, Перечню медицинских изделий, который был утвержден;
2) В течение 15 дней после проведения оценки проекта стандарта медицинской помощи, органы здравоохранения должны проверить следующие аспекты:
а) Соответствия медицинских услуг номенклатуре медицинских услуг, а также корректности усредненных показателей частоты предоставления и кратности применения медицинских услуг;
б) Соответствия средних доз компонентов крови клиническим рекомендациям и корректности усредненного показателя частоты предоставления компонентов крови;
Регистрационное подтверждение специализированных продуктов лечебного питания обязательно.
По окончании оценки проекта стандарта медицинской помощи в информационной системе, соответствующий отдел при соблюдении всех необходимых процедур разрабатывает проект нормативного правового акта, утверждающего стандарт медицинской помощи и формирует набор документов, обязательных для его публикации.
Используемые документы в области стандартизации на территории РФ:
— Национальные стандарты;
— Национальные военные стандарты;
— Межгосударственные стандарты, введенные в действие в РФ;
— Правила стандартизации, нормы и рекомендации в области стандартизации;
— Общероссийские классификаторы технико-экономической и социальной информации, применяемые в соответствии с правилами;
— Стандарты организаций.
Техническое регулирование — это направленная деятельность, целью которой является достижение максимальной организации в сфере здравоохранения через создание и установление требований, стандартов, правил, условий, продукции, технологий, работ и услуг, используемых в данной сфере.
Как эксперт в области медицинской техники, я считаю, что структура стандартов на этот тип оборудования играет критическую роль в обеспечении его безопасности и эффективности. Стандарты устанавливают требования к проектированию, производству, использованию и обслуживанию медицинской техники, что помогает минимизировать риски для пациентов и медицинского персонала.
Одной из ключевых составляющих структуры стандартов на медицинскую технику является их актуальность и соответствие современным технологическим и научным достижениям. Регулярное обновление стандартов позволяет учитывать новейшие требования безопасности и качества оборудования, что, в свою очередь, способствует развитию отрасли.
Еще одним важным аспектом структуры стандартов является их системность и комплексность. Необходимо учитывать не только технические характеристики медицинского оборудования, но и медицинские, этические, правовые и другие аспекты, связанные с его применением в здравоохранении.
В целом, структура стандартов на медицинскую технику должна быть построена таким образом, чтобы обеспечивать безопасность, качество и эффективность оборудования, а также учитывать современные тенденции развития медицинской отрасли и потребности пациентов. Только такой подход позволит создать надежную и инновационную медицинскую технику, способную улучшить результаты лечения и обеспечить высокий уровень заботы о пациентах.
Федеральный закон о техническом регулировании
Федеральный закон №184-ФЗ от 27.12.2002 года о техническом регулировании был принят для решения нескольких задач. В первую очередь, это ликвидация необоснованных административных барьеров, снятие ограничений для развития технологий и вовлечение бизнеса в нормотворческий процесс. Механизм достижения этих целей заключается в переходе от ведомственного нормирования и обязательных стандартов к разработке и введению в действие технических регламентов.
МЕТОДИКА СТАНДАРТИЗАЦИИ В ОБЛАСТИ ТЕХНИЧЕСКОГО И ТЕХНОЛОГИЧЕСКОГО ОБОРУДОВАНИЯ МЕДИЦИНСКИХ ОРГАНИЗАЦИЙ
Данный документ является результатом принятия международного договора РФ, ратифицированного в соответствии с законодательством РФ, а также межправительственного соглашения, заключенного в порядке, установленном законодательством РФ, ФЗ, УП РФ, или ПП РФ и содержит обязательные требования к объектам технического регулирования, которые обязательны для соблюдения и исполнения.
Стандарты технической поддержки медицинских организаций формируют организационно-функциональную матрицу, которая представляет структуру следующим образом. Прежде всего, стандарт, на наш взгляд, является управляющим документом планового характера, описывающим многоуровневый, многокомпонентный процесс его разработки и внедрения на всех этапах в агрегатах. Эта модель основана на типах структур (данных), отражающих общие характеристики, состав, техническое оборудование, технологическую поддержку, нормы выполнения, организационную и исполнительную структуру стандарта.
К-К- К^РАКБАЕВ, Д.С. ИСАЕВ, Б. НХРХЛЛА, А.Б. К*МАР, КАМАЛОВ К., А.Э. ИГЛИКОВА, А. Ш. РУСТЕМОВА
С.Ж. Асфендияров атындагы йазагылық медицина университеті
Денсаулық сақтау жүйелерінің ресурстық камтамасыз етілуін дамыту жағдайында
Система медицинских услуг основана на технологиях, которые соответствуют стандартам. Для успешного диагностирования, лечения, реабилитации и предоставления высококачественных услуг используются определенные технологии, которые соответствуют стандартам, утвержденным в медицине. Концептуальная основа этих технологий включает в себя различные методики и подходы к обеспечению качественной медицины.
Авторами данной статьи являются К.К. Куракбаев, Д.С. Исаев, Б. Нурулла, А.Б. Кумар, К. Камалов, А. Игликова, А. Рустемова, работающие в Казахском Национальном Медицинском Университете имени С.Д. Асфендиярова.
Статья опирается на методологические основы развития ресурсного обеспечения организаций здравоохранения и рассказывает о важности использования стандартов в медицинской практике. В течение последних трех лет Казахстан Республика плотно работает над улучшением медицинского обслуживания населения.
Авторы статьи обращают внимание на то, что в медицине нужно следовать определенным стандартам и использовать высокотехнологичные технологии для достижения наилучших результатов.
Резюме: Новая методология создания стандартов медицинской практики основана на концептуальном компоненте и заключается в переходе от стандартных фиксированных технологий к регулируемым, гибким, конструктивным процессам управления качеством диагностики, лечения, реабилитации и профилактики. Иными словами, мы считаем целесообразным пересмотреть ключевые положения медицинской практики, учитывая реальную динамику финансовой составляющей и ее значительный вклад в здравоохранение за последние 3 года в Республике Казахстан, включая разработку и внедрение новых технологий.
Авторы: К.К. Куракбаев, Д.С. Исаев, М.К. Кошимбеков, Б. Нурулла, А.Б. Кумар, К. Камалов, А.Э. Игликова, А. Ш. Рустемова
Источник: Казахский Национальный Медицинский Университет им. С.Д. Асфендиярова
Стандартизация технического и технологического оснащения в области стандартизации технического и технологического оснащения в области стандартизации в области здравоохранения предлагает организационно-функциональную матрицу, которая отражает нижеприведенную структуру.
Во-первых, стандарт является регламентирующим документом планового характера, который описывает многоуровневый, многокомпонентный процесс разработки и реализации стандарта на всех этапах в агрегированных показателях. Эта модель основана на типичных структурах данных, которые отражают общие характеристики, состав, техническое оснащение, технологическое сопровождение, результативность стандарта, организационно-исполнительную структуру стандарта.
Ключевые слова: стандартизация, техническое и технологическое оснащение, организации здравоохранения
Материалы и методы. В частности, общие характеристики стандарта включают наличие лицензии, название, кодификатор, формулировку назначения, роли и места в диагностике, лечении, реабилитации, сравнительную характеристику с известными стандартами (способы и устройства), дату и место изготовления, временной ресурс, характеристику эффекта, побочные воздействия, перечень учреждений, ответственных за гарантийный ремонт и постгарантийное обслуживание. Результаты. Состав стандарта подразумевает его структурные составляющие, целевое предназначение, нормативы потребления и обслуживания, штаты, вспомогательный персонал, показатели (шкалы) и их значение, варианты комплексации с другой медицинской техникой, ресурсное наполнение (объемы затрат на строительство или реконструкцию помещений, создание испытательных стендов), стоимость лицензий, запасного и основного оборудования, потребность в материально-технических, трудовых и информационных ресурсах, сетевой график эксплуатации с привязкой к исполнителям, мероприятиям и затратам. Техническое сопровождение отображает наличие запасных частей, условия доставки, хранения, установки, ремонта, ревизии и т.д.
Технологическое обеспечение требует следования стандартам при проведении процедур диагностики, лечения и восстановления. Это Включает в себя соблюдение условий эксплуатации и сроков использования оборудования, его контроль и замену, а Выполнение стандартов и условий их реализации. При этом необходимо учитывать объекты и субъекты, а также уровень их использования.
Результативность стандартов определяется критериями и перечнем информации, которые должны соответствовать новым знаниям, современным требованиям к материалам, моделям, способам и устройствам. Кроме того, высокий уровень внедрения и дальнейшее использование стандартов должны обеспечивать их рентабельность, продуктивность, эффективность и качество.
Организационно-исполнительная структура стандарта — один из ключевых компонентов модели, включающий правовую регламентацию, создание экспертной рабочей группы из медицинских специалистов, службы сервиса и технического персонала организаций здравоохранения. Организационно-функциональная матрица является главным механизмом управления качеством услуг в медицинской сфере.
Модель управления качеством медицинской помощи можно представить графически на рисунке, отражающем оценку ресурсного обеспечения и технологического оснащения организаций здравоохранения. Рисунок демонстрирует положительные изменения, которые достигаются при процессе управления качеством медицинской помощи.
Система представленных критериев, которые характеризуют процессы влияния составляющих ресурсную базу и соответствующие технологии на управление качеством медицинской помощи, определяет тенденции развития в этой области. Мы создали комплекс рекомендаций, направленных на совершенствование нормативно-правовой базы технического и технологического обеспечения организаций здравоохранения. Рисунок 1 демонстрирует, как ресурсное оснащение (РО) и технологическое обеспечение (ТО) оказывают воздействие на качество медицинской помощи. Уровень качества медицинской помощи определяется ее устойчивостью, адекватностью, достаточностью, доступностью, рациональностью, безопасностью, достоверностью, технологичностью, своевременностью, полнотой, кратностью, специфичностью, доступностью, удовлетворенностью, безопасностью, эффективностью, инновациями и профилактикой.
При проведении контент-анализа все материалы, которые регулируют характер определенных процессов, выглядят однотипными и стандартизированными. Они содержат только приложения, которые перечисляют нормативы, а также указывают характеристики и назначение определенных устройств и оборудования, таких как медицинские приборы, аппараты, изделия и предметы, специально разработанные для выполнения определенных функций. Кроме того, информация о количестве единиц оборудования также представлена в этих материалах. Поэтому нам кажется логичным пересмотреть структуру минимальных нормативов, включив в нее такие показатели, как высокая технологичность, специфичность и разрешающая способность, а также многофункциональность технологий, таких как диагностика, лечение и реабилитация. Мы предлагаем учитывать соответствие технических аспектов, установленных нормативами, технологическим процессам, которые используются при диагностике, лечении и реабилитации.
Необходимо зафиксировать ясный порядок финансирования, учитывая приоритетность закупок, форму собственности и виды деятельности медицинских организаций, а также придерживаясь принципа концентрации ресурсов на наиболее важных направлениях здравоохранения, определенных в Государственной программе развития и реформирования здравоохранения РК. С целью замены используемых на данный момент нормативных списков (табелей оснащения), мы разработали "Паспорт технического оснащения медицинских организаций".
В сфере здравоохранения необходимо создавать стандарты в зависимости от уровня, месторасположения, специфики (медицинские центры/клиники для смешанных, семейных или специализированных случаев), профиля, количества койкомест, частоты посещений и количества участков. В связи с увеличивающейся потребностью в медицинской помощи необходимо гарантировать ее доступность и финансирование для нашего населения, включая бесплатную медицинскую помощь (БМП), с финансовым обеспечением, чтобы создать гибкую и динамичную систему медицинского обслуживания и удовлетворить все потребности пациентов.
Наша компания хочет обратить особое внимание на то, что наши рекомендации связывают технические аспекты использования новых технологий в медицине с информационной поддержкой их внедрения и обслуживания. Мы считаем, что для успешного внедрения новых методов лечения и диагностики, а также для эффективной реабилитации пациентов, необходим систематический мониторинг и оценка соответствия утвержденным нормативам в области здравоохранения.
При выборе медицинского оборудования следует учитывать ряд важных факторов, таких как стоимость, сроки поставок, затраты на ремонт и обслуживание, а также планируемые затраты на длительность эксплуатации, замену или улучшение оборудования, срок гарантии и остаточную стоимость после выработки ресурса. Мы предлагаем нашим клиентам подбирать оборудование с учетом всех этих факторов, чтобы их инвестиции в медицинское оборудование были максимально эффективными.
Для измерения эффективности использования оборудования, включая стоимость нового оборудования, эксплуатационные и амортизационные расходы, срок гарантий, стоимость продажи устаревшего оборудования, коэффициент надежности и безопасности, предлагается использовать интегрированный показатель, который учитывает базовые расходные индикаторы. Это позволит оценить продуктивность и в конечном итоге повысить качество медицинской помощи. Для этого необходима математическая база, формализующая процессы технического и технологического обеспечения организаций здравоохранения, отражающая новый индикатор ресурсной эффективности их деятельности.
1 Методологические принципы создания стандартов для обеспечения ресурсов медицинских организаций. Кульжанов М.К., Абильдинова Н.А. // Журнал "Медицинские кадры XXI века" — Бишкек, 2009, №1 — С.34-35
2 Закон "О техническом регулировании" Республики Казахстан от 9 ноября 2004 г. — Астана: 2004
3 Приказ Министерства Здравоохранения Республики Казахстан № 313 от 30 июня 2005 г. "Об утверждении стандартов оснащения медицинской техникой и изделиями медицинского назначения для детских и родовспомогательных организаций здравоохранения". — Астана: 2005
4 Создание, обеспечение и оценка качества медицинской помощи как основа управления общественным здравоохранением: диссертация на соискание ученой степени доктора медицинских наук 14.00.33. Калажанов М.Б. — Алматы: 2006, 278 с.
В статье Данишевского К.Д. рассматриваются факторы, которые могут препятствовать успешному внедрению эффективных технологий управления в системе здравоохранения (Гл.врач, 2003, №2, С.43-46).
Исаев Д.С. и другие авторы представляют работу, посвященную оценке и прогнозированию качества общественного здоровья в Алматы (2006, 203 с.).
Авторский коллектив из К.К- К^РАКБАЕВ, Д.С. ИСАЕВ, Б. НХРХЛЛА, А.Б. К*МАР, КАМАЛОВ К., А.Э. ИГЛИКОВА, А. Ш. РУСТЕМОВА составил научную работу о медицинском университете им. С.Ж.
Асфендиярова.
Важность технических и технологических инноваций в области здравоохранения подчеркивается в статье о ДЕНСАУЛЫК САКТАУ, опубликованной на сайте университета (ЖАБДЫКТАЛУЫН, техникалыК жЭне технологиялыК саласындаГы, 2021).
Мы представляем методику стандартизации оборудования в сфере медицины на основе матрицы, разработанной функциональными специалистами. В настоящее время мы можем получить стандарты безопасности, описывающие детали процедуры и технологии безопасности и организации.
Общая характеристика стандартизации включает описание процесса, его техническое обоснование, технологическое описание, обоснование примененных технологий, результаты стандартизации и ее реализации. Авторы — К.К. Куракбаев, Д.С. Исаев, Б. Нурлла, А.Б. Кумар, К. Камалов, А. Игликова, А. Рустемова и работают в Казахском национальном медицинском университете имени С.Д.
Асфендиярова.
Наша работа направлена на улучшение качества и безопасности оборудования в области здравоохранения.
Структура стандартов технической поддержки медицинских организаций
Как мы видим, стандарт технической поддержки медицинских организаций представляет собой организационно-функциональную матрицу, которая описывает многоуровневый, многокомпонентный процесс его разработки и реализации на всех этапах. Этот стандарт является законодательным документом, который описывает общие характеристики, состав, техническое оборудование, технологическую поддержку, нормы производительности, организационную и исполнительскую структуру в соответствии с типами структур (данных).
Одним из распространенных заблуждений о структуре стандартов на медицинскую технику является мнение о том, что они унифицированы и одинаковы для всех стран. В действительности стандарты могут отличаться в зависимости от страны или региона, в котором применяются. Например, стандарты Европейского союза могут отличаться от стандартов, принятых в США или Азии.
Еще одним заблуждением является мнение о том, что стандарты на медицинскую технику разрабатываются только экспертами в области медицины. На самом деле в разработке стандартов участвуют специалисты различных областей — от инженеров до юристов. Это необходимо для того, чтобы учесть все аспекты безопасности и качества медицинской техники.
Также некоторые люди считают, что стандарты на медицинскую технику являются обязательными для всех производителей. Однако это не так — стандарты могут быть добровольными или обязательными, в зависимости от законодательства страны. В некоторых случаях производители добровольно следуют стандартам для повышения качества своей продукции и доверия потребителей.
Основные положения государственной системы стандартизации для медицинской техники
Государственная система стандартизации включает в себя:
- Нормативно-техническую документацию
- Категории НТД для медицинских и фармацевтических товаров
- Процесс сертификации
- Тема 1.4: Метрология и метрологическая служба. Для дополнительной информации обратитесь к страницам 518-519. 2. Н. Б. Дремова представляет основные положения государственной системы стандартизации.
Закон Российской Федерации "О стандартизации" (10.06.1993 № 5154-1) определяет стандартизацию как процесс установления норм, правил и характеристик продукции, работ и услуг для:
- обеспечения безопасности для жизни, окружающей среды, здоровья и имущества;
- достижения технической и информационной совместимости, а Взаимозаменяемости продукции;
- гарантирования качества продукции, работ и услуг в соответствии с уровнем развития науки, техники и технологии;
- осуществления единства измерений и т.д.
В соответствии с ГОСТ 1.0-85, стандартизация представляет собой процесс, направленный на решение повторяющихся задач в области науки, экономики и техники с целью достижения максимальной степени упорядоченности в определенной сфере деятельности.
Стандартизация способствует улучшению качества продукции, ее упаковки и внешнего вида, а также продления срока службы товаров. Она играет важную роль в управлении различными отраслями экономики. Государственная система стандартизации включает правила и положения, определяющие ее цели и задачи, методы проведения работ, а также комплекс взаимосвязанных правил. Создание нормативно-технической документации, определяющей требования к продукции для разных отраслей народного хозяйства, ее производству, разработке и использованию, является главной задачей стандартизации. Таким образом, стандартизация является неотъемлемой частью менеджмента экономики, способствующей ее развитию и повышению качества продукции.
Нормативно-техническая документация (НТД) включает в себя стандарты, классификаторы, правила, руководящие документы и другие материалы, которые содержат требования к условиям производства, технологиям, работам и услугам. При разработке этих документов учитываются достижения отечественной и зарубежной науки, техники, технологии и передовой опыт.
С помощью стандартизации определяются единицы измерений, термины и обозначения, сырье, производственные процессы, методы испытаний и измерений, а также технические требования, которые обеспечивают качество продукции, безопасность людей и сохранность материальных ценностей. НТД также защищает экономические интересы покупателей, предоставляя им возможность использовать продукцию в течение определенного срока, исправлять выявленные дефекты за счет предприятия и получать полную замену или возврат полной стоимости продукта в случае преждевременной поломки. В области здравоохранения стандартизация направлена на достижение оптимальной организации с помощью разработки и установления требований, норм, правил и характеристик условий, продукции, технологий, работ и услуг, используемых в здравоохранении. Документы государственной стандартизации обязательны для всех предприятий, независимо от их формы собственности и отрасли хозяйства.
- Нормативно-техническая документация
Стандарт на продукцию – это документ, который устанавливает требования к продукции или её группе для обеспечения соответствия её назначению. Основные виды стандартов:
- Государственный стандарт России (ГОСТ Р) – устанавливается на продукцию, работы и услуги, отвечающие межотраслевым потребностям и утверждается Госстандартом России;
- Отраслевой стандарт ОСТ – разрабатывается, если отсутствует ГОСТ Р или при необходимости установления дополнительных требований, которые расширяют установленные ГОСТом России.
- Стандарт предприятия
Если на объекте стандартизации нет ГОСТ Р или ОСТ, то разрабатывается СТП для предприятия. Технические условия определяют требования к продукции, процессу или услуге и могут являться частью стандарта.
Международные стандарты ИСО разрабатываются международной организацией по стандартизации (ISO) с целью облегчения международного обмена товарами и услугами. Стандарты ИСО серии 9000 (для систем качества на предприятиях) были введены в 1987 году, а в России начали выдавать сертификаты на соответствие требованиям ИСО 9000 с 1995 года (выдано 22 сертификата).
В 1996 году было зарегистрировано 56 стандартов ИСО, в 1997 году — 95, в 1998 году — 132, а к 1999 году их число достигло 541. В 2000 году в Международной организации по стандартизации (ИСО) поступило предложение о разработке документа, направленного на внедрение стандартов ИСО 9000 в сфере здравоохранения. Этот документ предназначен для повышения качества медицинской и фармацевтической помощи, оказываемой в различных учреждениях здравоохранения, включая аптеки, производственные предприятия медицинского оборудования и фармацевтических товаров. Важно отметить, что для медицинской техники существуют отдельные стандарты ИСО 13485.
Существуют нормативно-технические документы, утверждаемые для медицинских и фармацевтических товаров, классификация которых изображена на рисунке 7. Интересно отметить, что уже в 1973 году был утвержден ГОСТ 19126-73 на медицинские инструменты.
- Виды нормативно-технических документов для медицинских и фармацевтических товаров:
Для медицинских и фармацевтических товаров существуют нормативно-технические документы, классификация которых изображена на рисунке 7 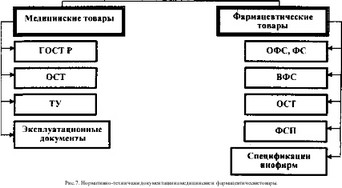 .
.
Существует общий нормативный документ, в котором закреплены требования к техническим характеристикам медицинского инструмента, контрольно-измерительным приборам и методам их проверки, правилам маркировки, упаковки, хранения и транспортировки. В 1975 году был утвержден ГОСТ 20790-75 «Приборы, аппараты и оборудование медицинские. Общие и технические условия».
Кроме того, действуют нормативные документы, регламентирующие технические характеристики медицинских принадлежностей, в том числе перевязочных материалов, шприцев, игл, режущих и зажимных инструментов и других. Утверждение отраслевых стандартов осуществляется Министерством здравоохранения РФ и является обязательным для всех медицинских предприятий и организаций. Контроль качества произведенной продукции осуществляется в соответствии с техническими условиями.
Стандарты на медицинские изделия состоят из следующих разделов: а) назначение изделия; б) классификация (в случае стандартов на группу изделий); в) основные размеры; г) технические требования; д) комплектность изделия; е) правила приемки и методы испытаний; ж) маркировка, упаковка, хранение. Стандарт качества лекарственных средств (JIC) — это нормативный документ, содержащий перечень нормируемых показателей и методов контроля качества ЛС, утверждаемый М3 РФ.
Для J1C и лекарственного растительного сырья применяются следующие виды НТД: общие фармакопейные статьи (ОФС), фармакопейные статьи (ФС), временные фармакопейные статьи (ВФС), ОСТ, фармакопейные статьи предприятий (ФСП). ОФС — государственный стандарт качества JIC; включает в себя перечень нормируемых показателей или методов испытания для конкретной лекарственной формы, описание физических, физико-химических, химических, биохимических, биологических, микробиологических методов анализа JIC, требования к используемым реактивам, титрованным растворам, индикаторам. ФС — государственный стандарт качества JIC под международным непатентованным наименованием (МНН), содержит обязательный перечень показателей и методов контроля качества с учетом его лекарственной формы. ФС утверждаются на J1C, имеющие наибольшую терапевтическую ценность, широко вошедшие в медицинскую практику и имеющие высокие качественные показатели. ФС включаются в государственную фармакопею (серийное производство). Термин «Фармакопея» происходит от греческих слов pharmakon
- Руководство по приготовлению лекарств — это poieo, что означает "делаю" на греческом языке, переведенное на русский язык.
Государственная фармакопея (ГФ) — это установленный законодательно сборник государственных стандартов качества JIC. На данный момент действует ГФ XI издания, выпущенное в 1987 году. ГФ утверждается для JIC и лекарственного растительного сырья, а также для первых промышленных серий новых JIC, намеченных для медицинского применения и рекомендованных фармакопейным комитетом, чтобы перейти на серийное производство.
Он действительный на ограниченный срок — не более трех лет, и ОСТ устанавливаются на дополнительные технические требования и групповые характеристики, необходимые для изготовления и поставки JIC (термины, обозначения, правила приемки, маркировка, упаковка, хранение, транспортирование и др.). Они утверждаются Министерством здравоохранения РФ и медицинской промышленностью.
ФСП или стандарт качества JIC под торговым названием — это перечень показателей и методов контроля качества J1C, произведенного конкретным предприятием, учитывающий конкретную технологию данного предприятия. Этот стандарт проходит экспертизу и регистрацию в установленном порядке.
Многие страны имеют свои национальные фармакопеи, но с 1951 года ВОЗ издаёт международную фармакопею, которая состоит из пяти томов. В первом томе содержатся общие методы анализа, в то время как во втором и третьем томах содержатся спецификации для контроля качества фармакопейных препаратов: том 2 — 126 субстанций, том 3 — 157 субстанций. Четвёртый и пятый тома содержат спецификации для контроля качества готовых лекарственных форм, вспомогательных средств и упаковочных материалов. Импортные JIC могут включать в себя такие фармакопеи как ГФ, ВФС и зарубежные фармакопеи.
Кроме того, в комплект изделия, выпущенного предприятием-изготовителем, входят эксплуатационные документы. Простым изделиям, которые уже хорошо известны потребителям, прилагается этикетка с наименованием, обозначением и индексом изделия, техническими характеристиками, номером стандарта или ТУ, информацией о приемке ОТК, количеством изделий в одной упаковке и датой выпуска.
Для сложных изделий необходимо иметь паспорт или формуляр. В паспорте содержатся основные характеристики и параметры изделия, а также информация, аналогичная той, что на этикетке. В дополнение к этому, там содержатся гарантийные обязательства предприятий, данные о консервации и упаковке.
Если есть необходимость, то к паспорту могут быть приложены журналы или листки, на которых указана информация о работе изделия и техническом обслуживании. Эти документы называются формуляром. При эксплуатации изделия важно иметь технический паспорт (ТО) или инструкцию по эксплуатации (ИЭ). В некоторых случаях они могут объединяться.
- Сертификация
Чтобы убедиться в соответствии товара определенному уровню качества, указанному в НТД, проводится процедура сертификации, которая заканчивается выдачей специального документа — сертификата. Сертификация является важным механизмом контроля качества и является одним из прогрессивных направлений развития стандартизации. В России законодательно установлены требования по сертификации продукции и услуг, прописанные в Законе РФ, который введен в действие с 01.06.93г.
Суть сертификации заключается в проверке соответствия изделий установленным требованиям международных, национальных стандартов стран-импортеров, а также государственных стандартов. Эту деятельность осуществляет компетентная и независимая организация.
Сертификация имеет несколько основных целей: во-первых, она помогает потребителям при выборе качественной продукции; во-вторых, защищает их от недобросовестных изготовителей и продавцов; в-третьих, обеспечивает контроль безопасности для окружающей среды, здоровья, жизни и имущества; в-четвертых, подтверждает заявленные производителем показатели качества. Сертификационные испытания проводятся только в аккредитованных лабораториях, входящих в Российскую систему сертификации.
После проведения исследований выдается протокол испытаний, который может использоваться только как документ, содержащий результаты тестов и дополнительную информацию, относящуюся к их проведению. Испытательные лаборатории не имеют права выдавать сертификаты.
Уникальность данного текста состоит в том, что сертификат соответствия для продукции выдается через систему сертификации для подтверждения соответствия требованиям. Он выдается на бланке формы, имеющем идентификационные водяные знаки, и является действительным в течение срока годности. Подтверждение соответствия продукции требованиям также осуществляется знаком соответствия.
Знак соответствия подтверждает соответствие продукции требованиям маркировкой, установленной системой сертификации. Необходима обязательная сертификация для медицинских и фармацевтических товаров.
 Обязательная сертификация подтверждает соответствие товара (работы, услуги) обязательным требованиям. Это необходимо для обеспечения безопасности сертифицированной продукции для потребления. Госстандарт России и другие государственные органы осуществляют контроль и надзор за сертифицированной продукцией.
Обязательная сертификация подтверждает соответствие товара (работы, услуги) обязательным требованиям. Это необходимо для обеспечения безопасности сертифицированной продукции для потребления. Госстандарт России и другие государственные органы осуществляют контроль и надзор за сертифицированной продукцией.
Вопросы контроля качества находятся в ведении Департамента государственного контроля JIC, ИМН и медицинской техники М3 РФ, который в основном занимается контролем качества продукции.
Для работы по экспертизе медицинской и фармацевтической продукции и ее дальнейшей государственной регистрации приняты следующие документы:
- «Правила регистрации медикаментов»
- «Положение об ускоренной процедуре регистрации ЛС»
- Основные принципы стандартов качества медикаментов установлены в соответствии с ОСТ № 91500.05.001-00.
- В Российской Федерации был разработан целый комплекс мероприятий, направленных на активное введение в действие Правил проведения сертификации в Системе сертификации ЛС Системы сертификации ГОСТ Р, утвержденных Постановлением Госстандарта России от 24.05.2002 г. № 36 (зарегистрировано Минюстом России от 29.07.2002 г. № 3556). Они гарантируют абсолютную идентичность сертифицируемой продукции, а также повышают надежность сертификатов соответствия. Кроме того, они создают возможность точного учета количества медикаментов, находящихся в обороте.
- Метрология и метрологическая служба — это неотъемлемая часть данного комплекса мероприятий.
Метрология — наука, изучающая измерения, способы обеспечения их единства и достижения необходимой точности. Единство измерений означает, что результаты измерений выражены в соответствии с установленными стандартами и их погрешность известна с определенной вероятностью.
Важность единства измерений проявляется при проведении товароведческих экспертиз в различных организациях с использованием различных средств измерения в разное время. Результаты таких измерений должны быть сопоставимы и близки к истинному значению, что указывает на точность измерений.
Законодательство большинства стран мира предписывает проведение мероприятий по обеспечению точности единиц измерения. Для достижения этой цели регулярно проверяются меры и измерительные приборы, находящиеся в эксплуатации. В России в 1993 году был принят Закон "Об обеспечении единства измерений", который регулирует развитие метрологии.
Охрану единства измерений в России осуществляет Государственный комитет по стандартизации, метрологии и сертификации (Госстандарт России). В его компетенцию входит Государственная метрологическая служба, включающая государственные научные метрологические центры и органы государственной метрологической службы на территориях субъектов РФ. Основой государственной системы единства измерений являются государственные стандарты. Чтобы проверить свои знания по данной теме, можно попробовать ответить на вопросы для самоконтроля.
Общая медицинская стандартизация была начата в России в 1997 году после принятия решения "Об основных положениях стандартизации в здравоохранении".
Цели стандартизации в медицине
Стандартизация в медицинской сфере помогает достигнуть следующих целей:
- разработать общие критерии для оценки работы медицинских учреждений;
- установить единые требования к содержанию и объему медицинских услуг;
- нормировать деятельность специалистов в рамках сертификации и лицензирования их услуг, а также аккредитации медицинских учреждений;
- обеспечить наличие метрологического контроля в медицинской практике;
- разработать систему классификации, каталогизации и кодирования медицинских услуг.
Перечень национальных стандартов в области медицинских изделий

Начиная с 30 мая 2011 года, существует 4082 регламентации по безопасности в области медицинских электрических изделий. В соответствии с ГОСТ Р 50267.12-2006, аппараты искусственной вентиляции легких для интенсивной терапии должны соответствовать частным требованиям безопасности.
Кроме того, ГОСТ Р 52770-2007 устанавливает методы санитарно-химических и токсикологических испытаний для гарантированного соблюдения требований безопасности медицинских изделий. ГОСТ Р ЕН 13795-1-2008 и ГОСТ Р ЕН 13795-2-2008 регулируют хирургическую одежду и белье, используемые в качестве медицинских изделий для пациентов и персонала, а также оборудования. Общие требования и методы испытаний определены соответствующими частями этих стандартов. Никаких нарушений указанных стандартов в области медицинских изделий быть не должно, чтобы обеспечить безопасность пациентов и персонала в медицинском учреждении.
В данной статье описывается использование хирургической одежды и белья в качестве медицинских изделий для различных целей, включая использование для пациентов, хирургического персонала и оборудования. Весь процесс направлен на обеспечение безопасности и комфорта всех участников.
Для этого были разработаны специальные требования и уровни исполнения, отраженные в ГОСТ Р ИСО 9919-2007. В качестве другого примера использования медицинских изделий, ГОСТ Р ИСО 10993-1-2009 описывает оценку биологического воздействия медицинских изделий, включая исследования и выводы, а ГОСТ Р ИСО 10993-2-2009 описывает требования к обращению с животными. Наконец, исследование генотоксичности, канцерогенности и токсического воздействия на репродуктивную функцию описывается в ГОСТ Р ИСО 10993-3-2009. Эти стандарты позволяют гарантировать безопасность и эффективность использования медицинских изделий.
В данном документе рассмотрены вопросы оценки воздействия медицинских изделий на организм человека. Четвертая часть посвящена исследованию эффекта на изделия, взаимодействующие с кровью, пятая часть — методам invtro на цитотоксичность, а шестая — исследованию местного действия после имплантации. Девятая часть изучает основные принципы идентификации и количественного определения продуктов деградации, а десятая — общие принципы оценки биологического воздействия. Все указанные требования представлены в государственном стандарте РФ "ГОСТ Р ИСО 10993-5-2009", "ГОСТ Р ИСО 10993-6-2009", "ГОСТ Р ИСО 10993-7-2009", "ГОСТ Р ИСО 10993-9-2009" и "ГОСТ Р ИСО 10993-10-2009".
Исследования воздействия медицинских изделий на организм. Часть 10. Оценка раздражительного и аллергического действия
ГОСТ Р ИСО 10993-11-2009
Определение общего токсического эффекта медицинских изделий. Часть 11. Детальный анализ воздействия на организм.
ГОСТ Р ИСО 10993-12-2009
Изготовление проб и контрольных образцов медицинских изделий. Часть 12. Оценка биологической активности.
ГОСТ Р ИСО 10993-13-2009
Идентификация и определение количества продуктов деградации полимерных медицинских изделий. Часть 13.
ГОСТ Р ИСО 10993-14-2009
В данном тексте речь идет об оценке биологического воздействия медицинских изделий. Части 14, 15, 16 и 17 ГОСТ Р ИСО 10993-2009 регулируют процедуры идентификации и количественного определения продуктов деградации изделий из керамики, металлов и сплавов, моделирования и исследования токсикокинетики продуктов деградации и вымывания, а также установление пороговых значений для вымываемых веществ. Все эти процедуры необходимы для того, чтобы гарантировать безопасность и эффективность медицинских изделий, используемых в лечении и диагностике многих заболеваний.
В данном документе описывается оценка биологического действия медицинских изделий путем исследования их химических свойств. Эти правила установлены в ГОСТ Р ИСО 15193-2007. Также описывается измерение величин в пробах биологического происхождения при диагностике invitro. В соответствии с ГОСТ Р ИСО 15194-2007, приведены референтные методики выполнения измерений, а также описание стандартных образцов при их проведении, представленных в ГОСТ Р ИСО 15198-2009. Важным аспектом является подтверждение методик контроля качества, рекомендуемых изготовителями пользователям, на что указывает ГОСТ Р ИСО 17511-2006, который регулирует изделия медицинского назначения для клинической лабораторной медицины.
Предназначенные для проведения диагностики внутриорганизмовых процессов, медицинские изделия требуют точных измерений в биологических пробах. Аттестация калибраторов и контрольных материалов обеспечивает метрологическую прослеживаемость значений. Соответствующие требования прописаны в стандарте ГОСТ Р ИСО 17593-2009.
Системы мониторинга invitro необходимы при самотестировании антикоагулянтами. Для этого медицинские изделия и клинические лаборатории должны соответствовать требованиям, установленным в ГОСТ Р ИСО 18153-2006.
Для корректного измерения каталитической концентрации ферментов в биологических пробах необходима метрологическая прослеживаемость значений. Это процедура, которая описана в ГОСТ Р ИСО/ТО 14969-2007 в контексте измерения величин в средствах медицинской диагностики invitro.
Системы менеджмента качества — неотъемлемая составляющая производства медицинских изделий. Их применение регулируется ГОСТ Р ИСО/ТО 16142-2008.
Вопросы безопасности и характеристик медицинских изделий регулируются специальными стандартами, которые нужно учитывать при выборе изделий. Один из таких стандартов — ГОСТ Р ИСО/ТС 10993-19-2009, который описывает исследования физико-химических, морфологических и топографических свойств материалов. Еще один стандарт, ГОСТ Р ИСО/ТС 10993-20-2009, уделяет внимание исследованию иммунотоксичности медицинских изделий. Другой стандарт, ГОСТ Р ИСО/ТС 19218-2008, определяет структуру кодов, описывающих виды и причины неблагоприятных событий, связанных с медицинскими изделиями. Кроме того, есть ГОСТ Р МЭК 60580-2006 и ГОСТ Р МЭК 60601-1-1-2007, которые регулируют измерители произведения дозы на площадь и соответствующие медицинские изделия.
Требования безопасности для медицинских электрических изделий описаны в ГОСТ Р МЭК 60601-1-6-2007. В этом документе охвачены общие требования безопасности, а также эксплуатационная пригодность.
В данном списке упоминается ГОСТ Р МЭК 60601-1-8-2007, который описывает общие требования безопасности, испытания и руководящие указания для систем сигнализации медицинских электрических изделий и медицинских электрических систем.
Изделия медицинские электрические, работающие в диапазоне от 1 до 50 МэВ, подпадают под требования безопасности, указанные в ГОСТ Р МЭК 60601-2-1-2009.
ГОСТ Р МЭК 60601-2-2-2006 описывает частные требования безопасности для медицинских ускорителей электронов.
Вторая часть стандарта ГОСТ Р МЭК 60601-2-7-2006 содержит частные требования к безопасности высокочастотных электрохирургических аппаратов. Часть 2-7 этого же стандарта устанавливает частные требования к рентгеновским питающим устройствам диагностических рентгеновских генераторов. Часть 2-22 стандарта ГОСТ Р МЭК 60601-2-22-2008 определяет частные требования безопасности к работе с хирургическим, косметическим, терапевтическим и диагностическим лазерным оборудованием. Часть 2-33 этого же стандарта содержит частные требования к безопасности медицинского диагностического оборудования, работающего на основе магнитного резонанса. И, наконец, часть 2-43 стандарта ГОСТ Р МЭК 60601-2-43-2008 устанавливает частные требования к безопасности медицинского оборудования, используемого в диагностике.
Частные требования безопасности к рентгеновским аппаратам для интервенционных процедур описаны в изделиях медицинских электрических, соответствующих ГОСТ Р МЭК 60601-2-43.
Чтобы обеспечить безопасность при использовании регистрирующих и анализирующих электрокардиографов, необходимо соблюдать Частные требования безопасности с учетом основных функциональных характеристик, описанные в изделиях медицинских электрических, соответствующих ГОСТ Р МЭК 60601-2-51-2008.
Требования к параметрам акустического выхода в технической документации на приборы ультразвуковой диагностики описаны в изделиях медицинских электрических, соответствующих ГОСТ Р МЭК/ТО 60977-2009, являющихся частью Государственной системы обеспечения единства измерений.
Руководство по проверке функциональных характеристик медицинских электронных ускорителей от 1 МэВ до 50 МэВ описано в изделиях медицинских электрических, соответствующих ГОСТ Р МЭК 61157-2008.
- Лабораторная диагностика
- Исследование микромира
- Анализ простейших существ
- Изучение гельминтов
- Определение опасных насекомых
Стандартизация — это процесс установления общих правил и характеристик, которые добровольно и многократно используются. Таким образом, можно достичь упорядоченности в производстве и реализации товаров. Сейчас существует единая классификация в соответствии со стандартами ISO.
Стандартизация фармацевтических изделий и медицинской продукции основывается на научных достижениях, передовом опыте и технике. Этот процесс непосредственно влияет на качество медицинских товаров. Главной целью стандартизации является повышение уровня качества продукции и определение ключевых показателей.
— Гарантировать защиту интересов потребителей и государства через регулирование номенклатуры и качества продукции;
— Возможность повышения качества фармпродукции;
— Обеспечение взаимозаменяемости и совместимости медпродукции;
— Содействие экономии материальных, людских и энергоресурсов;
— Установка технических барьеров в производстве и продажах;
— Обеспечение конкурентоспособности продукции фармацевтики.

Стандартизация основывается на нескольких принципах: согласия, единообразия, значимости, актуальности, комплектности, проверяемости, экономии и содействия.
Объектами стандартизации являются вещи, процессы и отношения, которые должны иметь повторяемость в пространстве или времени. Это позволяет укреплять нормы и правила, в том числе юридические и социальные.

Работа, связанная со стандартизацией систем качества в сфере здравоохранения, осуществляется Интернациональной организацией по стандартизации (ИСО) и ГОСТами. ИСО ответственна за создание и внедрение стандартов, включая те, которые связаны с медицинской сферой, основанные на ИСО 9001. Стандарты этой области деятельности являются самыми разнообразными, при этом ИСО имеет различные статусы, такие как сертификация, указания руководства, а также стандарты, которые представлены в виде руководств и пояснений.
Примером стандартов в области систем качества в здравоохранении является ИСО 15378:2006, который был разработан для материалов внутренней упаковки медицинских изделий. Этот стандарт применяется для организаций, занимающихся разработкой, производством и поставкой соответствующих материалов.
ISO 13485:2003 — это набор требований, предъявляемых к компаниям, которые занимаются организацией, проектированием, разработкой, монтажом, обслуживанием и продажей изделий, устройств и оборудования для области медицины. В стандарте представлены руководящие указания, детально описывающие требования ISO 13485:2003. Но стоит отметить, что этот стандарт не предназначен для сертификации, а лишь является вспомогательным.
ISO 14971:2007 определяет процесс выявления рисков, связанных с медицинскими изделиями на стадиях их производства (от диагностики до контроля) и следит за эффективностью мониторинга. ISO IWA1:2005. Этот стандарт был создан в результате международного соглашения. Он призван оказать помощь организациям здравоохранения на всех этапах разработки, внедрения и улучшения менеджмента качества. Стоит отметить, что этот стандарт также не предназначен для сертификации.
Сегодня в мире существует огромный объем разработанных стандартов ГОСТ и ИСО. Например, одним из таких является стандарт по иммунотоксикологии. Он содержит информацию о потенциальных иммунологических медицинских изделиях, а также предоставляет инструкции по методам исследования различных видов медицинских изделий.
Данный стандарт формировался на основе многих публикаций, написанных разными группами специалистов по иммунотоксикологии. Данные включают исследования за последние двадцать лет, а также с момента создания иммунотоксикологии как отдельной дисциплины в науке.
Как считают противники ИСО, эти стандарты способствуют разделению труда на руководящие и исполнительские функции, что является фундаментальной ошибкой в управлении с точки зрения организации. Руководитель принимает решения, а исполнитель их выполняет, что приводит к нерациональному использованию ресурсов. Кроме того, такой подход может негативно сказаться на инновациях.
Однако для инноваций необходимо видеть продукт глазами потребителей и полностью управлять процессом от начала и до конца, что предоставляет ГОСТ, в отличие от ИСО. Даже противники стандартов утверждают преимущества ГОСТа перед ИСО.
— Возврат к содержанию раздела "диагностика в лаборатории"




