Да, сертификат соответствия на медицинское оборудование необходим для обеспечения безопасности пациентов и качества медицинских услуг. Он подтверждает соответствие изделия установленным стандартам и требованиям.
В следующих разделах статьи мы рассмотрим процесс получения сертификата соответствия на медицинское оборудование, основные требования к качеству и безопасности продукции, а также роль регуляторных органов в этом процессе. Узнаем, как выбрать подходящего сертификационного органа и какие последствия могут быть в случае нарушения требований.
- Сертификат соответствия на медицинское оборудование является обязательным требованием для того, чтобы продукция могла быть использована в медицинских учреждениях.
- Сертификат удостоверяет, что оборудование соответствует всем необходимым стандартам и требованиям безопасности.
- Наличие сертификата повышает доверие к производителю и продукции, позволяет убедиться в качестве и надежности оборудования.
- Без сертификата соответствия могут возникнуть проблемы при прохождении контроля и аккредитации медицинских учреждений.
- Для эксплуатации медицинского оборудования без сертификата могут возникнуть последствия, такие как отказ в приеме пациентов или нарушение правил безопасности.
Сертификация медицинской техники и оборудования в Российской Федерации
В России установлена система государственных стандартов (ГОСТ Р), которая является основой для сертификации медицинских изделий. Прежде чем предприниматели получат право производить, импортировать и реализовывать медицинскую продукцию, необходимо проходить оценку ее качества. Без такой проверки деятельность будет незаконной и может привести к серьезным административным и уголовным наказаниям.
Кроме того, медицинская техника и оборудование также подлежат государственной регистрации в Росздравнадзоре. Регистрационное удостоверение, полученное в результате проверки, является необходимым для легального использования продукции в медицинских учреждениях и в частной практике.
Выбор продукции, подлежащей проверке
Врачи используют огромное количество медицинской техники и оборудования для диагностики и лечения разных заболеваний. Продукцию можно разделить на четыре класса в зависимости от степени опасности:
- Класс 1 характеризуется низкой степенью опасности (медицинские весы, микроскопы и аналогичные приборы);
- Класс 2А относится к средней степени (лабораторная техника, спирометры);
- Класс 2Б имеет повышенный уровень риска (аппараты искусственной вентиляции легких, дефибрилляторы, кардио анализаторы);
- Класс 3 подразумевает самую высокую степень опасности (эндопротезы, имплантаты).
Новости о сертификации
Согласно постановлению №1133, принятому Правительством Российской Федерации 10 июля 2023 года, продлено действие упрощенного порядка подтверждения соответствия продукции требованиям технических регламентов и стандартов национального и международного уровня при ее ввозе из-за границы или выпуске на территории страны до 1 сентября 2024 года. Однако упрощенный режим не будет применяться к продукции, которая подлежит сертификации в соответствии с ТР ТС 007 и 017. Подробности данного вопроса изложены в Приказе Министерства промышленности и торговли Российской Федерации от 13 апреля 2023 года №1303 "О внесении изменений в приказ МПиТ РФ от 2 ноября 2022 года №4616", где приведен перечень таких продуктов.
Сертификат соответствия на медицинское оборудование – это ключевой документ, подтверждающий качество и безопасность продукции. Наличие сертификата обеспечивает доверие покупателей, позволяет убедиться в соответствии изделия требованиям законодательства и стандартам качества. Благодаря этому у покупателей есть уверенность в том, что оборудование прошло необходимую проверку и соответствует всем необходимым стандартам безопасности и эффективности.
Кроме того, наличие сертификата соответствия на медицинское оборудование обеспечивает защиту от некачественных и поддельных товаров. Это особенно важно в медицинской сфере, где качество оборудования напрямую влияет на здоровье и безопасность пациентов. Сертификат является гарантией того, что продукция прошла все необходимые проверки и испытания перед попаданием на рынок, что обеспечивает безопасность и надежность для конечного пользователя.
Таким образом, сертификат соответствия на медицинское оборудование играет важную роль в обеспечении качества и безопасности продукции. Этот документ является неотъемлемой частью процесса производства и реализации медицинского оборудования, обеспечивая доверие со стороны потребителей и гарантируя их защиту от некачественных товаров. Поэтому наличие сертификата соответствия на медицинское оборудование необходимо и обеспечивает высокий уровень безопасности и качества для всех участников этого процесса.
Особенности сертификации и декларирования соответствия медицинских изделий
Важно знать, что каждый производитель медицинских изделий обязан иметь сертификат соответствия или декларацию о соответствии на свою продукцию. Эти документы гарантируют качество и безопасность медицинских изделий, а также защищают интересы пациентов и потребителей.
Существуют различные виды сертификатов и деклараций, зависящие от уровня риска, класса и назначения медицинского изделия. Общее требование для все типов сертификации — это прохождение испытаний на соответствие стандартам, установленным законодательством в сфере медицинских изделий.
Но не только производители обязаны следить за соответствием своей продукции, но и регуляторные органы. Они проводят проверки и аудиты, чтобы убедиться, что медицинские изделия соответствуют требованиям. В случае возникновении проблем с медицинским изделием, регуляторные органы принимают меры, чтобы свести риски к минимуму и обеспечить безопасность пациентов и потребителей.
Выводя на рынок медицинские изделия, обязательно проверяйте наличие сертификатов или деклараций о соответствии. Они гарантируют качество и безопасность продукции, а также могут предотвратить негативные последствия для потребителей.

Согласно решению Правительства Российской Федерации от 1 декабря 2009 года №982 (в новой редакции от 04.07.2020) был утвержден единый перечень продукции, которая должна быть сертифицирована, а также перечень продукции, соответствие которой подтверждается через подачу декларации о соответствии (с изменениями). Кроме того, Правительство Российской Федерации приняло решение от 4 июля 2020 года №982 об отмене определенных актов и положений, содержащих обязательные требования в отношении медицинских изделий, которые рассматривались при проведении мероприятий по государственному контролю за их использованием.
С начала 2021 года нет необходимости предоставлять сертификат соответствия или декларацию о соответствии для медицинских изделий.
Такие изделия исключены из "Единого перечня продукции, подлежащей обязательной сертификации" и "Единого перечня продукции, подтверждение соответствия которых осуществляется в форме принятия декларации о соответствии".
Оформление необходимых документов
Непросто разобраться во всех требованиях законодательства в области регистрации и сертификации соответствия медицинских изделий самостоятельно. Если Вы хотите сэкономить свое время, обратитесь в Центр регистрации медицинских изделий. Наши эксперты — опытные специалисты, которые помогут ответить на любые ваши вопросы. Мы предоставляем услуги регистрации и сертификации соответствия, а также поможем найти сертификат соответствия для медицинского оборудования иностранного производства, объясним, какие документы нужно собрать и сколько времени займет процесс. В нашей компании Вы сможете получить любую необходимую услугу, включая:
- организацию испытаний медицинских изделий в аккредитованной лаборатории с подготовкой соответствующих протоколов;
- Составление и оформление документов для регистрации;
- Поддержка процесса регистрации в Росздравнадзоре;
- Добровольная сертификация.
Процедура получения сертификата на медицинское изделие
Согласно действующему законодательству, обязательная сертификация медицинских изделий является соответствием стандартам и нормативам, утвержденным на уровне федеральных властей. Один из таких документов – ГОСТ 51609-2000 «Изделия медицинские. Классификация в зависимости от потенциального риска. Общие требования», который разделяет медицинские изделия на четыре типа, и основывается на трех принципах:
- Продолжительность контакта между изделием и пациентом;
- Степень и способ проникновения товара в тело человека;
- Лечебное, энергетическое воздействие на пациента.
Различают несколько классов МИ, которые обозначаются специальными символами: I, IIа, IIb и III. Чем больше цифра, тем выше риск использования изделия. Одно МИ может относиться только к одной категории:
- Класс I – низкий уровень опасности;
- Класс IIа – средний риск;
- Класс IIb – повышенный уровень опасности;
- Класс III – высокий уровень риска.
В зависимости от вида медицинского изделия применяются различные схемы сертификации. Заявитель, который хочет сертифицировать МИ класса I, имеет большую свободу действий. В этом случае можно использовать декларацию изготовителя. Однако для применения других схем сертификации производитель должен иметь систему качества.
При производстве стерильных изделий контроль за процессом стерилизации осуществляется в соответствии со стандартами по валидации процесса.
К сожалению, МИ класс I не может полностью соответствовать схемам европейских директив. Причина заключается в низком уровне отечественного производства и невозможности получения прямых поставок медицинских изделий. Из-за этого декларация не всегда может быть надежной.
Тем не менее, для повышения соответствия российской сертификации европейским директивам можно расширить использование на серийные партии. Для этого необходимо представить технический файл, который содержит следующие документы:
- Имя и адрес производителя;
- Идентификационные признаки изделия;
- Полное описание товара;
- Производственные и рабочие чертежи с разъяснениями;
- Компиляция списка правил и стандартов;
- Составление протоколов лабораторных испытаний;
- Создание руководства по качеству;
- Формирование описания процедур проверки в процессе изготовления.
Наш центр обеспечивает квалифицированную поддержку в проведении лабораторных исследований, оформлении сертификатов и деклараций, проверке и регистрации медицинских изделий:
- Мы готовы выводить продукцию на рынок в минимальное время;
- Берем на себя все вопросы по регистрации продукции;
- Проводим учет МИ в соответствии с правилами ЕАЭС;
- Предоставляем новым клиентам скидку 10%.
Вы можете позвонить нам по указанному на сайте номеру телефона или заполнить форму обратной связи, чтобы получить бесплатную консультацию и предварительный расчет.
Процедуры, входящие в процесс принятия декларации о соответствии, включают в себя следующее:
- Осуществление разработки и проверки документации в соответствии с нормами и техническими требованиями;
- Проведение испытательных процедур;
- Создание пакета доказательственных материалов;
- Принятие и засвидетельствование декларации о соответствии продукции.
Для наибольшей эффективности оформления декларации о соответствии, рекомендуется своевременно предоставлять органу сертификации копии регистрационного удостоверения на медицинский препарат или прибор.
В соответствии с ГОСТ Р, декларированию соответствия подлежат:
- Медицинская техника;
- Диагностические и терапевтические приборы;
- Контрольно-измерительные приборы;
- Хирургические материалы;
- Имплантаты для стоматологии и хирургии;
- Стоматологические материалы;
- Медицинские инструменты;
- Протезно-ортопедические изделия.
- изделия для медицинского применения, изготовленные из полимерных материалов;
Согласно ГОСТ Р, декларация о соответствии действительна в течение 3 лет. Маркировка знаком говорит о том, что медицинское изделие прошло процедуру декларирования соответствия:

Одним из распространенных заблуждений является убеждение, что сертификат соответствия на медицинское оборудование необходим только для тех устройств, которые продаются на международном рынке. Однако фактически сертификат соответствия является обязательным для любого оборудования, которое будет использоваться на территории Российской Федерации.
Еще одним заблуждением является мнение о том, что можно обойтись без сертификата соответствия, если оборудование не имеет прямого контакта с пациентом. На самом деле, все медицинское оборудование, независимо от того, какую функцию оно выполняет, должно иметь соответствующий сертификат.
Также часто ошибочно считается, что сертификация оборудования слишком дорогостоящая и сложная процедура. На самом деле существуют различные организации, которые могут помочь с получением сертификата соответствия по разумной цене и в кратчайшие сроки.
Важно помнить, что наличие сертификата соответствия на медицинское оборудование обеспечивает безопасность его использования, защищает пациентов и врачей от возможных проблем, а также позитивно сказывается на репутации компании-производителя.
Надо ли получать сертификат для медицинских устройств?
Для того, чтобы медицинское оборудование можно было производить и продавать, необходимо оформить регистрационное удостоверение Росздравнадзора (РУ). Это требование установлено ПП РФ №1416.
Во время оформления этого документа, оборудование подвергается тщательной проверке в испытательных лабораториях на соответствие всем показателям безопасности и эффективности.
Для измерительных приборов, таких как тонометры, кардиографы и весы, необходимо заказать свидетельство об утверждении типа средств измерений (СУТСИ).
После получения обязательного разрешения производители и импортеры могут заказать добровольный сертификат на медицинское оборудование.
Особенности получения регистрационного удостоверения
Необходимо указать, что процесс получения сертификата РУ является длительным и стоимым из-за выполнения комплексной проверки по влиянию изделия на организм человека.
Стоит отметить, что данное удостоверение не имеет срока действия и может быть использовано на всей территории Российской Федерации.
О процессе государственной регистрации и сертификации медицинских изделий
Регистрация товаров, относящихся к медицинской сфере, требует прохождения сложной процедуры проверки качества и безопасности. В случае соблюдения всех необходимых требований, продукт ставится на учет. Обязательное оформление сертификата осуществляет Росздравнадзор.
Заказать услугу Задать вопрос

Медицинские изделия, требующие обязательной регистрации
- Изделия для профилактики заболеваний и патологий;
- Изделия для диагностики;
- Изделия для лечения;
- Изделия для реабилитации;
- Изделия для предотвращения или прерывания беременности;
- Изделия для других медицинских целей.
Классификация по потенциальному риску
Медицинские изделия могут иметь разный уровень риска для здоровья пациента в зависимости от их сложности, области применения и других факторов. Классификация по потенциальному риску определяет степень возможного вреда, который может нанести изделие, даже если рекомендации по использованию были соблюдены. Существуют следующие классы:
- Класс 1 – низкий риск;
- Класс 2а – средний риск;
- Класс 2б – повышенный риск;
- Класс 3 – высокий риск.
Медицинские изделия, которые не требуют регистрации
Несмотря на то, что законодательство требует, чтобы практически все медицинские изделия были зарегистрированы, есть некоторые исключения. Согласно статье 38 пункту 5 Федерального закона 323-ФЗ, регистрация медицинского изделия не будет требоваться, если его назначение прямо связано с лечением конкретного пациента. Эти изделия изготавливаются с учетом характера заболевания и рекомендаций лечащего врача. Это снижает вероятность его использования другими пациентами, поэтому его не нужно регистрировать.
Процедура регистрации
С начала 2022 года Россия вместе с другими странами-участниками Евразийского экономического союза перешла на единые правила государственной регистрации и сертификации медицинских товаров. Все процессы регулируются решением Коллегии ЕЭК от 12.02.2016 № 46. По этому документу регистрация медицинских изделий в Росздравнадзоре состоит из нескольких этапов.
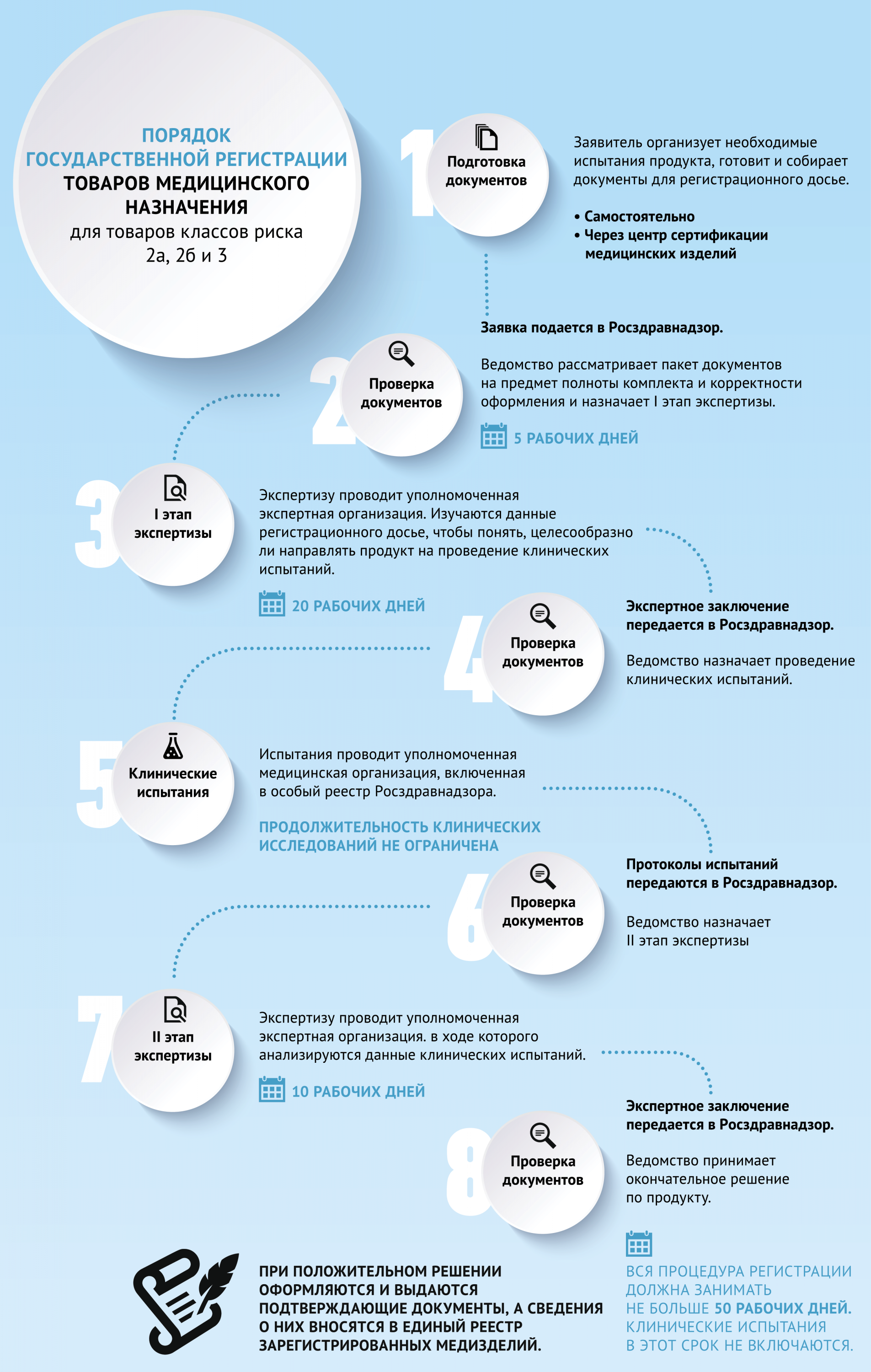
- Организация, подающая заявку на государственную регистрацию медицинского изделия, обязана провести необходимые испытания, собрать все нужные документы и составить полное регистрационное досье.
- Кроме того, заявитель должен выбрать референтное государство, где он будет подавать заявки на регистрацию изделия, и государства-участники, где его продукт может быть продан после получения регистрационного удостоверения.
- После того, как все документы готовы, заявитель подает регистрационное заявление и досье в Росздравнадзор.
- Эксперты ведомства тщательно изучают представленные документы и, если обнаруживают ошибки, требуют дополнительной экспертизы.
- Затем квалифицированные эксперты проводят тестирование продукта на соответствие регистрационному досье. По их результатам составляется экспертное заключение, которое передается в Росздравнадзор для принятия решения о госрегистрации изделия.
- Ведущие специалисты, прошедшие аккредитацию, проводят проверку оборудования, технологических процессов и других параметров в производстве медицинских изделий, чтобы гарантировать их соответствие установленным нормативам.
- Аккредитованная медицинская организация проводит клинические испытания, в ходе которых изучается качество, безопасность и эффективность продукта. Результаты испытаний оформляются в соответствии с протоколами и передаются в Росздравнадзор.
- Специалисты Росздравнадзора изучают полный пакет документов по продукту и, в случае положительной рекомендации, выданной медицинскими экспертами, размещают информацию в межгосударственной информационной системе для доступа сотрудников уполномоченных органов государств признания.
- Сотрудники государственных уполномоченных органов изучают документацию по продукту и принимают решение о возможности его регистрации.
- Затем Росздравнадзор производит государственную регистрацию продукта. Если результат оказывается положительным, работники органа выдают регистрационное удостоверение и вносят информацию о продукте в Единый реестр зарегистрированных продуктов.
Перечень сроков
Полная продолжительность процесса регистрации состоит из нескольких этапов:
- Процедура изучения документации на продукт и принятие решения о ее дальнейшей регистрации — 5 рабочих дней;
- Экспертиза регистрационного досье на протяжении 60 рабочих дней;
- Проверка производства продукта в течение 90 рабочих дней;
- Согласование экспертного заключения государственными уполномоченными органами в течение 30 календарных дней;
- Для регистрации продукции требуется 10 рабочих дней на принятие решения и еще 10 дней на оформление регистрационного удостоверения.
Размер государственной пошлины
Статьей 333.32.2 Налогового кодекса РФ установлены две государственные пошлины:
- тысяч рублей за выдачу регистрационного удостоверения;
- от 72 до 184 тысяч рублей в зависимости от класса риска изделия за проведение экспертизы.
Часто совершаемые ошибки при самостоятельной подаче документов
Часто заявители допускают ошибки при подаче документов в Росздравнадзор, такие как:
- неполный или неправильно оформленный пакет документов на изделие;
- Не проведение всех необходимых испытаний;
- Нарушение сроков подачи заявки;
- Отсутствие необходимой документации при запросе от ведомства;
- Другие ошибки, которые могут препятствовать успешной регистрации.
Преимущества работы с нашим центром
Наш уполномоченный центр «Безопасность» предоставляет помощь в регистрации медицинских изделий любой категории. Благодаря многолетнему сотрудничеству наших экспертов с Росздравнадзором в этой области, они знают все требования, действующие на сегодняшний день. Это гарантирует, что ваша заявка будет удовлетворена с первого раза, а вы сможете быстро пройти государственную регистрацию, вывести ваш продукт на рынок и занять достойное место среди ведущих производителей.
Наш центр специализируется на:
- регистрации медицинских изделий любой категории;
- помощи в прохождении государственной регистрации продукции;
- консультациях по соблюдению стандартов и требований в этой области.
Мы предлагаем профессиональную помощь, даже если вы не знаете, что нужно делать, чтобы зарегистрировать ваше медицинское изделие. Обратившись к нам, вы можете сэкономить время и избежать возможных штрафов.
Категории виновного лица:
- Санкции за производство или продажу медицинского изделия, не зарегистрированного — от 100 до 600 тысяч рублей или остановка работы до 90 суток.
- Санкции за продажу медицинского изделия, не зарегистрированного, через интернет — от 150 до 600 тысяч рублей или остановка работы до 90 суток.
- Санкции за нарушение регистрационных требований — от 1 до 5 миллионов рублей или остановка работы до 90 суток.




