Для проверки сертификации медицинского оборудования необходимо обратить внимание на наличие маркировки CE, которая свидетельствует о соответствии продукции европейским стандартам безопасности и качества. Также важно удостовериться, что устройство имеет сертификат качества от аккредитованного органа по сертификации.
В следующих разделах статьи мы расскажем о процессе сертификации медицинского оборудования, о том, какие стандартные требования должны быть выполнены для получения сертификата, а также об основных преимуществах использования сертифицированного оборудования в медицинских учреждениях. Узнайте, почему правильный выбор оборудования может способствовать повышению безопасности пациентов и улучшить качество оказываемой медицинской помощи.
- Проверьте наличие маркировки CE на оборудовании. Эта маркировка обозначает соответствие изделия европейским стандартам безопасности и качества.
- Удостоверьтесь, что оборудование имеет сертификат качества, выданный аккредитованным органом по сертификации.
- Просмотрите документацию к оборудованию: инструкции по эксплуатации, сертификаты соответствия, гарантийные документы. Вся эта информация должна быть на официальном языке производителя и содержать подпись ответственного лица.
- Обратитесь к официальному представителю производителя оборудования или к дистрибьютеру, чтобы уточнить информацию о сертификации продукции.
- Проведите тестирование оборудования на соответствие заявленным характеристикам и безопасности работы. В случае сомнений обратитесь к квалифицированному специалисту или сервисному центру.
Реестр зарегистрированных медицинских средств
Для того чтобы найти информацию о зарегистрированных медицинских средствах, нужно ввести в строку поиска соответствующий запрос, такой как название медицинского средства, регистрационный номер или тип медицинского средства. Если вы хотите уточнить критерии поиска, вы можете воспользоваться кнопкой "Расширенный поиск".
Информация в этом разделе предоставляем пользователю для ознакомления и удобства. Компания "Невасерт" не имеет ответственности за достоверность данной информации. Для получения точной информации рекомендуем использовать официальный реестр Росздравнадзора.
Обновлено 31.03.2024 г.
Проверка наличия регистрационного удостоверения для медицинских средств в реестре
Федеральная служба по надзору в области здравоохранения (Росздравнадзор) отвечает за ведение Единого государственного реестра зарегистрированных медицинских изделий в соответствии с новыми правилами. Порядок ведения, проверки и обновления информации утвержден приказом ведомства от 6 мая 2019 года N 3371. Он обеспечивает возможность проверки регистрационного удостоверения на медицинские изделия в этой информационной базе за несколько минут, доступной на портале контролирующего ведомства.
На данный момент в реестре зарегистрировано более 70 тысяч медицинских изделий, обновляемых постоянно, поскольку производители товаров медицинского назначения подают заявки на проверку в Росздравнадзор и получают удостоверения регистрации. В реестре можно проверить информацию о медицинских изделиях различных категорий.
Как эксперт в области медицинской техники, я хотел бы поделиться своим мнением о том, как проверить, сертифицировано ли медицинское оборудование. Для начала, важно убедиться, что устройство имеет соответствующий сертификат качества и безопасности, выданный аккредитованным органом.
Также стоит обращать внимание на маркировку оборудования, наличие инструкции по эксплуатации на русском языке, а также наличие гарантии от производителя. Эти документы являются неотъемлемой частью сертификации и гарантируют качество устройства.
Другим важным аспектом является проверка актуальности сертификата. Сертификация медицинского оборудования подвергается регулярным проверкам и обновлениям, поэтому важно удостовериться, что сертификат не устарел и соответствует текущим стандартам и требованиям.
В целом, для проверки сертификации медицинского оборудования необходимо внимательно изучить предоставленные сертификаты и документацию, обратить внимание на маркировку и гарантийные условия. Это поможет удостовериться в качестве и безопасности приобретаемого оборудования.
Данные, которые представлены в едином государственном реестре зарегистрированных медицинских изделий
В Едином государственном реестре содержится обширная информация о зарегистрированных медицинских изделиях. Для каждого изделия доступен список данных, который может быть проверен:
- код записи о продукте в реестре;
- номер регистрации медицинского изделия в соответствии с выданным регистрационным удостоверением;
- дата осуществления государственной регистрации в Росздравнадзоре;
- срок действия регистрационного удостоверения;
- название медицинского изделия, получившего регистрационное удостоверение;
- название организации, которая представляет интересы производителя в процессе государственной регистрации. Бывает так, что изготовитель медицинского товара выступает в этой роли;
- местоположение этой организации.
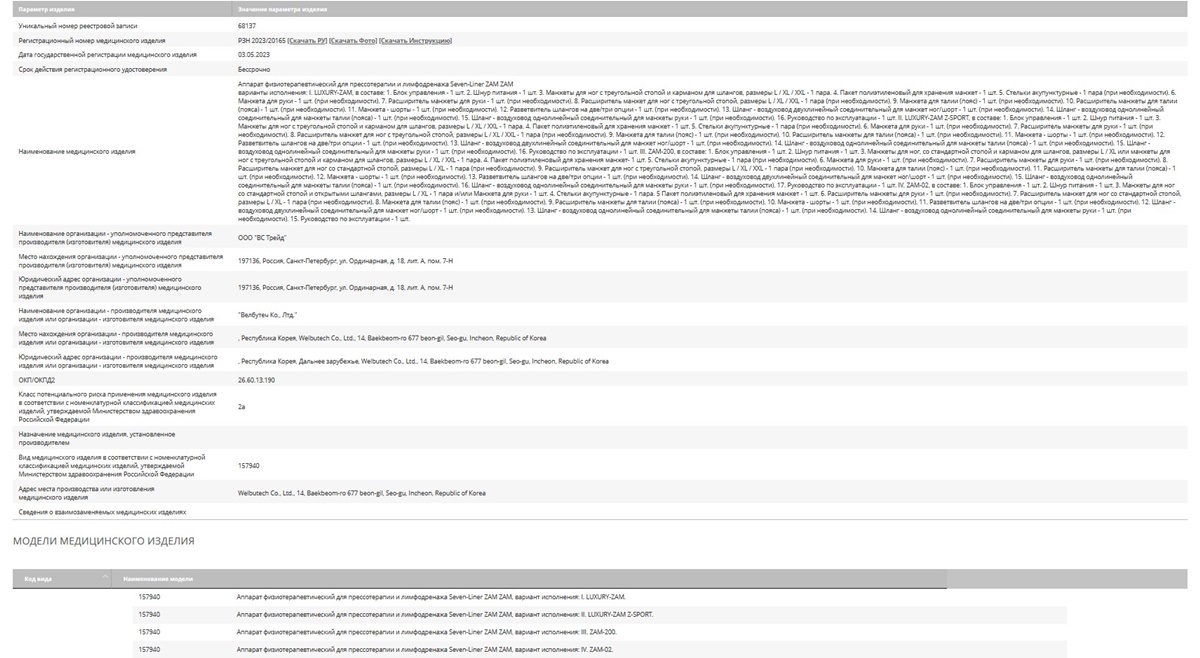
Третий этап. Ознакомьтесь с основными данными из регистрационного удостоверения в виде таблицы
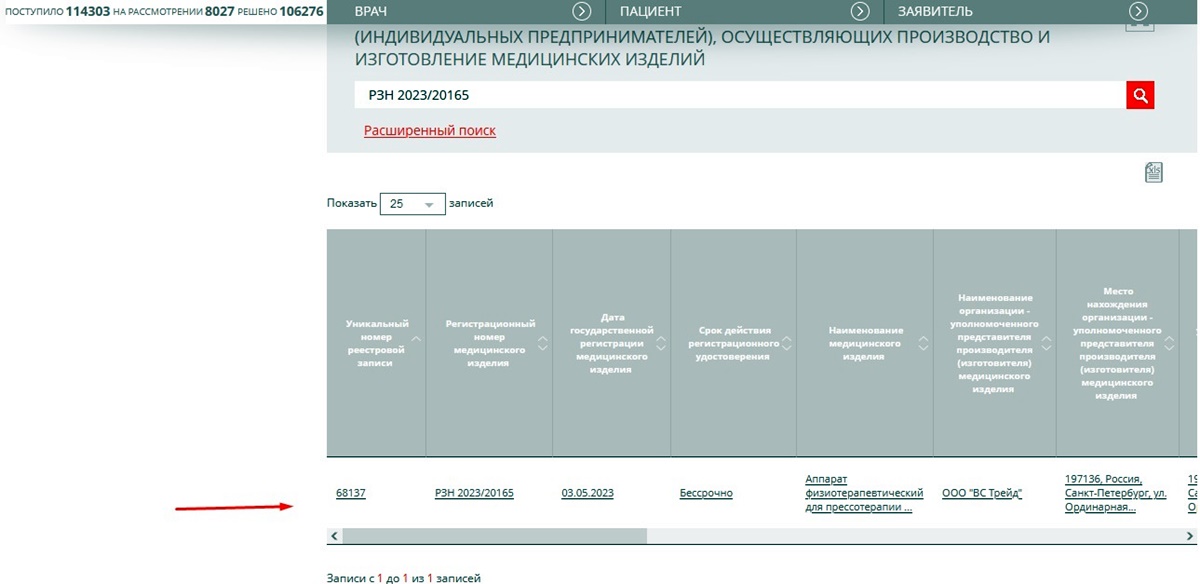
При правильном указании номера РУ или названия медтехники, под строкой поиска появится таблица, содержащая основные данные и pdf-файл с выпиской из реестра для скачивания. Если провести поиск РУ для массажеров Welbutech, то можно получить следующую информацию:
Если вам требуется более подробная информация из России, выберите пункт из таблицы. На странице вы найдете расширенные сведения о медицинском оборудовании, а также сможете получить сведения о моделях, зарегистрированных на рынке, загрузить фото, инструкции на русском языке и регистрационные удостоверения.
Здесь представлена реклама ИП Чиликин Максим Николаевича с указанием ИНН 780157890802.
Настоящая статья призвана информировать читателей и не может заменить консультацию квалифицированного специалиста. Мы рекомендуем не заниматься самолечением и обратиться к врачу при любых неудобствах. Отмечаем, что материалы, размещенные на сайте www.maxmassage.ru защищены законодательством РФ об охране результатов интеллектуальной деятельности и являются собственностью ИП Чиликина Максима Николаевича. Их использование другими лицами в любой форме возможно только с разрешения правообладателя или с прямой ссылкой на источник (если это предусмотрено законодательством).
В статье даны следующие сведения о товарах:
Как правильно работать с реестром лицензий на медицинское оборудование?
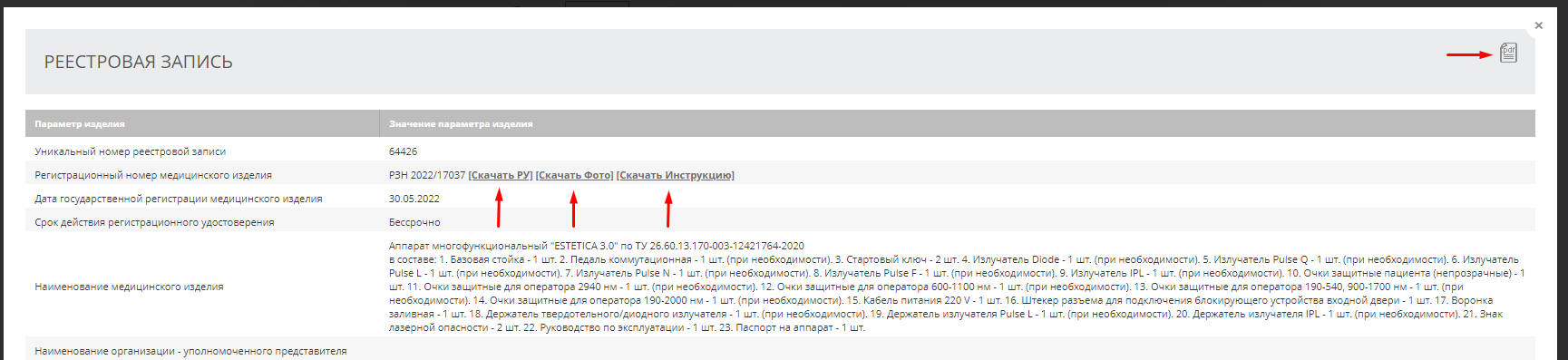
Необходимо обращать внимание на следующие факторы:
- Название медицинского устройства
- Комплектацию, указанную в регистрационном удостоверении – РАЗНЫЕ ВАРИАНТЫ ИСПОЛНЕНИЯ
Например, в реестре содержатся сведения о двух многофункциональных платформах, которые были произведены одной компанией.
Названия очень похожи, имеются одинаковые слова в названии.
Первая платформа:
Многофункциональный прибор FORYOU
Наименование компании — уполномоченного представителя производителя (изготовителя) медицинского изделия – ООО «РОМАШКА»
Наименование компании — производителя медицинского изделия или организации — изготовителя медицинского изделия – FORYOU Ltd.
Форма для нанесения FORYOU А
Форма для нанесения FORYOU Б
Форма для нанесения FORYOU В
Вторая платформа:
Косметологический прибор FORYOU 1.0
Наименование организации, которая является уполномоченным представителем производителя медицинских изделий – ООО «РОМАШКА».
Наименование организации, которая специализируется на производстве или изготовлении медицинских изделий – FORYOU Ltd.
Существуют три варианта аппликатора от FORYOU: А, Б и В.
Потому что все три аппликатора были созданы одним и тем же производителем, платформа «Аппарат многофункциональный FORYOU» может работать с любым из них, если они зарегистрированы в «Аппарате косметологическом FORYOU 1.0».
К сожалению, согласно законодательству, каждый аппликатор и каждая платформа трактуются как отдельное медицинское изделие, и их нельзя использовать в произвольной комбинации.
Презумпция соответствия и принцип «подцепил и работает» – это серьезные нарушения, связанные с обращением медицинских изделий.
Производитель не предусмотрел использование аппликаторов других медицинских изделий в официальной инструкции!
Будьте внимательны! Не позволяйте недобросовестным продавцам ввести вас в заблуждение.
Одним из распространенных заблуждений на тему проверки сертификации медицинского оборудования является уверенность в том, что наличие этикетки или пометки «сертифицировано» автоматически гарантирует соответствие изделия стандартам безопасности и качества. Однако это не всегда так, и многие подделки могут иметь ложные маркировки.
Другим заблуждением является уверенность в том, что высокая цена медицинского оборудования автоматически означает его сертификацию. В действительности, цена оборудования может зависеть от многих факторов, включая бренд, технические характеристики и другие аспекты, не обязательно связанные с сертификацией.
Также нельзя полагаться только на слова продавца или производителя оборудования о его сертификации. Важно самостоятельно проверять соответствие сертификации, обращая внимание на документы, прилагаемые к изделию, а также наличие необходимых разрешительных документов и маркировок.
Итак, чтобы быть уверенным в сертификации медицинского оборудования, необходимо внимательно изучать документацию, проверять подлинность маркировок и брендов, а также обращаться к официальным источникам для подтверждения соответствия стандартам качества и безопасности.
Оценка соответствия медицинских изделий при государственной регистрации
Согласно пункту 5 Правил государственной регистрации медицинских изделий (далее – МИ), утвержденных Постановлением Правительства РФ от 27.12.2012 № 1416, государственная регистрация МИ проводится на основе результатов проведенных испытаний и исследований, таких как:
- Технические испытания – проверка соответствия характеристик (свойств) МИ требованиям нормативной документации, технической и эксплуатационной документации производителя (изготовителя) и принятие решения о возможности проведения клинических испытаний;
- Исследования, проводимые с целью оценки безопасности и возможности проведения клинических испытаний медицинского изделия, называются токсикологическими.
- Для оценки безопасности и эффективности медицинского изделия включая участие людей в качестве субъектов, проводятся специально разработанные и запланированные клинические испытания.
Согласно Постановления Правительства РФ №1416, оценка соответствия медицинских изделий проводится в виде вышеупомянутых видов испытаний, учитывая классификацию в зависимости от потенциального риска использования продукции.
Для того чтобы зарегистрировать медицинское изделие, необходимо следовать установленному порядку проведения ОС. Это заявлено в Приказе Минздрава России от 09.01.2014 № 2н. В соответствии с данным порядком, необходимо провести технические испытания для всех медицинских изделий. Однако существует различие в порядке проведения таких испытаний для изделий in vitro и для других медицинских изделий.
Для токсикологических исследований существует правило: их необходимо проводить только в отношении тех изделий, которые контактируют с организмом человека в процессе использования в соответствии с назначением производителя (пункт 25 Порядка). Однако, необходимо быть осторожным. Медицинское программное обеспечение не контактирует с организмом человека, но оно записывается на материальные носители. На практике, Росздравнадзор требует проведения токсикологических исследований, чтобы получить разрешение на использование таких носителей, как флешки, диски и т.д.
Лаборатории, проводящие токсикологические исследования и технические испытания, должны иметь аккредитацию по установленным правилам.
Клинические испытания — это еще один способ проверки соответствия медицинских изделий. Они используются для всех видов МИ, включая in vitro, и учитывают их особенности. КИ могут проводиться путем анализа данных и оценки уже существующих результатов, либо с помощью проведения испытаний на людях. Обязательное участие человека в КИ предусмотрено в следующих случаях (п. 37 Порядка):
- а) при разработке нового вида медицинского изделия;
- б) при использовании новых сложных и (или) уникальных и (или) специальных методов профилактики, диагностики и лечения заболеваний и состояний, а также при использовании новых сложных медицинских технологий;
- Если проведенный анализ клинических данных не подтверждает эффективность и безопасность медицинского изделия, то оно не может быть одобрено.
Компании, занимающиеся медицинской деятельностью, могут получить право на проведение клинических испытаний, если им это разрешит Росздравнадзор.
Чтобы узнать подробнее о процессе оценки соответствия медицинских изделий во всех формах, необходимо обратиться к следующим статьям:
- Методы технических испытаний медицинских изделий;
- Результаты токсикологических исследований медицинских изделий;
- Организация и проведение клинических испытаний медицинских изделий.
Оценка соответствия законодательству о техническом регулировании медицинских изделий
Для некоторых видов товаров, которые продаваться на территории РФ, необходимо иметь документы, подтверждающие их соответствие техническим регламентам. Это может быть декларация о соответствии или сертификационный сертификат.
Чтобы получить декларацию или сертификат, товар должен пройти проверку на соответствие техническим регламентам. Правительством РФ устанавливаются перечни товаров, которые подлежат обязательной сертификации и декларированию соответствия, и эти перечни регулярно обновляются (статья 46 Федерального закона от 27.12.2002 № 184-ФЗ «О техническом регулировании»).
Для медицинских изделий отсутствует соответствующий технический регламент, в связи с чем необходимо обратиться к Постановлению Правительства РФ от 01.12.2009 № 982, чтобы определить, нуждается ли МИ в обязательном декларировании или сертификации. Например, «Перчатки медицинские диагностические одноразовые», «Изделия медицинские из латекса, медицинские клеи», «Перчатки хирургические» и др. обязаны получить декларацию.
В некоторых случаях, помимо свидетельства о государственной регистрации, медицинское изделие также должно иметь сертификат и/или декларацию соответствия. К тому же, производитель может пройти сертификацию в добровольном порядке, чтобы подтвердить качество своей продукции (декларирование в добровольной форме не предусмотрено).
Нормативы:
Каждое медицинское изделие должно соответствовать требованиям безопасности. Вы можете ознакомиться с перечнем действующих нормативных документов в таблице, размещенной в Системе Главного врача.
Надзорные органы проверяют регистрацию медицинских изделий, указанных в лицензии медучреждения, и их использование при оказании медицинской помощи пациентам.
Если перечень оборудования не соответствует требованиям Минздрава, такое нарушение будет рассматриваться экспертами.
Следует помнить, что медицинские изделия включают в себя приборы, аппараты, инструменты и материалы, а также специальное программное обеспечение, предназначенное для оказания медицинской помощи.
Комплексное оборудование и аппаратура нуждаются в техническом обслуживании.
Узнайте систему мониторинга безопасности медицинских препаратов, созданную экспертами Справочной Системы Главного врача. Получите доступ к шаблонам необходимых документов.

Чтобы оформить обслуживание медицинских изделий, необходимо предоставить 5 документов:
- Регистрационное удостоверение от Росздравнадзора, подтверждающее соответствие медицинского изделия стандартам качества и безопасности. Важно убедиться, что данное изделие выпущено в период действия удостоверения.
- Копия декларации или сертификата соответствия, выдаваемых органом по сертификации.
- Копия удостоверения на медицинское изделие об утверждении типа средства измерений, если в изделии присутствует встроенный прибор для измерения или оно является средством измерения. Этот документ выдаётся Росстандартом.
- Свидетельство о первичной поверке.
- Эксплуатационные документы на медицинское изделие.
Кроме того, могут потребоваться следующие документы:
- Паспорт медицинского изделия.
О сертификации медицинских изделий
В соответствии с федеральным законом № 323 «Об основах охраны здоровья граждан в РФ» от 21.11.2011 года, медицинскими изделиями считаются:
- инструменты, приборы, аппараты и оборудование, которые используются в сфере здравоохранения;
- материалы и подобные изделия, которые применяются в медицинских целях;
- специальное программное обеспечение для проведения исследований, диагностики, реабилитации и лечения.
Медицинские изделия классифицируются по виду продукции и делятся на следующие группы:
- класс 1 (например, микроскопы и весы);
- класс 2а (например, спирометры и лабораторное оборудование);
- класс 2б (например, кардиоанализаторы и дефибрилляторы);
- класс 3 (например, имплантаты и эндопротезы).
Важными компонентами сертификации медицинских изделий являются методика поверки изделий и руководство по эксплуатации.
Минздравсоцразвитие является органом, который проводит сертификацию продукции на соответствие требованиям безопасности и качеству. Кроме того, этот орган регламентируется приказом №735 от октября 2006 года. Аккредитация лабораторий и сертифицирующей организации обязательна для проведения процедуры, и это занимает на себя специализированная федеральная служба.
В случае, если товар является медицинским изделием и требуется сертификат безопасности, выдается Регистрационное удостоверение Минздравом. Для получения разрешительной бумаги при таможенном контроле, товар должен соответствовать Порядку ввоза МИ, установленному приказом №7н Минздрава.
Обязательная сертификация медицинских изделий в системе ГОСТ Р
Почти все медицинские товары в наше время должны пройти сертификацию в соответствующих органах. Удостоверение соответствия ГОСТам выдается следующим видам продукции:
- изделия из латекса и клея;
- изделия из резины (например, клеенки, трубки, шланги);
- бумага для медицинских целей и изделия из нее;
- мебель для медицинских учреждений;
- материалы для перевязок;
- компрессионные, эластичные и фиксирующие изделия;
- законно зарегистрированные лекарства;
- медикаментозные препараты;
- витамины для животных;
- витаминные комплексы для людей;
- протезы и ортопедические изделия;
- сыворотки и вакцины для животных;
- медицинские инструменты и шприцы;
- упаковка для лекарственных препаратов.
Требование к получению сертификата соответствия на медицинские материалы по–прежнему остается актуальным для тех, которые не указаны ниже:
- гамма–глобулины;
- сыворотки;
- иммуноглобулины;
- материал из крови;
- анатоксины;
- вакцины;
- токсины.
Наша компания специализируется на получении необходимых деклараций и разрешительных документов для медицинских изделий. Мы предоставляем помощь в получении сертификатов соответствия ГОСТ Р, ТР ТС 020/2011 и других документов в течение 1 дня. Заполните форму обратной связи или закажите звонок, и наши менеджеры свяжутся с вами в ближайшее время.
Как в мире проходит одобрение медицинских материалов?

Практически в каждой более-менее цивилизованной стране контроль за оборотом медицинской продукции является неотъемлемой частью ее функций. Развитая система техрегулирования в США, Европе и Азиатско-Тихоокеанском регионе гарантирует высокий уровень безопасности всей продукции.
Государственное регулирование оборота медицинских изделий это мощный инструмент воздействия на рынок, подтвержденный международным опытом. В Евросоюзе существует принцип добровольности, предоставляя производителям медицинских изделий свободу в создании своих собственных стандартов. Однако, необходимость в доказательной базе может стать дорогой ценой за такую свободу.
Существует только две глобальные системы контроля на медицинское оборудование, одна – европейская, другая – американская. Обе системы могут использоваться в качестве аналогов, но без тщательного внимания к деталям, мало что может получится, как бы вы не старались. Теперь рассмотрим каждый подход более подробно.
Контроль в США
Вся работа по контролю качества выполняется Федеральным управлением по контролю качества (FDA) и основана на законодательстве. FDA – это не частная компания, а государственная, которая имеет прекрасное взаимодействие с Министерством здравоохранения США. Благодаря этому существует отличная научно-техническая база и высококвалифицированные специалисты. Также имеется высокий уровень оценки потенциальной угрозы медицинского изделия, оперативной разработки норм и правил и защиты здоровья человека. Финансирование FDA осуществляется из бюджета страны.
Европейский контроль
В Европе существует единая система контроля качества медицинского оборудования. Согласно европейскому законодательству, медицинское оборудование оценивается в соответствии с установленными нормами. Система финансируется за счет платежей производителей.
Директивы содержат правила, описывающие множество медицинских изделий. Среди них две регулируют выпуск медицинских изделий и их использование при взаимодействии с пациентами. Эти директивы являются основой для разработки норм и правил. Без документа соответствия ни один продукт не может быть использован в европейских странах.
Кроме того, каждое государство должно регулировать деятельность производителей медицинских изделий, чтобы минимизировать возможные риски.
При сравнении систем ЕС и России можно выделить два принципиальных отличия:
- В Европейской системе контроль является цельным характером и описывается в одном документе. В России разделены сертификация и разрешительная документация.
- В Европе тесно связаны жесткий надзор и категоризация групп риска, поэтому процесс сертификации медицинского оборудования является эффективным и оправданным в глазах общественности.
Процедура сертификации медицинской техники в России
Процедура получения СС включает в себя следующие этапы:
- Выбор организации, которая будет проводить услугу;
- Отбор примеров оборудования для проведения испытаний;
- Проведение тестовых испытаний для выбранных примеров;
- Составление протокола;
- Формирование пакета документов;
- Принятие решения о выдаче разрешительного документа;
- Выдача СС и занесение информации в единый реестр.
Перечень необходимых испытаний зависит от типа техники и степени ее опасности.
Какие документы следует подготовить для сертификации медицинской техники?
Для проведения процедуры сертификации необходимо подготовить следующие материалы:
- Предоставление нотариально заверенных копий учредительных и регистрационных документов;
- Описание состава медицинских устройств и механизмов;
- Технические данные и документы на медицинское оборудование;
- Предоставление паспорта медицинского оборудования;
- Протоколы проведенных испытаний на медицинское оборудование;
- Инструкции по эксплуатации медицинского оборудования;
- Документальное подтверждение права собственности на производственную площадь (в случае аренды — предоставление соответствующего договора);
- Наличие сертификатов, регистрационных удостоверений и других документов подтверждающих соответствие медицинского оборудования требованиям безопасности и качества;
- Наличие контрактов на поставку медицинского оборудования (копии);
- Сопроводительные документы к медицинскому оборудованию;
- Иные имеющиеся документы.
Срок действия сертификата на медицинское оборудование
Справка о соответствии (СС) имеет срок действия в 1 или 3 года в зависимости от выбранной схемы оценки. Для партии товаров срок действия не устанавливается и действует до момента окончания реализации указанной партии. В это время возможны проверки организации и оценка производственного процесса с целью убедиться, что изготовитель соответствует государственным стандартам.
По истечении срока действия документа заявитель может подать заявку на продление. Справка о соответствии действительна на всей территории России.




