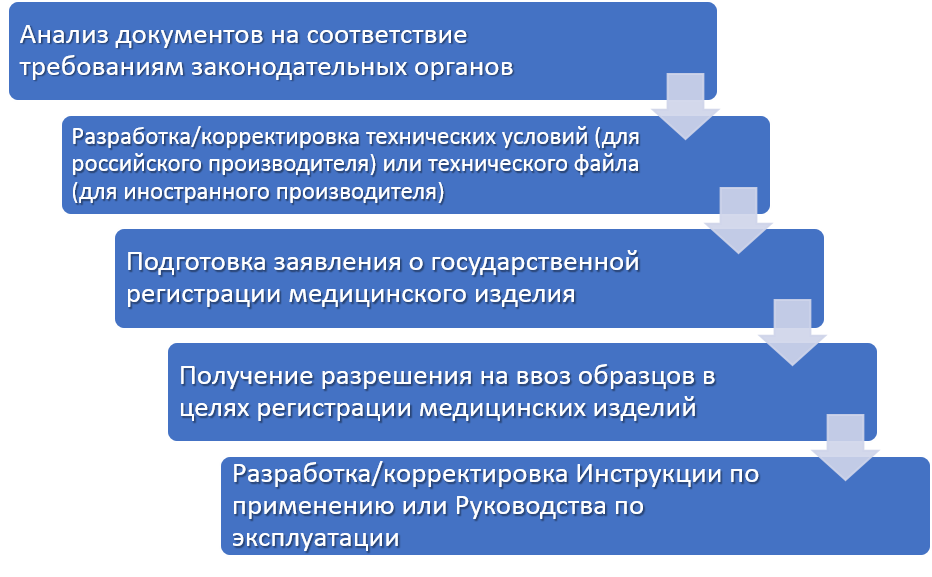
Для получения регистрационного удостоверения на медицинское оборудование необходимо обратиться в Федеральную службу по надзору в сфере здравоохранения.
В следующих разделах статьи мы рассмотрим требования к документации, необходимой для получения регистрационного удостоверения, процедуру подачи заявки, а также основные этапы испытаний и проверок медицинского оборудования перед его введением на рынок.
- Определите категорию медицинского оборудования, для которого требуется получить регистрационное удостоверение.
- Соберите необходимый пакет документов, включающий техническую документацию, сертификат качества, данные о производителе, инструкцию по эксплуатации.
- Обратитесь в Федеральную службу по надзору в сфере здравоохранения (Росздравнадзор) для начала процедуры регистрации оборудования.
- Пройдите необходимую экспертизу оборудования, проведенную уполномоченными организациями.
- Оплатите государственную пошлину за регистрацию медицинского оборудования.
- Получите регистрационное удостоверение, подтверждающее соответствие вашего оборудования требованиям законодательства и стандартам качества.
Получение удостоверения о регистрации в соответствии с законодательством РФ
В соответствии с пунктом 4 статьи 38 Федерального закона "Об основах охраны здоровья граждан в Российской Федерации" от 21 ноября 2011 года № 323-ФЗ, в Российской Федерации разрешено использование медицинских изделий, зарегистрированных в соответствии с порядком, установленным уполномоченным федеральным органом исполнительной власти Правительством РФ.
Государственная процедура регистрации медицинских изделий (МИ) разработана с целью обеспечения доступа на рынке лишь высококачественных, эффективных и безопасных изделий. Получение регистрационного удостоверения (РУ) является основным документом, подтверждающим соответствие МИ требованиям и факт их регистрации на территории России. Регистрация МИ в РФ — условие необходимое для их ввоза, производства, использования и продажи на рынке.
Федеральная служба по надзору в сфере здравоохранения РФ (Росздравнадзор) отвечает за регистрацию медицинских изделий (МИ) на территории России. Для процедуры государственной регистрации, Росздравнадзор отправляет регистрационное досье МИ на экспертизу качества, безопасности и эффективности в одну из подведомственных организаций.
Компания ООО «ССМК» предоставляет подготовку регистрационного досье (РД) в соответствии с законодательством и Правилами регистрации.
В настоящее время, помимо государственной регистрации, МИ могут быть зарегистрированы в соответствии с решением Совета ЕЭК от 12.02.2016 №46, если они получили регистрационное удостоверение по правилам ЕАЭС. В этом случае МИ могут быть обращены на территории других стран Евразийского экономического союза.
Комплект документов, необходимый для регистрации медицинских изделий – процесс подготовки регистрационного досье.


Получение регистрационных удостоверений на медицинские изделия занимает различное время, в зависимости от класса риска МИ, выбранной схемы регистрации, объема документации и требуемого объема испытаний. Мы стараемся обеспечить оперативное регистрирование изделий, выполняя этапы процедуры параллельно в тех случаях, где это возможно, чтобы сократить время ожидания. Сокращенные сроки подготовки РД начинаются от 1,5 месяцев и зависят от быстроты предоставления требуемой информации, документации и образцов. Среднее время подготовки РД составляет 3-4 месяца.
Сроки рассмотрения регистрационного досье в РЗН:


Документы, необходимые для регистрации медицинских изделий:
Для процесса регистрации медицинских изделий следует подготовить комплект документов, включающий:
Для местного производства изделий:
- Копии ИНН, ОГРН, выписка из ЕГРЮЛ;
- Нотариально заверенная доверенность на полномочия заявителя;
- Сертификат соответствия СМК (при наличии);
- Доказательства места производства изделий;
- Пояснительная записка (ПЗ) (в случае наличия, в противном случае выполнение ПЗ);
- Характеристика регистрируемой продукции;
- Индекс регистрируемых продуктов;
- Основные условия эксплуатации (в случае наличия, в противном случае выполнение).
- При наличии — предоставляем акт квалификационных испытаний;
- Для получения фотографий зарегистрированного изделия, в случае отсутствия образцов, мы выполняем их в собственном исполнении;
- Подбираем нужное количество образцов медицинского изделия в зависимости от типов и объема требуемых испытаний;
- Для зарубежного изделия требуется предоставление следующих документов:
- Документ о регистрации производителя как юридического лица в стране производства;
- На основании иметющихся сертификатов ISO 13485, ISO 9001, а также отчет об аудите, подтверждаем качество изделия;
- Предоставляем доверенность на нашего УПП для представления интересов производителя на территории Российской Федерации;
- Осуществляем проверку условий производства, включая наличие бизнес-лицензии;
- При наличии технического файла изделия, мы изучим его содержание и, в случае отсутствия, выполним разработку необходимой документации.
- При наличии эксплуатационной документации, она включается в список требуемых документов. В противном случае, мы разрабатываем ее сами.
- Если у нас есть образцы регистрируемого изделия, мы делаем фотографии сами. Если нет — раздобыть образцы.
- Для проведения испытаний мы подбираем определенное количество образцов медицинского изделия, соответствующих его типу и объему требуемых испытаний.
- После проведения испытаний мы составляем отчеты о результатах, которые предоставляем в виде тест-репортов.
- Файл менеджмента рисков также прилагается к списку требуемых документов.
- Отчеты о валидации, верификации и стабильности упаковки МИ — также обязательная часть списка документов, но конкретный список формируется в зависимости от требований к виду МИ в ходе анализа.
Перечень документов, необходимых для регистрации медицинских изделий, может меняться в зависимости от разнообразия классов риска, функциональных особенностей и степени сложности МИ.
Получив положительный ответ от федеральной службы, мы оформляем регистрационное удостоверение и соответствующее приложение к нему.
Наша компания оказывает помощь в ведении вашего медицинского проекта на всех его этапах, включая профессиональную подготовку документации, решение возникших замечаний и подготовку аргументированных ответов на запросы экспертов.
Вы можете направить нам запрос и наши специалисты по регистрации внимательно изучат ваши данные, подберут наиболее оптимальный способ регистрации, оценят необходимый объем работ по подготовке документов и предложат коммерческое предложение для выполнения работ.
Получение регистрации для изделий медицинского назначения
В России обязательна процедура регистрации медицинских изделий, которая была введена для обеспечения контроля качества и безопасности продукции, которая поступает и реализуется на рынке. Эта процедура гарантирует, что товары, которые предлагаются на рынке, эффективны в использовании и не представляют угрозы для жизни людей.
Подтверждением факта регистрации медицинского изделия является регистрационное удостоверение Росздравнадзора, выданное в соответствии с постановлением правительства РФ от 27 декабря 2012 года № 1416. Срок действия этого удостоверения не ограничен.
Для продажи медицинских изделий на территории РФ необходимо получить регистрационное удостоверение Росздравнадзора. Отсутствие этого документа может привести к незаконным действиям при использовании этих изделий.
Для получения регистрационного удостоверения на медицинское оборудование необходимо следовать определенным правилам и процедурам, установленным законодательством. В первую очередь, необходимо подготовить и предоставить все необходимые документы, подтверждающие качество и безопасность продукции.
Далее следует обратиться в уполномоченный орган по регистрации медицинского оборудования, который проведет экспертизу предоставленных документов и самого оборудования. Тщательная проверка качества и соответствия стандартам играет решающую роль в процессе получения регистрационного удостоверения.
Кроме того, необходимо учитывать особенности законодательства страны, в которой планируется регистрация медицинского оборудования, так как требования и процедуры могут отличаться в зависимости от региона.
Важно помнить о необходимости соблюдения всех процедур и требований при оформлении регистрационного удостоверения на медицинское оборудование, так как это гарантирует безопасность и качество продукции для конечных потребителей.
Процесс регистрации медицинских изделий в РФ и сопровождение всех этапов оформления регистрационных удостоверений
Мы предлагаем полный комплекс услуг по сопровождению процесса регистрации медицинских изделий на территории РФ, включая оформление регистрационных удостоверений на всех этапах. Наши специалисты окажут необходимую помощь в сборе и подготовке необходимой документации, а Взаимодействии с регулирующими органами.

Создание документации технического и эксплуатационного характера для медицинских устройств
Развертывание технических, токсикологических и ЭМС-испытаний
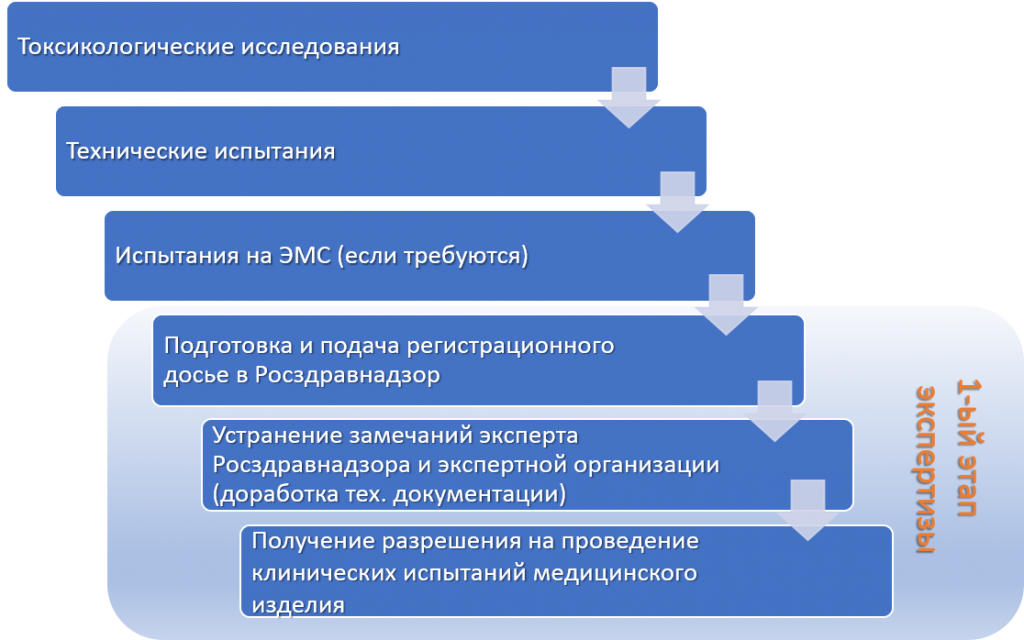
Осуществление клинических исследований
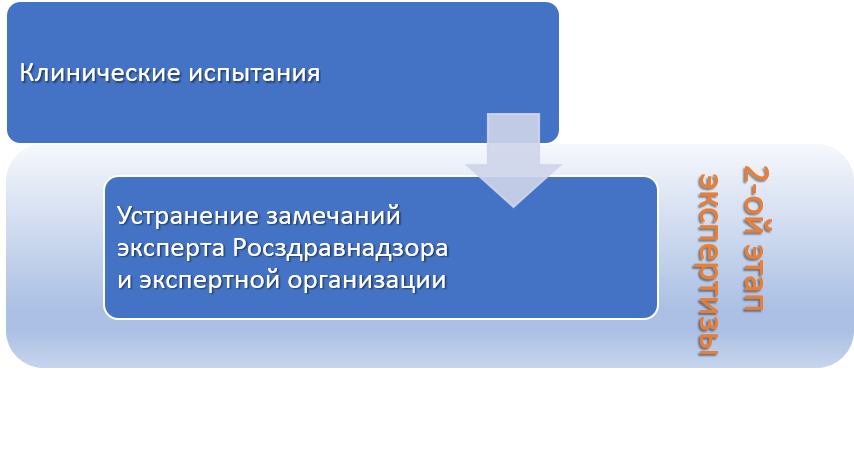
Получение подлинного РУ документа
Для того, чтобы получить подлинную копию РУ документа, необходимо следовать определенным правилам и процедурам. Одним из важных этапов является заполнение заявки на выдачу РУ документа. Необходимо указать точное название документа, номер, дату выдачи, а также данные о самом заявителе.
Заявку на получение подлинного РУ документа можно подать как лично, так и через представителя. В некоторых случаях может потребоваться предоставление дополнительных документов и сведений, например, копии паспорта или свидетельства о рождении, а также платеж для оплаты услуг.
Следует заметить, что получение подлинного РУ документа может занять некоторое время, и некоторые документы могут не подлежать выдаче. В любом случае, следует следовать процедурам и заявляться только по настоящим причинам и основаниям, чтобы избежать проблемных ситуаций.
Список необходимых документов, требуемых для оформления регистрационного удостоверения иностранными компаниями
- Свидетельство о регистрации изготовителя
- Документы, подтверждающие условия производства изделий медицинского назначения (сертификат / декларация соответствия требованиям СЕ 93/42 или СЕ 98/79, а также сертификаты стандартов ISO 13 485), а также документы, подтверждающие соответствие изделий стандартам качества и безопасности (национальные сертификаты контроля качества продукции, сертификаты свободной продажи и декларации / сертификаты соответствия для медицинских изделий, классифицированных в риске 1 или 2a, а также 2б и 3)
- Нотариально заверенная доверенность, выданная российским заявителем
- Руководство по эксплуатации
- Технический документ или техническая спецификация
Отзывы
Свежие новости
Перечень актуальных ОКПД 2
Министерство здравоохранения выяснило, как подтвердить товарный знак при регистрации медицинских изделий
Нужно ли такое Евразийское экономическое сообщество в медицинской промышленности?
КАК ВЫГЛЯДИТ?
Сертификат гарантирует прохождение оборудованием установленных испытаний в соответствии с нормативными документами и его готовность к безопасному использованию.
Документ содержит следующие данные:
- индивидуальный номер;
- дата выдачи и период действия;
- название получающей организации;
- наименование оборудования или комплекса;
- название производителя медицинских изделий;
- ссылка на стандарт или технические требования к оборудованию;
- класс риска медицинского изделия;
- заключение об использовании.
- Для получения удостоверения Росздравнадзора необходимо получить подпись руководителя и печать организации.
Процедура получения свидетельства Росздравнадзора включает несколько этапов:
- Подача заявки в сертификационный центр "Рос-Тест" на составление регистрационного документа;
- Сбор необходимых документов, содержащих информацию о производителе медицинской продукции, технические характеристики и нормативную документацию на производимые изделия;
- Проведение проверки медицинского оборудования с целью установления его соответствия требованиям в сфере здравоохранения и соответствии стандартам и нормам регламентов;
- Принятие решения о выдаче регистрационного удостоверения.
- подача заявки на получение разрешительного документа, который будет зарегистрирован в едином государственном реестре;
УСЛОВИЯ ДЛЯ ЗАЯВИТЕЛЕЙ
Для того, чтобы получить разрешительный документ, юридические лица или частные предприниматели должны быть официально зарегистрированы в соответствии с действующим законодательством.
Для подтверждения качества изделий медицинского назначения необходимо предоставить следующие документы:
- заявку на получение удостоверения медицинского оборудования;
- документацию о продукции, ее основных свойствах и специфике;
- руководящие документы производителя, включающие устав, учредительные документы и регистрационные данные;
- протоколы и акты квалификационных испытаний, проведенных в независимой аккредитованной лаборатории.
- Документы, которые регламентируют весь жизненный цикл продукции;
- Эксплуатационные документы на товары;
- Наличие лицензий и сертификатов.
Государственная регистрация медицинских изделий
Государственная регистрация медицинских изделий — это услуга, которую предоставляют за плату. Регистрация включает две составляющие:
- Пошлина за оформление РУ, которая составляет 11 000 рублей;
- Пошлина за проведение экспертизы изделия, которая зависит от его потенциального риска и класса. Если изделие относится к первому классу риска, то стоимость экспертизы составляет 72 000 рублей. Если же это изделие второго класса (2а или 2б), то стоимость экспертизы составляет 104 000 или 136 000 рублей соответственно. Изделия третьего класса стоят 186 000 рублей.
Перед подачей заявления на государственную регистрацию необходимо произвести оплату государственной пошлины. Помимо этого, при рассмотрении экспертного заключения, уполномоченными органами государств необходимо уплатить пошлину, размер которой будет соответствовать определенному классу риска медицинского товара. Также необходимо учесть, что каждое государство признания будет требовать оплаты пошлины за рассмотрение документации по изделию.
Расширенный список преимуществ работы с центром Helmets
Организация госрегистрации медицинских товаров может быть непростой задачей, особенно с учетом новых правил. Для того чтобы успешно пройти этот процесс, необходимо изучить действующую правовую базу, провести нужные испытания и подготовить полный комплект документов, а также соблюсти очень много формальностей. Однако, есть вероятность, что в процессе работы можно совершить ошибки и потребуется начинать всю работу заново. Чтобы избежать подобной ситуации, рекомендуется обратиться в центр Helmets, где подготовленные эксперты смогут успешно провести все необходимые этапы регистрации и организовать получение РУ на медицинский товар. Вот основные преимущества работы с нами:
- Мы оказываем услуги по регистрации медицинских товаров в любом регионе России.
- Наши эксперты ведут полный цикл работы по оформлению РУ, что значительно ускоряет процесс и позволяет снизить расходы.
- Актуализация и оформление комплекта для заявления
Мы уделяем внимание каждой детали и стремимся экономить время наших клиентов, помогая им на всех этапах получения регистрационного удостоверения. За счет опыта и знаний наших экспертов мы гарантируем получение РУ в срок и без лишних затрат!
Одним из распространенных заблуждений на тему получения регистрационного удостоверения на медицинское оборудование является уверенность в том, что этот процесс прост и быстр. На самом деле, он может занять значительное количество времени и потребует от вас предоставления большого объема документации и информации.
Еще одним заблуждением является уверенность в том, что можно обойти процедуру регистрации и просто начать продажу медицинского оборудования. Незаконная продажа не зарегистрированного оборудования может повлечь за собой серьезные штрафы и юридические последствия.
Также некоторые люди считают, что можно получить регистрационное удостоверение на медицинское оборудование без необходимых клинических испытаний и сертификации. Однако без подтверждения безопасности и эффективности оборудования такая регистрация не будет возможной.
Важно помнить, что получение регистрационного удостоверения на медицинское оборудование — это сложный и ответственный процесс, который требует соблюдения всех законодательных требований и нормативов. Поэтому лучше обратиться к профессионалам в этой области и получить их помощь и поддержку.
Наша команда
Наши эксперты:
- Дарья Сергеевна — эксперт СРО
- Яна Николаевна — эксперт сертификации
- Артём Михайлович — инженер-проектировщик
- Мария Владимировна — эксперт СРО
- Юлия Владимировна — эксперт СРО
- Алина Васильевна — руководитель отдела документооборота
- Лидия Сергеевна — специалист отдела документооборота
- Алёна Андреевна — инженер-проектировщик
- Екатерина Юрьевна — эксперт сертификации
- Инна Юрьевна — руководитель отдела проектирования
Артём Викторович является руководителем нашего отдела сертификации, а Анастасия Сахибовна — наш коммерческий директор.
Наша команда объединяет эффективность, опыт и профессионализм для того, чтобы помочь Вам в решении любых вопросов, связанных с получением РУ.
Светлана Князева — руководитель отдела проектирования, тоже обладает большим опытом и знаниями в своей области.
Наталья Валерьевна — эксперт в области сертификации, а также Раиса Борисовна и Юлия Андреевна имеют аналогичные квалификации. Кроме того, Александр Иванович является экспертом СРО, а Светлана Александровна занимает должность главного бухгалтера. Роман Николаевич также является экспертом СРО, а Ульяна Анатольевна — экспертом по согласованию перепланировок.
Компания обладает аккредитациями, подтверждающими ее профессиональный уровень и качество услуг.
Однако, в 2020 году в связи с нехваткой средств защиты от вирусных инфекций, Правительством РФ было принято Постановление №299 от 18 марта 2020 года "О внесении изменений в Правила государственной регистрации медицинских изделий". Изменения затронули список медицинских изделий с низкой степенью потенциального риска их применения, в первую очередь касающихся борьбы с COVID-19.
Оформление РУ на медицинские изделия: различные варианты
Для получения РУ на медицинское оборудование в Санкт-Петербурге можно воспользоваться двумя упрощенными способами:
- Временное РУ действительно на 150 дней, при этом не требуются токсикологические, технические или клинические испытания;
- Бессрочное РУ требует предъявления базового пакета документов и образцов для проведения испытаний. Стоит отметить, что срок оформления по упрощенной схеме может достигать до 25 календарных дней, без учета времени для устранения возможных замечаний Росздравнадзора.
РУ может быть также оформлено на серийное производство и на партии медицинских изделий. Но важно помнить, что правильное оформление документов играет ключевую роль в получении РУ для медицинских изделий быстро и без ошибок.
Перед оформлением РУ необходимо подготовить нужные документы:
- сертификат;
- декларация;
Нам необходимо получить следующую документацию:
- Медицинское свидетельство регистрации;
- Другие документы.
Для оформления запроса нам необходимо предоставить следующую информацию:
- Организационно-правовую форму и полное наименование юридического лица на кириллице, а также ФИО индивидуального предпринимателя и реквизиты документа, удостоверяющего личность ИП;
- Наименование медицинского изделия (МИ) и его назначение;
- Сведения о принадлежностях, необходимых для применения МИ по назначению;
- Указание товарного знака и других средств индивидуализации МИ, если они есть на упаковке;
- Название ЮЛ (если есть) и его ИНН;
- Адрес места нахождения ЮЛ и номер телефона компании. Адрес должен соответствовать документам, подтверждающим право ЮЛ на производство и содержать название компании.
- Адрес электронной почты, предоставленный заявителем.
- Тип медицинского изделия и уровень потенциального риска в соответствии с классификацией медицинских изделий.
- Код продукции по видам экономической деятельности, согласно Общероссийскому классификатору.
- Детали об уплате государственной пошлины, включая номер и дату платежного поручения.
Изготовление и согласование документов
- Подача заявки на регистрацию медицинского изделия.
Мы поможем вам оформить необходимые документы:
Мы ответственно следим за каждым этапом обработки заявок на выдачу РУ на МИ, от начала до конца.
Мы помогаем решить спорные вопросы в процессе оформления Регистрационного Удостоверения на медицинские изделия.
Как только мы получим оригинал документа, мы начнем процесс получения вашего регистрационного удостоверения на медицинское изделие.
Мы бесплатно отправим вам оригинал документа, чтобы вы могли сверить его с копиями, которые мы вам предоставим.
Что такое Регистрационное Удостоверение на медицинские изделия
Зачем нужно получать удостоверение
Согласно Федеральному закону от 21.11.2011 No323-ФЗ, все товары для здоровья, включая прежде всего медицинские изделия, обязаны пройти государственную регистрацию.
Наличие соответствующего удостоверения на медицинское изделие подтверждает его соответствие всем стандартам и безопасность при использовании потребителями.
Регистрационный сертификат на медицинское изделие – это официальный документ, подтверждающий факт регистрации изделия в России, а Включение его данных в государственный реестр медицинской техники и изделий.
Обязательна регистрация сертификата при изготовлении или продаже следующих товаров:
Лекарственные препараты
Средства для дезинфекции
Средства индивидуальной защиты
Медицинское оборудование
Хирургические инструменты
Медицинские приборы
Согласно Федеральному закону №532 от 31.12.2014, за изготовление или продажу товаров без соответствующего сертификата предусмотрено наказание в виде лишения свободы сроком от 3 до 5 лет и штрафа от полумиллиона до двух миллионов рублей
Для того, чтобы подтвердить качество и безопасность продукции, а также иметь возможность законно ее производить и продавать в России, необходимо получить регистрационное удостоверение. Его выдачей занимается Федеральная служба по надзору в сфере здравоохранения (Росздравнадзор), которая подчиняется Министерству здравоохранения РФ. Порядок получения данного документа регулируется Постановлением Правительства РФ No1416 от 27.12.2012. Чтобы проверить наличие этого удостоверения, можно воспользоваться виртуальным ресурсом Росздравнадзора по специальному реестру. Согласно государственному стандарту 31508-2012, медицинские маски, перчатки и халаты относятся к первому классу продуктов, у которых степень риска при использовании низкая.
Срок действия полученного медицинского удостоверения не имеет ограничений.
Получение медицинского удостоверения: инструкция
Для получения медицинского удостоверения необходимо обратиться в уполномоченный орган, который имеет право выдавать регистрационное удостоверение. Этим органом может быть как индивидуальный предприниматель (но не физическое лицо), так и юридическое лицо, являющиеся изготовителями медицинских изделий.
В соответствии с постановлением Правительства РФ No1416 от 27.12.2012, изготовитель должен подать в Росздравнадзор:
- тематическое заявление
- сведения о нормативной документации, регулирующей параметры изделия
- техническую документацию на медицинское изделие от разработчика или производителя
- результаты проведенных технических испытаний изделия
- инструкцию по применению
- описание
- образец продукции
- и многие другие документы, упомянутые в постановлении
Вам нужна помощь в оформлении удостоверения?
Если у вас нет времени и желания вникать в законы, а также не хочется многократно получать отказы из-за неправильно оформленных документов при регистрации медицинского изделия, то вы всегда можете поручить эту задачу профессионалам. К тому же, каждый раз, когда вы подаете заявление, вам нужно оплачивать значительную сумму государственной пошлины. Эксперты нашего центра сертификации готовы помочь вам получить регистрационное удостоверение.
- Мы готовы предложить вам следующие услуги:
Получите помощь в получении регистрационного удостоверения в нашем центре аккредитации и лицензирования
Сэкономьте время и деньги
Возможность законного производства и продажи необходимых средств индивидуальной защиты без боязни проверок контролирующих органов — это то, что мы предлагаем. Наш опыт и компетенция позволят вам довериться нашим услугам.
Мы профессионально работаем в соответствии с договором и доверенностью!
Не стесняйтесь связываться с нами любым удобным способом и спокойно оформлять регистрационные удостоверения!
Наши заслуги
FILLERIX — Центр эстетики и косметологии
Dental Station — Стоматологическая клиника
ООО ЦАЛ
Наши услуги
ООО "Центр аккредитации и лицензирования" известно как ООО "ЦАЛ". Наш юридический адрес: 450097, респ. Башкортостан, г. Уфа, ул. Казанская, 2. Фактический адрес: 450097, респ. Башкортостан, г. Уфа, ул.
Казанская, 2. Директор: Иссенский Евгений Викторович. ИНН: 0274949680 КПП: 027801001 ОГРН: 1190280058759
Навигация по сайту
- Главная
- Лицензии
- Медицинская лицензия
- Образовательная лицензия
- Фармацевтическая лицензия
- Лицензия на дезинфекцию
Контакты
Адреса офисов компании:
- г. Москва, ул. Лобанова 8
- г. Ростов на Дону, ул. Пушкинская 65
- г. Самара, пр. Карла Маркса, 201Б
- г. Уфа, ул. Казанская, 2
- г. Санкт-Петербург, Малоохтинский пр., 64 Б
- г. Новосибирск, ул. Советская, 5
- г. Екатеринбург, ул. Розы Люксембург, 49
- г. Челябинск, ул. Кирова, 159
- г. Нижний Новгород, ул. Максима Горького, 117
- г. Красноярск, ул. Карла Маркса, 93А
- г. Казань, ул. Николая Ершова, 1А
- г. Омск, ул. Гагарина, 14, 4
- г. Пермь, ул. Куйбышева, 95б
- г. Волгоград, ул. им. Рокоссовского, 62
Этапы государственной регистрации
В Российской Федерации Росздравнадзор ответственен за проверку и выдачу регистрационных удостоверений на медицинские товары. Процедура регистрации зависит от класса потенциального риска, связанного с использованием товара.
Но, в большинстве случаев алгоритм госрегистрации выглядит следующим образом:
- Заявитель проводит обязательные тестирования товара, включая токсикологические и технические, составляет отчеты о результатах испытаний и подготавливает другие необходимые документы.
- Поданный пакет документов отправляется в Росздравнадзор на рассмотрение.
- После получения пакета документов Росздравнадзор проводит его проверку, и в случае отсутствия ошибок как в оформлении, так и в содержании, ведомство приступает к I этапу экспертизы качества, действенности и безопасности товара.
- На данном этапе уполномоченная экспертная организация проводит содержательный анализ информации, содержащейся в регистрационном пакете. После этого эксперты делают заключение о характеристиках продукта и необходимости продолжения процедуры госрегистрации, которое передается в Росздравнадзор.
- После того, как сотрудники ведомства ознакомятся с заключением экспертов и получат положительные рекомендации, они осуществляют процедуру клинических испытаний.
- Медицинская компания, имеющая аккредитацию, проводит испытания на практике и оформляет их результаты согласно стандартному протоколу. После этого протокол передается в орган Росздравнадзора.
- Представители указанного ведомства знакомятся с полученными данными и в случае, если они подтверждают эффективность и безопасность продукта для конечного пользователя, назначаются дополнительные экспертизы второго этапа.
- Определенная экспертная организация выполняет исследование документов, полученных в процессе клинических испытаний второго этапа экспертизы. После анализа все результаты оформляются в виде экспертного заключения, которое направляется в Росздравнадзор для последующей рассмотрения.
- Сотрудники компетентного ведомства тщательно исследуют последнее экспертное заключение, чтобы принять окончательное решение о возможности государственной регистрации продукта. Если исход будет положительным, они оформляют соответствующее зарегистрированное свидетельство и передают его заявителю, а также заносят информацию о регистрации во Всероссийский реестр зарегистрированных медицинских товаров, доступный на сайте ведомства. Это удостоверение не подвержено ограничениям по сроку действия.
Тем не менее, оговоркой является то, что продукты, классифицированные как категория 1 в отношении потенциального риска использования, то есть представляющие минимальную угрозу для пациентов, проходят клинические испытания еще до регистрации, то есть на стадии составления регистрационного досье. Это означает, что для них не проходит первый этап экспертизы и клинических испытаний, назначая сразу второй этап экспертизы на основе изучения соответствующей документации Росздравнадзором.
Во все моменты заявленная продолжительность процесса регистрации не должна выходить за пределы 50 рабочих дней. Тем не менее, этот срок не включает в себя временной промежуток, необходимый на проведение клинических испытаний, которые могут занять различное количество времени в зависимости от сложности и возможных рисков, связанных с использованием медицинских изделий.
Подача заявления на регистрацию в госструктуру
Поступление заявки от заявителя, который хотел бы получить разрешение на использование, становится основанием для начала процесса регистрации. Разрешенный формат составления этого документа определяется пунктом 9 Постановления № 1416. В него входят:
В заявлении необходимо указать название медицинского продукта и сопутствующих принадлежностей, без которых его использование по назначению невозможно. Если для идентификации товара используются товарный знак или другие дополнительные средства, то эта информация должна быть указана в заявлении.
В заявлении требуется указать полное и сокращенное название компании-разработчика, организационно-правовую форму компании, адрес ее местонахождения и контактные данные – телефон и электронную почту. Аналогичные сведения должны быть представлены и в случае, если заявителем выступает индивидуальный предприниматель – в этом случае следует указать фамилию, имя и отчество ИП, реквизиты документов, подтверждающих его личность.
Также необходимо указать те же данные о компании-изготовителе и об уполномоченном представителе производителя, если такой имеется.
- Требуется представление одних и тех же персональных данных заявителя, обратившегося за выдачей свидетельства о регистрации.
- Нужно указать место, где был изготовлен товар.
- Производитель должен определить назначение продукта.
- В соответствии с приказом Минздрава от 6 июня 2012 года N 4н, продукты должны быть классифицированы по конкретному типу.
- Класс потенциального риска применения продукта также определяется в соответствии с приказом № 4н.
- Товары должны быть отмечены кодом согласно общероссийскому классификатору ОК 034-2014 (КПЕС 2008).
- Необходимо указать предпочитаемый метод получения свидетельства о регистрации – бумажный или электронный.
При подаче заявления на регистрацию, соискатель обязан приложить список документов, который подтверждает соответствие предоставляемого на регистрацию продукта установленным требованиям.
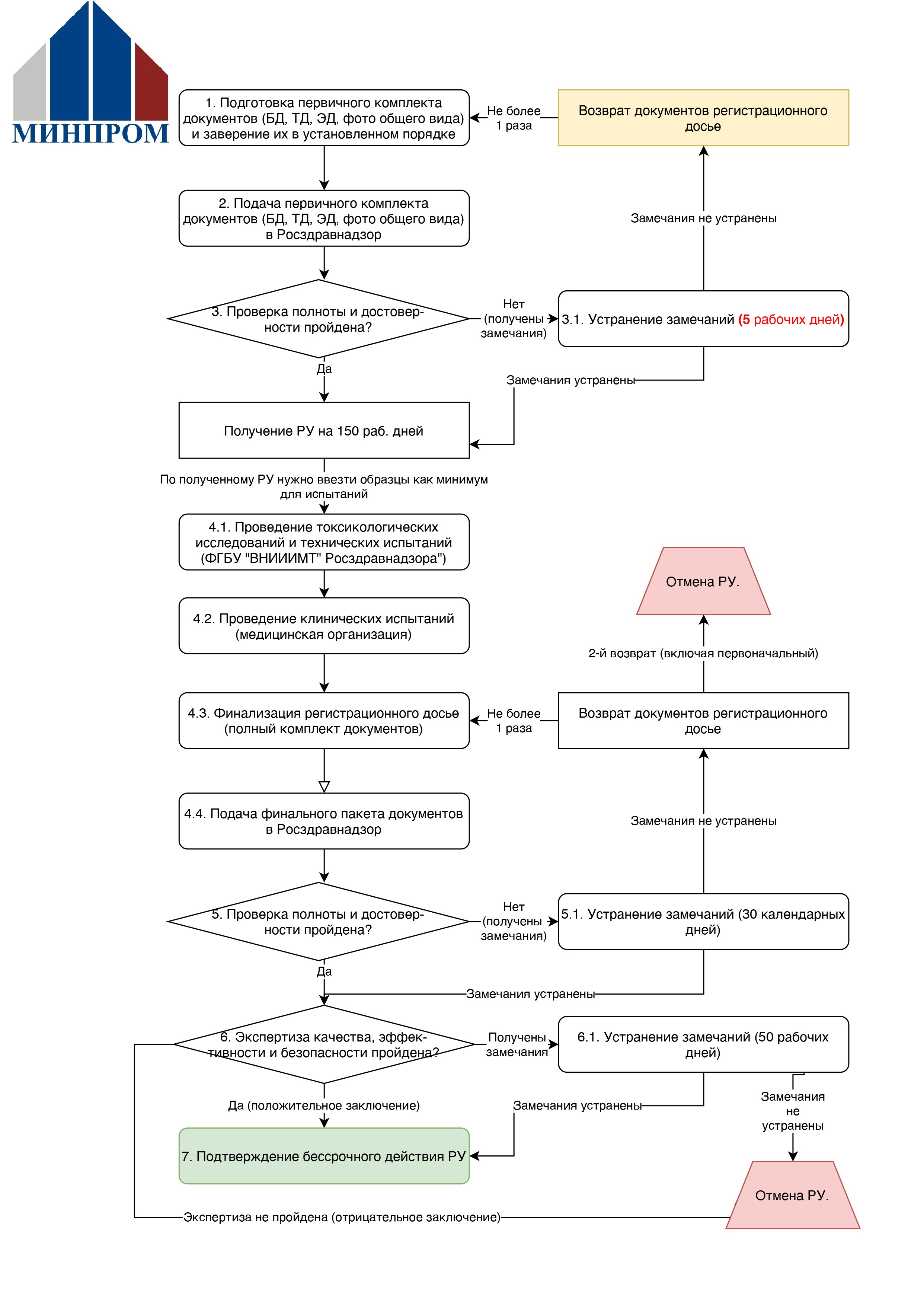
Процесс простой регистрации
Для начала необходимо подготовить комплект базовых документов юридического характера, техническую и эксплуатационную документацию, а также фотографии общего вида.
Сформированный пакет документов должен быть направлен в Росздравнадзор для дальнейшей проверки на полноту и достоверность.
Результаты проверки могут привести к вынесению уведомления об устранении нарушений, которые необходимо устранить в течение 5 рабочих дней. В противном случае РУ могут быть аннулированы.
Для того чтобы избежать аннулирования РУ, необходимо провести токсикологические, технические и клинические испытания, а также доработать техническую и эксплуатационную документацию при необходимости.
После проделанных работ необходимо подать пакет документов в Росздравнадзор и дождаться результатов проверки полноты и достоверности, которые могут привести к вынесению уведомления об устранении нарушений, которые необходимо устранить в течение 30 календарных дней, или направление в экспертное учреждение.
В процессе своей работы экспертное учреждение проводит экспертизу в соответствии со стандартной процедурой, аналогичной процедуре, выполняемой при обычной регистрации медицинских изделий 1-го класса риска. Результат экспертизы может быть положительным, с замечаниями, которые необходимо устранить в течение 50 рабочих дней, или отрицательным. В последнем случае государственная регистрация отменяется, и необходимо провести регистрацию в соответствии со стандартной процедурой.
Если же экспертиза завершается с положительным результатом, то регистрация продолжает действовать бессрочно.
Какие документы требуются для оформления регистрационного удостоверения?
Важно помнить, что для получения регистрационного удостоверения иностранного медицинского изделия необходимо предоставить копию документа, который подтверждает полномочия уполномоченного представителя производителя (доверенность). Этот документ должен быть заверен апостилем или в российском консульстве в стране, где производитель зарегистрирован (с подтверждением полномочий подписанта). Рекомендуется ознакомиться с текстом и примером доверенности для оформления регистрационного удостоверения (которая подтверждает статус уполномоченного представителя производителя).
В итоге минимальный набор документов, необходимых для оформления, состоит из:
а) копии документа, подтверждающего полномочия уполномоченного представителя производителя (в случае иностранного производителя); б) технической документации производителя (в случае российского производителя) для медицинского изделия (согласно ГОСТ Р 1.3-2018 "Технические условия на продукцию" с общими требованиями к содержанию, оформлению, обозначению и обновлению); в) эксплуатационной документации производителя для медицинского изделия, включая инструкцию по применению или руководство по эксплуатации медицинского изделия (должны соответствовать требованиям Приказа Министерства здравоохранения РФ от 19 января 2017 г. N 11н "Об утверждении требований к содержанию технической и эксплуатационной документации производителя медицинского изделия"); г) фотографических изображений медицинского изделия в общем виде вместе с принадлежностями, необходимыми для его применения (размером не менее 18 на 24 сантиметра); д) описи документов.
В дальнейшем необходимо доставить (в течение 150 дней):
а) копия документа, который подтверждает полномочия уполномоченного представителя производителя (изготовителя);
б) информация о нормативной документации на медицинское изделие;
в) документы, упомянутые в пункте 572 настоящих Правил в подпунктах "б", "в" и "г" (в случае, если были внесены изменения в них после проведения испытаний (исследований) медицинского изделия);
г) документы, которые подтверждают результаты технических испытаний медицинского изделия, выданные федеральным государственным бюджетным учреждением "Всероссийский научно-исследовательский и испытательный институт медицинской техники" Федеральной службы по надзору в сфере здравоохранения (далее — учреждение);
д) документы, которые подтверждают результаты токсикологических исследований медицинского изделия, использование которого предполагает контакт с организмом человека, выданные учреждением;
е) документы, которые подтверждают результаты испытаний медицинского изделия с целью утверждения типа средств измерения (относительно медицинских изделий, которые относятся к средствам измерения в сфере государственного регулирования обеспечения единства измерений, перечень которых утверждается Министерством здравоохранения Российской Федерации), выданные учреждением;
ж) документы, которые подтверждают результаты клинических испытаний медицинского изделия, проведенных в медицинской организации государственной системы здравоохранения, соответствующей требованиям, утвержденным Министерством здравоохранения Российской Федерации;
з) копии документов, подтверждающих качество лекарственного препарата, фармацевтической субстанции, биологического материала и другого вещества, используемых при производстве медицинского изделия или входящих в его состав и предназначенных для применения только с учетом назначения медицинского изделия, определенного производителем, и выданных в соответствии с законодательством страны происхождения лекарственного препарата, фармацевтической субстанции, биологического материала и другого вещества;
и) оригинал регистрационного удостоверения;