pH крови человека обычно находится в диапазоне от 7,35 до 7,45, что делает её слегка щелочной. Этот узкий диапазон важен для поддержания нормальных физиологических процессов и обмена веществ в организме.
Нарушение кислотно-щелочного баланса может привести к кислотозу или алкалозу, что может отрицательно сказаться на здоровье и функционировании органов. Поэтому поддержание нормального pH крови является критически важным для общего состояния организма.
- Определение pH крови: pH крови — это мера кислотности или щелочности крови, которая регулируется несколькими механизмами в организме.
- Нормальные значения: Нормальный диапазон pH крови составляет от 7.35 до 7.45, что делает кровь слегка щелочной.
- Значение pH: Изменения pH крови могут влиять на функции органов и общие метаболические процессы.
- Факторы, влияющие на pH: На уровень pH крови могут влиять дыхание, обмен веществ, а также потребление пищи и жидкости.
- Расстройства: Состояния как ацидоз (снижение pH) и алкалоз (повышение pH) могут привести к серьезным нарушениям здоровья.
- Диагностика: Чтобы определить уровень pH крови, проводят артериальный газовый анализ.
Какой уровень кислотности у крови
Кислотно-щелочное балансирование представляет собой важный фактор, который поддерживается в крови человека в определенных пределах. Это необходимо для нормального функционирования различных систем организма, проведения биохимических реакций и оптимальной работы ферментов.
Кислотами называют вещества, способные отдавать ионы водорода, в то время как основаниями (щелочами) называются вещества, принимающие указанные ионы. Уровень кислотности и щелочности растворов оценивается по шкале рН от 0 (сильные кислоты) до 14 (сильные щелочи). По шкале рН нейтральное значение равно 7.
Оптимальный уровень кислотности крови лежит в диапазоне 7,35 — 7,45 на шкале рН. Если показатель опускается ниже 7,35, это говорит о наличии ацидоза (увеличение кислотности крови). При значении рН выше 7,45 возникает алкалоз (избыток щелочных веществ в крови).
В ходе метаболических процессов в организме образуется большое количество продуктов, которые могут повлиять на данный показатель. Главная роль в регуляции кислотно-щелочного равновесия принадлежит легким, почкам и буферным системам крови.
Во время дыхания легкие выводят из организма углекислый газ, который образуется в метаболизме. Углекислый газ взаимодействует с водой, образуя углекислую кислоту. Избыток углекислого газа приводит к ацидозу, а его недостаточное количество вызывает алкалоз.
Органы выделяют избыток кислот и оснований с мочой, чтобы поддерживать уровень рН крови. Почки могут регулировать количество кислот и оснований, поглощаемых и выводимых из организма, обеспечивая баланс.
Буферные системы крови состоят из слабых кислот и оснований, которые нейтрализуют избытки кислот или оснований, помогая поддерживать стабильный уровень рН крови.
Главная причина ацидоза или алкалоза — тяжелое заболевание, при котором механизмы регуляции рН крови не справляются с изменениями.
Совпадения в русском языке
Изменения уровня кислотности и щелочности крови, дисбаланс кислотности и щелочности.
Совпадения в английском языке
Смещение pH в кислотно-щелочном балансе, гомеостаз.
Признаки и симптомы
Манифестации кислотоза и алкалоза часто замаскированы под симптомы основного заболевания, которое привело к изменению кислотно-щелочного баланса крови.
При кислотозе могут наблюдаться следующие признаки:
- нюхота, беспокойство
- ускоренное дыхание
- головная мигрень
- состояние опьянения (вплоть до бессознательности)
- падение артериального давления (при тяжелых формах кислотоза)
- сердечные аритмии.
Признаки алкалоза могут включать в себя:
- мигри в голове
- верткие повороты
- тяжесть сознания (до потери сознания)
- судороги в различных группах мышц
- нарушения сердечного ритма
Основные сведения об заболевании
Оптимальное кислотно-щелочное равновесие в организме является ключевым фактором для сохранения здоровья, его норма составляет от 7,35 до 7,45 по шкале рН.
Если рН опускается ниже 7,35, это говорит о наличии ацидоза. В случае увеличения рН выше 7,45, возникает алкалоз.
Выделяют метаболический (обменный) и респираторный (дыхательный) ацидоз и алкалоз в зависимости от причин их возникновения.
Респираторный ацидоз возникает из-за избыточного накопления углекислого газа в крови, который при сочетании с водой превращается в углекислую кислоту. Это приводит к увеличению кислотности крови. Такое состояние может возникнуть из-за нарушений в дыхании, вызывающих недостаточную легочную вентиляцию.
В таких случаях организм начинает производить энергию не из глюкозы, а из жиров — альтернативный путь для получения энергии. Расщепление жиров в печени приводит к образованию большого количества кетоновых кислот, что вызывает развитие ацидоза.
- Нарушение работы почек. Почки играют важную роль в регуляции кислотно-щелочного баланса в крови. При заболеваниях почек, приводящих к нарушению их функций, могут быть нарушены процессы выведения кислот и поглощения веществ с щелочной реакцией, что становится причиной ацидоза.
- Избыточная потеря щелочей из организма вместе с желудочными соками. Такое состояние возможно при сильной диарее или после хирургического вмешательства в области кишечника.
- Отравление ядовитыми веществами и токсинами. Процессы разложения этих веществ в организме могут привести к образованию избытка кислот, что способно вызвать ацидоз.
Главными причинами метаболического алкалоза являются:
- Потеря большого количества кислотного содержимого желудка. Это может произойти при сильной рвоте или аспирации содержимого желудка через специальный зонд.
- Применение диуретиков.
- Повышенное выделение ионов водорода почками может возникнуть при избытке гормона альдостерона, который регулирует водно-электролитный баланс в организме. Уровень альдостерона может повышаться при заболеваниях надпочечников или патологии других органов, таких как сердце.
Таким образом, развитие ацидоза или алкалоза часто связано с патологическими процессами, при которых изменения кислотно-щелочного баланса превышают компенсационные возможности организма. Важным этапом лечения является нормализация состояния пациента, основное заболевание, вызвавшее отклонения в рН крови.
Кто может находиться в группе риска?
Группе риска нарушений кислотно-щелочного баланса крови могут принадлежать:
- Лица, которые страдают заболеваниями органов дыхания (как, например, бронхиальная астма)
- Лица, у которых есть заболевания почек с нарушением их функций
- Лица, страдающие от сахарного диабета
- Лица, у которых есть поражения нервной системы (как, например, травмы головного мозга, инсульты)
- Лица, пережившие значительные потери содержимого желудочно-кишечного тракта (как, например, при обильной рвоте, частом жидком стуле)
- Лица, принимающие определенные лекарства (как, например, мочегонные, аспирин)
- Лица, злоупотребляющие алкоголем.
Диагностика
Важную роль в проведении диагностики играют лабораторные методы исследования, которые позволяют установить уровень рН крови, ее газовый состав, параметры водно-электролитного обмена и другие жизненно важные показатели, контроль и коррекция которых являются неотъемлемыми при таких состояниях.
- Измерение уровня кислотности крови и газового состава. Эти параметры обычно определяются специальными приборами, такими как газоанализаторы. Анализ проводится на артериальной крови.
- Анализ состава крови. Этот метод позволяет определить основные компоненты крови: количество эритроцитов, гемоглобина, лейкоцитов и тромбоцитов. Хотя этот анализ не дает точную информацию о наличии ацидоза или алкалоза, он помогает выявить причины изменений в кислотно-щелочном балансе крови.
- Анализ мочи с микроскопией. Этот метод позволяет оценить основные физико-химические свойства мочи, рН и выявить наличие патологических или физиологических продуктов обмена веществ.
- Уровень глюкозы в крови. Глюкоза — главный источник энергии для человеческого организма. Увеличение содержания глюкозы в крови наблюдается при наличии сахарного диабета. Нарушения обмена веществ, связанные с этим заболеванием, могут привести к развитию ацидоза.
- Калий, натрий, хлор в сыворотке. Калий, натрий и хлор являются основными электролитами в организме человека, выполняющими целый ряд функций, включая транспортировку веществ через клеточные мембраны и поддержание водно-электролитного баланса.
- Аланинаминотрансфераза (АЛТ). АЛТ — фермент, присутствующий во многих клетках организма, особенно в печени. При поражении печени уровень этого фермента в крови возрастает. Нарушение работы печени может привести к нарушениям кислотно-щелочного равновесия в крови.
- Креатинин и мочевина — это конечные продукты обмена белков в организме человека, которые выходят из организма через почки. Если функция почек нарушена, уровень этих показателей может повыситься, что может привести к изменениям в кислотно-щелочном балансе.
В зависимости от клинической ситуации могут потребоваться другие лабораторные анализы для определения причин ацидоза или алкалоза, такие как уровень кетоновых тел в крови и моче, концентрация молочной кислоты в крови и другие.
- Рентгенография позволяет выявить патологические изменения в легких, такие как воспаление, которое может привести к изменениям в дыхании.
- УЗИ исследование является методом, основанным на использовании ультразвука, который позволяет визуализировать внутренние органы, выявлять изменения в их структуре и наличие опухолей или кист, что может быть важным для определения причин нарушений кислотно-щелочного баланса в крови.
- Компьютерная томография (КТ) предоставляет информативные изображения внутренних органов, что помогает выявить заболевания, ставшие причиной ацидоза или алкалоза, например, нарушения дыхания или кровоизлияния в мозг.
Лечение
Для лечения нарушений кислотно-щелочного баланса в организме необходимо сосредоточиться на лечении основного заболевания, которое стало причиной ацидоза или алкалоза. Для нормализации уровня pH могут быть использованы внутривенные инъекции растворов, нейтрализующих кислоты (при ацидозе) или щелочи (при алкалозе).
Лечение респираторного ацидоза направлено на восстановление нормальной частоты и глубины дыхания, при необходимости пациент может быть подключен к аппарату искусственной вентиляции легких.
При респираторном алкалозе можно применить ингаляции смесей воздуха с углекислым газом.
Меры профилактики
Не существует специфической профилактики изменений кислотно-щелочного баланса в крови. Пациентам с заболеваниями, способными нарушить рН крови (например, сахарным диабетом), следует строго следовать рекомендациям лечащего врача, регулярно проходить обследования и лечение.
Рекомендуемые анализы
- Определение рН крови
- Определение газового состава крови
- Общий анализ крови
- Общий анализ мочи с микроскопией
- Глюкоза в плазме крови
- Калий, натрий, хлор в сыворотке
- Аланинаминотрансфераза (АЛТ)
- Креатинин в сыворотке
- Мочевина в сыворотке
Какой ph у крови
1 ГБОУ ВПО «Саратовский государственный медицинский университет им. В.И. Разумовского» Минздрава России

967 КБ
1. Ю.Я. Агапов. Сбалансированность кислот и щелочей. – Москва, 1968. – 184 страницы.
2. В.А. Войнов. Атлас патофизиологии. – Москва, 2004. – 218 страниц.
3. Г.П. Гусев. Роль почек в регуляции кислотно-щелочного баланса // Почечная физиология: Руководство. – Ленинград, 1972. – Стр. 142–168.
4. В.Ф. Жалко-Титаренко. Водно-электролитный обмен и кислотно-основной статус в здоровье и болезни. – Киев, 1989.
5. С.С. Костюченко. Кислотно-щелочной баланс в интенсивной терапии. – Минск, 2009. – 268 страниц.
6. Н.И. Лосев, В.А. Войнов. Физико-химический гомеостаз организма // Гомеостаз / Под ред. П.Д.
Горизонтова. – Москва, 1981. – Стр. 186–240.
7. В.Д. Малышев. Кислотно-основной статус и водно-электролитный баланс в интенсивной терапии: Учебное пособие. – Москва: ОАО «Издательство «Медицина», 2005. – 228 страниц.
8. Книга Рут Г. "Кислотно-щелочное состояние и электролитный баланс" была опубликована в Москве в 1978 году и содержит 118 страниц.
9. Статья Г. Тавса "Газы крови и кислотно-щелочное равновесие" входит в книгу "Физиология человека", под редакцией Р. Шмидта и Г. Тавса. Она была опубликована в Москве в 1986 году и занимает страницы с 241 по 268.
10. У. Хейтц и М. Горн написали краткое руководство "Водно-электролитный и кислотно-основный баланс", которое издано в Москве издательством "БИНОМ. Лаборатория знаний" в 2009 году. Книга содержит 359 страниц.
11. В работе К. Хруски "Патофизиология кислотно-основного обмена", включенной в сборник "Почки и гомеостаз в норме и патологии", изданном в Москве в 1987 году, описывается аспекты кислотно-основного обмена на страницах с 170 по 216.
Состояние кислотно-щелочного баланса (рН) в организме является одним из ключевых и наиболее строго регулируемых параметров гомеостаза. Ферменты, гормоны, процессы окислительно-восстановительного обмена, обмен веществ, функции органов и систем, стабильность водно-электролитного баланса, проницаемость биологических мембран и другие процессы зависят от соотношения водородных и гидроксильных ионов внутренней среды организма. Активность кислотно-щелочной реакции влияет на способность гемоглобина переносить и доставлять кислород к тканям.
Уровень активности среды обычно оценивается по концентрации ионов водорода в жидкостях.
Уровень кислотности (рН) является одним из самых строгих параметров крови, который в организме человека остается в узких пределах — в артериальной крови рН составляет от 7,35 до 7,45; в венозной — от 7,32 до 7,42. Значительные изменения рН крови свидетельствуют о нарушениях обмена в организме. В других жидкостях и клетках рН может быть отличным от крови.
Отклонения рН крови за указанные границы могут привести к серьезным изменениям в окислительно-восстановительных процессах, активности ферментов, проницаемости клеточных мембран, что приводит к сбоям в работе сердечно-сосудистой, дыхательной и других систем организма; сдвиг на 0,3 может вызвать коматозные состояния, а на 0,4 — часто становится непригодным к жизни.
Механизмы гомеостаза поддерживают кислотно-щелочное равновесие в организме. Они опираются на особенности физико-химических свойств крови и участие дыхательной, почечной, печеночной, желудочно-кишечной систем.
Химические буферные системы первыми реагируют на изменения pH организма, чтобы предотвращать их быстро.
Буферные системы – это смеси, которые не позволяют изменить pH в среде при добавлении кислот или оснований. Они лишь временно удерживают H+, чтобы восстановить КОС. Эти смеси состоят из слабой кислоты и ее соли с сильным основанием, или из слабого основания и соли с сильной кислотой.
Самыми эффективными системами буферизации крови считаются бикарбонатный, фосфатный, белковый и гемоглобиновый. Первые три активно работают в плазме крови, в то время как гемоглобиновый буфер, наиболее мощный из них, функционирует внутри эритроцитов.

Бикарбонатный буфер — одна из самых важных систем внеклеточного буферования, состоящая из слабой угольной кислоты Н2СО3 и её соли — сильного основания. Угольная кислота образуется в результате взаимодействия углекислого газа и воды: CO2 + H2O ↔ H2CO3. Далее угольная кислота диссоциирует на водород и бикарбонат: H2CO3 ↔ H+ + HCO3-.
При нормальных условиях (pH крови около 7,4) содержание бикарбоната в плазме превышает содержание углекислоты в 20 раз.
Бикарбонатная система составляет 53% всей буферной емкости крови, причем на бикарбонат плазмы приходится 35%, а на бикарбонат эритроцитов — 18% буферной емкости.

Когда в плазме появляются излишки кислорода, ионы водорода взаимодействуют с анионами бикарбоната (). Образующийся избыток углекислоты в плазме попадает в эритроциты, где при помощи угольной ангидразы расщепляется на углекислый газ и воду. Углекислый газ выделяется в плазму, стимулирует дыхательный центр, и излишек СО2 удаляется из организма через легкие. Это быстрое превращение любой кислоты в угольную бикарбонатом, который легко удаляется из организма через легкие, делает бикарбонатный буфер самым неустойчивым буфером.

Бикарбонатный буфер способен нейтрализовать избыток оснований, приводя к образованию менее сильного основания — бикарбонатных солей, которые выделяются почками.
Уровень рН крови остается в пределах нормы благодаря поддержанию пропорционального соотношения между угольной кислотой и бикарбонатом натрия в соотношении 1:20.
Фосфатный буфер состоит из солей однозамещенных и двухзамещенных фосфатов, обеспечивая 5% буферной емкости крови и являясь основной буферной системой клеток.
Кислотное свойство одноосновной соли проявляется при её диссоциации, образуя ион  , который в свою очередь способен принять ион водорода: NаН2РО4 ⇒ Nа+ +
, который в свою очередь способен принять ион водорода: NаН2РО4 ⇒ Nа+ +  ; ⇒Н+ + . Двухосновный фосфат, напротив, проявляет свои основные свойства при диссоциации, образуя ион , который способен связать ион водорода: + Н+ ⇒ .
; ⇒Н+ + . Двухосновный фосфат, напротив, проявляет свои основные свойства при диссоциации, образуя ион , который способен связать ион водорода: + Н+ ⇒ .
При нормальном пН в плазме соотношение фосфатных солей NаН2РО4: Nа2НРО4 = 1:4. Этот буфер играет важную роль в регуляции кислотно-основного состояния почек, а также участвует в регуляции реакций в некоторых тканях. В крови его функция в основном сводится к поддержанию постоянства и воспроизводства бикарбонатного буфера.
Система белковых буферов является мощным инструментом, способным регулировать кислотно-щелочной баланс за счёт амфотерных свойств белков. Эта система буферов обеспечивает около 7% всей буферной способности крови. Белки плазмы содержат как кислотные, так и щелочные остатки, что позволяет им эффективно реагировать в различных средах, где происходит диссоциация белков.
Гемоглобиновая буферная система является самой вместимой. Она обладает до 75% всей буферной способности крови. Главным свойством данной буферной системы является способность гемоглобина постоянно находиться в двух формах: восстановленной (редуцированной) форме Hb и окисленной (оксигемоглобин) форме HbO2.
Когда речь идет о гемоглобиновом буфере, он способен нейтрализовать как летучие, так и нелетучие кислоты, в отличие от бикарбонатного буфера. Окисленный гемоглобин действует как кислота, повышая концентрацию ионов водорода, тогда как восстановленный (дезоксигенированный) гемоглобин действует как основание, борясь с избытком H+.
Гемоглобин является примером идеального белкового буфера, его эффективность невероятно высока. Гемоглобин на шесть раз эффективнее в качестве буфера, по сравнению с плазменными белками.
Превращение окисленной формы гемоглобина в восстановленную предотвращает смещение рН в сторону кислотности при контакте крови с тканями, а появление оксигемоглобина в легочных капиллярах помогает избежать смещения рН в сторону щелочности за счет вывода из эритроцитов CO2 и ионов хлора и появления в них бикарбоната.
Система аммиак/ион аммония (NH3/NH4+) – в основном активна в моче.
Помимо использования буферных систем для поддержания стабильного уровня рН, активное участие в этом процессе принимают физиологические системы. Основными из них являются легкие, почки, печень и желудочно-кишечный тракт.
Роль дыхательной системы в регуляции кислотно-щелочного баланса организма является значительной, хотя для компенсации сдвигов в рН крови требуется от 1 до 3 минут. Легкие отвечают за поддержание оптимального уровня углекислоты, причем ключевым показателем их работы является парциальное давление углекислого газа в крови. Легочные механизмы обеспечивают временную компенсацию, вызывая сдвиг диссоциации оксигемоглобина влево и уменьшая кислородный потенциал артериальной крови.
Когда функция газообмена в легких стабильна, они выводят около 850 граммов углекислого газа в сутки. При увеличении уровня углекислого газа в крови на 10 мм рт. ст., происходит увеличение вентиляции в 4 раза.
Почки играют не менее важную роль в регуляции активной реакции крови, чем дыхательная система. Почечный механизм компенсации работает медленнее, чем респираторный. Полноценная почечная компенсация проявляется только через несколько дней после изменения уровня pH.
Выделение кислот при потреблении обычной смешанной еды у человека с нормальным здоровьем превосходит выделение оснований, что делает мочу кислой (рН 5,3–6,5) и делает концентрацию ионов водорода в ней примерно в 800 раз больше, чем в крови. Почки вырабатывают и выводят в мочу количество ионов водорода, соответствующее количеству, непрерывно поступающему в плазму из клеток организма, заменяя при этом ионы водорода, выделяемые эпителием канальцев, на ионы натрия первичной мочи. Этот процесс реализуется за счет нескольких химических реакций.
Один из них — это процесс реабсорбции натрия при превращении двохзамещенных фосфатов в однозамещенные. Когда фосфатный буфер исчерпывается (при рН мочи ниже 4,5), реабсорбция натрия и бикарбоната происходит за счет аммониогенеза.
Еще одним процессом, который задерживает натрий в организме и выводит избыток ионов водорода, является превращение бикарбонатов в угольную кислоту в канальцах почек.
Четвертым процессом, который помогает сохранить натрий в организме, является образование аммиака в дистальных почечных канальцах (аммониогенез) и его использование для нейтрализации и вывода кислотных эквивалентов с мочой.
Образовавшийся свободный аммиак легко проникает в канальцы, где он объединяется с ионами водорода, превращаясь в аммонийный катион, который не способен вернуться обратно в клетку стенки канальца.
В итоге концентрация ионов водорода в моче может значительно превышать их концентрацию в крови.
Это свидетельствует о высокой способности почек удалять ионы водорода из организма.
Механизмы почечной регуляции кислотно-основного баланса не способны быстро скорректировать уровень рН, в отличие от дыхательного механизма, но они работают в течение нескольких дней, пока рН не восстановится до нормы.
Регуляция обмена веществ в организме при участии печени. Печень окисляет недоокисленные вещества из крови, поступающей из кишечника, и превращает их в конечные продукты; также синтезирует мочевину из азотистых соединений, таких как аммиак и хлорид аммония, которые поступают в кровь через портальную вену из пищеварительного тракта; печень играет важную роль в выведении избыточных кислотных и щелочных продуктов метаболизма через желчь в кишечный тракт. При избытке кислот в печени увеличивается их нейтрализация, что приводит к уменьшению синтеза мочевины. Неиспользованный аммиак нейтрализуется кислотами и выводится из организма в виде аммонийных солей с мочой. При увеличении количества щелочных веществ в печени увеличивается выработка мочи, а снижается процесс образования аммиака, что сопровождается уменьшением вывода аммонийных солей с мочой.
Уровень водородных ионов в крови также зависит от работы желудка и кишечника. Слизистые клетки желудка вырабатывают соляную кислоту в очень высокой концентрации. При этом ионы хлора переходят из крови в желудок в соединении с ионами водорода, образующимися в эпителии желудка с помощью карбонангидразы. Вместо хлоридов в плазму поступает бикарбонат в процессе желудочной секреции.
Поджелудочная железа активно регулирует кислотно-щелочной баланс крови, производя большое количество бикарбоната. Образование бикарбоната замедляется при избытке кислот и усиливается при их недостатке.
В условиях избытка нелетучих кислот и оснований кожа может выделять основания с помощью пота. Это особенно важно при нарушении работы почек.
Костная ткань – это самая медленно реагирующая система в организме. Ее участие в регуляции кислотно-основного баланса крови заключается в способности обмениваться ионами Са2+ и Na+ на протоны Н+ с плазмой крови. Происходит растворение кальциевых солей костного матрикса, высвобождение ионов Са2+ и связывание ионов HPO42– с Н+ для образования дигидрофосфата, который выводится с мочой. И, параллельно, при снижении уровня pH (активации) происходит поступление ионов H+ внутрь остеоцитов и вывод ионов калия наружу.
Диагностика кислотно-щелочного баланса в организме
При изучении уровня кислотности и щелочности важнейшее значение имеет анализ крови. Показатели в капиллярной крови практически идентичны показателям артериальной крови. В настоящее время для определения уровня кислотности использовуется эквилибрационный микрометод Аструпа. Этот метод помимо истинного уровня pH крови позволяет также определить уровень углекислого газа в плазме (рСО2), уровень бикарбоната в крови (АВ), стандартный уровень бикарбоната (SB), общую сумму оснований в крови (ВВ) и уровень недостатка или избытка оснований (ВЕ).
Определение кислотно-щелочного баланса: Почему важно проводить исследования кислотно-щелочного баланса в рамках обычного биохимического анализа крови?
Статья, опубликованная специалистами клиники в американском онлайн-журнале "Прогрессивные исследования в органической и неорганической химии (AROIC)" от издательства Corpus Publishers, посвящена необходимости включения значений уровня pH крови в стандартный биохимический анализ.

Как эксперт в области медицины и биохимии, я могу с уверенностью сказать, что pH крови является критически важным показателем для общего состояния здоровья организма. Нормальный уровень pH человеческой крови варьируется в диапазоне от 7,35 до 7,45. Это значение указывает на слабо щелочную природу крови и является результатом сложного химического равновесия между кислородом, углекислым газом и другими растворёнными веществами.
Если уровень pH крови падает ниже 7,35, мы говорим о состоянии, известном как ацидоз. Это может произойти из-за различных факторов, таких как накопление углекислого газа в результате заболеваний дыхательной системы или накопление кислот в результате метаболических нарушений. Ацидоз может привести к серьёзным осложнениям, включая нарушение функций сердца и нервной системы.
С другой стороны, если pH крови превышает 7,45, это состояние называется алкалозом. Алкалоз может возникнуть в результате гипервентиляции, которая приводит к снижению уровня углекислого газа или же из-за избытка щелочных веществ в организме. Как и в случае с ацидозом, алкалоз также может вызвать негативные последствия для здоровья.
Регуляция pH крови осуществляется с помощью различных систем в организме, включая легочную, почечную и буферные системы. В легких происходит обмен газов, который помогает удалить лишний углекислый газ, тогда как почки управляют уровнем кислот и оснований через выведение или задержку определённых ионов.
Поэтому поддержание нормального уровня pH крови критично для поддержания гомеостаза. Даже незначительные отклонения от нормы могут вызвать серьёзные проблемы, поэтому мониторинг pH является важной частью медицинских обследований и диагностики. Следует учитывать, что здоровье организма является результатом взаимодействия множества факторов, и pH крови — лишь один из этих показателей.
Значения pH крови для своевременной диагностики ХНИЗ
Нормальный pH уровень крови составляет от 7,35 до 7,45, а любые изменения за пределами этого диапазона указывают на серьезные проблемы в организме. Авторы статьи отмечают важность оценки кислотно-щелочного баланса при проведении стандартных биохимических анализов крови.
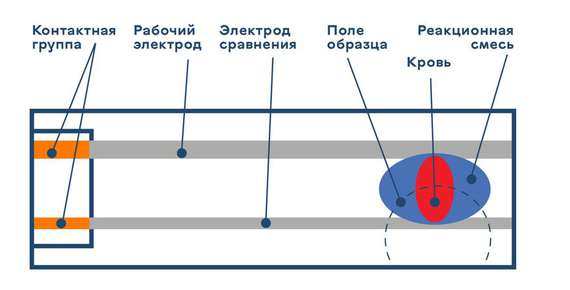
Результаты таких исследований помогут терапевтам и специалистам первой помощи выявить отклонения в обмене веществ у пациентов, выявить, например, метаболический ацидоз, который характерен для хронических и острых заболеваний. Авторы предлагают рассмотреть возможность создания тест-полосок для оценки pH крови на основе электрохимических принципов, аналогичных принципам глюкометров.
Разбирается сложность измерения pH крови в современных условиях. Для достоверных данных требуется изучение в специализированных лабораториях и расшифровка проводится профильными специалистами. Обсуждается значимость анализа pH крови для точной и быстрой диагностики заболеваний. Предлагается метод, способствующий получению верного и своевременного лечения пациентами в медицине и ветеринарии.
Журнал Advance Research in Organic and Inorganic Chemistry (AROIC) — это электронное издание, созданное издательством Corpus Publishers, с целью обмена научными исследованиями в области органической и неорганической химии между химиками-медиками, биохимиками, фармакологами и фармацевтическими технологами. Журнал публикует научные работы, которые помогают понять связь между молекулярной структурой и биологической активностью.
Информация о журнале / издании:
Издательство Corpus Publishers
Международное издательство академических журналов с открытым доступом, способствующее распространению научных знаний и проведению оригинальных исследований в различных областях науки. Платформа, объединяющая студентов, преподавателей, авторов научных работ и ученых-исследователей, где они могут обмениваться инновационными идеями. Издательство Corpus предлагает широкий спектр услуг для исследователей и обеспечивает быструю публикацию в удобном формате. На данный момент издательство Corpus Publishers выпускает 35 научных журналов.
Опубликована книга от издательства BP International. Одну из глав подготовили специалисты клиники доктора Шишонина. Исследование показало, что восстановление артериального кровотока к ромбовидной ямке шейных позвонков приводит к нормализации уровня HbA1c у пациентов с предиабетом.
Доказано, что для предотвращения и лечения артериальной гипертензии требуется комплексный подход, включающий аэробные упражнения, способствующие снижению артериального давления.
Исследован вопрос восстановления пациентов после травм верхних конечностей с применением изолированной лечебной гимнастики.
Часто задаваемые вопросы
Что показывает уровень pH в крови?
Уровень pH крови является показателем, отображающим соотношение кислот (способных выделять ионы водорода) и оснований (способных принимать эти ионы) в крови.
Как определить нарушение кислотно-щелочного баланса?
Тошнота, рвота, учащенное дыхание, головная боль, нарушение сознания (вплоть до комы), снижение артериального давления (в случае тяжелых форм ацидоза), нарушения сердечного ритма.
Как влияет уровень pH на организм?
РН организма человека регулируется таким образом, чтобы усвоение полезных веществ происходило в соответствии с нормой. Если кислотно-щелочной баланс нарушен, минералы и другие питательные вещества могут не усваиваться, что может привести к проблемам со здоровьем, разрушению клеток и, в конечном итоге, к болезням или даже к смерти.
Как определить кислотность в организме?
Для того чтобы понять, насколько организм окислен, нужно проверить рН мочи и слюны. Это позволит оценить, сколько лишних кислот присутствует в организме в данный момент. Для этого можно использовать индикаторную бумагу и тест-полоски или прибор для измерения кислотности — рН-метр.
Полезные рекомендации
Рекомендация №1
Если вы подозреваете нарушение кислотно-щелочного баланса в организме, обратитесь к врачу для назначения анализа на уровень PH в крови. Этот показатель может указать на наличие различных заболеваний.
РЕКОМЕНДАЦИЯ №2
Не забывайте, что уровень PH в крови может изменяться при заболеваниях легких, почек, сердца, печени, а также при нарушениях обмена веществ. Систематический контроль этого показателя поможет выявить проблемы вовремя.
