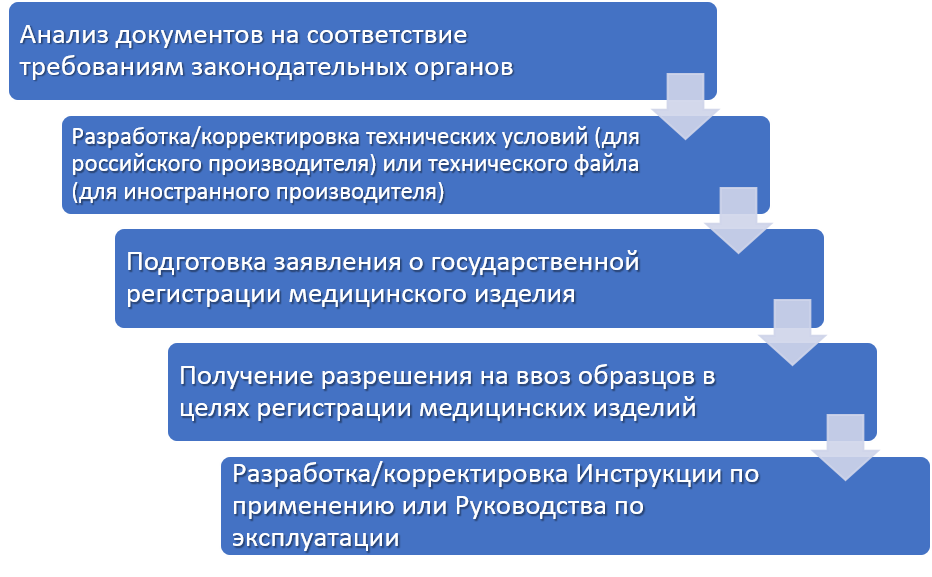
Для регистрации медицинской техники необходимо предоставить определенный пакет документов, включающий в себя сертификат соответствия, техническое описание устройства, инструкцию по эксплуатации, декларацию о соответствии требованиям безопасности и другие необходимые документы.
В следующих разделах статьи мы поговорим о процедуре регистрации медицинской техники, основных требованиях к документам, которые необходимо предоставить, а также о роли уполномоченного органа в этом процессе. Также мы рассмотрим возможные сложности и трудности, с которыми могут столкнуться производители и поставщики медицинской техники при регистрации.
- Свидетельство о регистрации организации
- Свидетельство о присвоении идентификационного номера медицинского изделия
- Сертификат соответствия медицинской техники
- Паспорт медицинского изделия
- Технический паспорт на медицинское оборудование
- Копия документа о заключении договора на обслуживание медицинской техники
Процедура регистрации медицинских изделий в РФ
Регистрационное свидетельство на продукцию медицинского назначения – это документ, выдаваемый Росздравнадзором, который подтверждает соответствие данного изделия установленным требованиям и стандартам качества, безопасности и эффективности.
Получение официального документа является необходимым условием для производства и реализации медицинских изделий на территории РФ.
Оформление Регистрационного Удостоверения (РУ) может занять некоторое время и потребовать дополнительных затрат на проведение технических испытаний, испытаний на электромагнитную совместимость (при необходимости), токсикологических исследований и клинических испытаний, переводы иностранных документов (в случае если медицинское изделие иностранного производства), оплату государственных пошлин. Однако наличие РУ позволяет производителю медицинского изделия законно продавать свою продукцию на территории России и получать государственную поддержку в виде налоговых льгот и других преференций.
Получение РУ — это обязательный этап для производства и продажи медицинских изделий на территории РФ, и его отсутствие может привести к серьезным последствиям, включая штрафы и ограничения на деятельность.
Мы предлагаем
| Регистрация медицинских изделий в соответствии с национальными правилами по Постановлению Правительства №1416 | от 300 000 руб. |
| Упрощенная регистрация медицинских изделий в соответствии с Постановлением Правительства №299 | от 300 000 руб. |
| Ускоренная регистрация медицинских изделий в соответствии с Постановлением Правительства №552 | от 320 000 руб. |
| Упрощенная регистрация серии (партии) медицинских изделий по Постановлению Правительства №430 | от 300 000 руб. |
| Регистрация медицинских изделий в соответствии с Правилами №46 по Евразийскому экономическому союзу | от 500 000 руб. |
| Внесение изменений в Регистрационное Удостоверение | от 25 000 руб. |
| Внесение изменений в регистрационное досье | от 80 000 руб. |
| Разработка регистрационного досье | от 100 000 руб. |
| Разработка технических условий/анализа риска и других отдельных документов | от 5 000 руб. |
| Помощь специалиста на отдельном этапе регистрации | по расчету |
Мы готовы предоставить вам необходимые документы для первоначального анализа, подобрать специалиста, который соответствует требованиям вашего медицинского изделия и создать стратегию регистрации. Вам понадобятся следующие документы: технические условия (ТУ) или технический файл, эксплуатационную документацию — инструкцию по применению и руководство по эксплуатации, файл менеджмента риска на медицинское изделие, сведения о нормативной документации (СНД), валидацию программного обеспечения (ПО) — акт, программа и протокол, файл проектирования с учетом эксплуатационной пригодности, валидацию процесса упаковки, валидацию процесса стерилизации и таблицу сравнения с аналогами в рамках клинических испытаний.
В соответствии с Федеральным законом № 323 «Об основах охраны здоровья граждан в Российской Федерации» статья 38, медицинские изделия представляют из себя различные инструменты, аппараты, приборы и материалы, применяемые отдельно или в сочетании между собой для достижения медицинских целей, а В сочетании с другими принадлежностями, необходимыми для их использования по назначению. К таким принадлежностям относится специальное программное обеспечение. Производители медицинских изделий могут предназначать их для:
- профилактики, диагностики, лечения и медицинской реабилитации заболеваний;
- мониторинга состояния организма человека;
- проведения медицинских исследований;
- восстановления, замещения, изменения анатомической структуры или физиологических функций организма;
- предотвращения или прерывания беременности;
- Медицинские изделия, которые выполняют свою функцию не за счет фармакологического, генетического или метаболического воздействия на организм человека, а за счет других способов, могут быть признаны взаимозаменяемыми в случае сравнимости их функционального назначения, технических и качественных характеристик, а Возможности замены одного изделия другим.
Если изделие относится к медицинским, следует определить его класс риска, зависящий от возможных побочных эффектов и осложнений при использовании: класс 1, 2а, 2б, 3 и для диагностики in vitro.
После определения класса риска и выбора изделия, производится расчет стоимости услуги в соответствии с таблицей цен.
| Вид услуги | Стоимость, руб. |
| Процедура "Ин витро" | От 1 500 000 |
| Вирусологические исследования без оценки | От 200 000 |
| Вирусологические исследования с оценкой | От 650 000 |
| Разрешение на медицинское изделие 1-го класса риска | От 900 000 |
| Разрешение на медицинское изделие 2а класса риска | От 1 200 000 |
| Разрешение на медицинское изделие 2б класса риска | От 1 500 000 |
| Разрешение на медицинское изделие 3-го класса риска | От 1 800 000 |
Предполагаемая стоимость услуг при регистрации медицинских изделий
При регистрации медицинской техники необходимо предоставить определенный набор документов, чтобы обеспечить соответствие оборудования требованиям законодательства и стандартам безопасности.
Важным документом для регистрации является сертификат соответствия, подтверждающий качество и безопасность медицинского оборудования. Также требуется технический паспорт, в котором содержится информация о характеристиках и функциях устройства.
Для регистрации необходимо также предоставить документацию, подтверждающую происхождение и право собственности на медицинскую технику. Это может быть акт приема-передачи, договор купли-продажи или иной документ, удостоверяющий права собственности.
Не стоит забывать о регистрационных документах, таких как заявление на регистрацию, выписка из реестра предприятий-изготовителей медицинской техники и прочие формальности, необходимые для законного использования оборудования.
Порядок проверки заявлений на регистрацию медицинских изделий
Когда заявитель предоставляет комплект документов, соответствующих требованиям закона, Росздравнадзор проводит их экспертизу, чтобы проверить полноту набора документов и правильность их заполнения. Ведомство обязано выполнить эту проверку в течение пяти рабочих дней. Если будут обнаружены несоответствия между предъявленными документами и установленным списком, Росздравнадзор сообщит об этом заявителю.
В соответствии с административным регламентом регистрации медицинских товаров, определяющим порядок выполнения этой процедуры, заявителю будет предоставлено 30 дней на сбор недостающих документов и представление их в уполномоченный орган, если будут обнаружены несоответствия. Такие и другие правила регистрации медицинских изделий определены в приказе Росздравнадзора от 6 мая 2019 года №3371.
Этап I экспертизы госрегистрации: главная часть процедуры
После получения полного пакета документации, предусмотренной постановлением № 1416 и смежными нормативными документами, специалисты контролирующего ведомства оценивают ее на соответствие действующим требованиям и принимают решение о начале процедуры госрегистрации. Однако, если в ходе проверки выявилось несоответствие продукта нормам, то ему может быть отказано в регистрации на данном этапе. Также Росздравнадзор может прийти к такому же выводу на любом этапе регистрации.
Если решено начать процедуру регистрации, то государственное учреждение выдает задание экспертной организации, которая проведет проверку предоставленных заявителем документов. Эта проверка будет выполнена с особой тщательностью, чтобы проверить параметры медицинского изделия. После такой проверки будет составлено подробное заключение, которое будет отправлено на рассмотрение в контролирующее ведомство.
Исследования в клинике
Организация, ответственная за госрегистрацию, не имеет решающего голоса в процессе – это право принадлежит экспертам Росздравнадзора, которые анализируют заключение специалистов. Положительный результат оценки продукта относительно его безопасности и эффективности может быть причиной назначения клинических испытаний для продвижения этапов. Такие испытания разрешены только для узкого круга медицинских организаций, которые находятся в закрытом списке Росздравнадзора. Это объясняется тем, что участие людей в их проведении требует особой осторожности и максимального обеспечения их безопасности.
Главная цель деятельности медицинской организации в процессе обзора медицинских изделий заключается в выявлении их реальных свойств, проверке их эффективности и оценке соответствия заявленным характеристикам. В соответствии с установленным порядком регистрации медицинских изделий Росздравнадзор будет включать в свой план проверки результаты испытаний и исследований, которые провела компания-производитель самостоятельно, а также определит необходимые дополнительные этапы в соответствии с требованиями законодательства. Если испытания не проводились, то регистрация медицинского изделия предполагает проведение полного комплекса исследований.
При проведении кlinических исследований в данном случае используется материал, собранный самим заявителем. Важно учитывать, что срок регистрации медицинских изделий продлится на время прохождения данной процедуры. После окончания испытаний результаты будут оформлены в отчете нужного образца, который будет представлен для анализа в государственный контрольный орган.
II этап государственной регистрации: основное звено процедуры
На основе анализа документации, полученной в ходе клинических изысканий, Росздравнадзор принимает решение о продлении процедуры государственной регистрации медицинского изделия. Это будет возможно только при условии, что результаты испытаний подтвердят высокую эффективность изделия в процессе тестирования на людях.
Когда данное условие выполняется, компетентные органы разрабатывают план на проведение нового экспертного исследования, в ходе которого профессиональные эксперты должны тщательно проанализировать результаты проведенных клинических испытаний. В процессе этого анализа определяются не только показатели эффективности продукта, но и оптимальные методы его применения, ограничения в использовании и прочие нюансы. Все выводы и рекомендации специалистов оформляются в виде экспертного заключения, которое отправляется в Росздравнадзор для принятия окончательного решения о регистрации товара или ее отказе.
Принятие решения
Решение Росздравнадзора по постановке товара на учет зависит от полного комплекта документов, содержащих все характеристики продукта. Только имея полные данные, сотрудники ведомства могут проверить наличие причин для отказа по пункту 35 Правил, утвержденных постановлением № 1416. Отрицательные выводы уполномоченной организации, свидетельствующие о недостаточном уровне действенности, безопасности и качества продукта, а также несоответствие реальных характеристик продукта и данных из заявления на регистрацию или сопроводительных документов могут быть включены в список причин для отказа.
Если все условия выполнены, то шансы на успешную регистрацию товара в контролирующем ведомстве повышаются.
Выдача регистрационного удостоверения
Согласно действующему регламенту регистрации медицинских изделий, окончательным этапом процедуры становится получение регистрационного удостоверения. Он представляет собой официальный документ, гарантирующий качество, безопасность и эффективность товара. Аналогично процессу сертификации медицинских изделий, госрегистрация предусматривает ограниченный срок на выдачу итогового документа: максимальный срок — 10 рабочих дней с даты окончания клинических испытаний.
Необходимо отметить, что информация об успешном прохождении продукта государственной регистрации должна быть внесена в специальный Единый реестр медицинских изделий, который доступен на веб-ресурсе Росздравнадзора. В соответствии с законодательством, регистрационные органы обязаны внести необходимые сведения в реестр в кратчайшие сроки после принятия решения о положительном результате регистрации продукта.
Процедура регистрации медицинских изделий
Регистрация медицинских изделий является обязательной процедурой на территории Российской Федерации. Она необходима для обеспечения контроля за качеством и безопасностью производимых и реализуемых на местном рынке медицинских товаров. Это гарантирует, что товары, предлагаемые потребителям, эффективны и безопасны в использовании, что существенно снижает риски нанесения вреда здоровью человека.
Документ Росздравнадзора о регистрации медицинского изделия, подтверждающий соответствие требованиям постановления правительства РФ № 1416 от 27 декабря 2012 года, называется регистрационным удостоверением. Важно отметить, что срок его действия не установлен.
Чтобы продавать медицинские изделия в России, необходимо иметь в своем распоряжении регистрационное удостоверение Росздравнадзора, в обратном случае использование этих изделий становится нелегальным. Надежность всех этапов регистрации МИ на территории РФ гарантируется нашей компанией
Процесс оформления регистрационного удостоверения медицинского изделия

Создание технической и эксплуатационной документации для медицинских устройств
Осуществление технических, токсикологических и электромагнитных испытаний
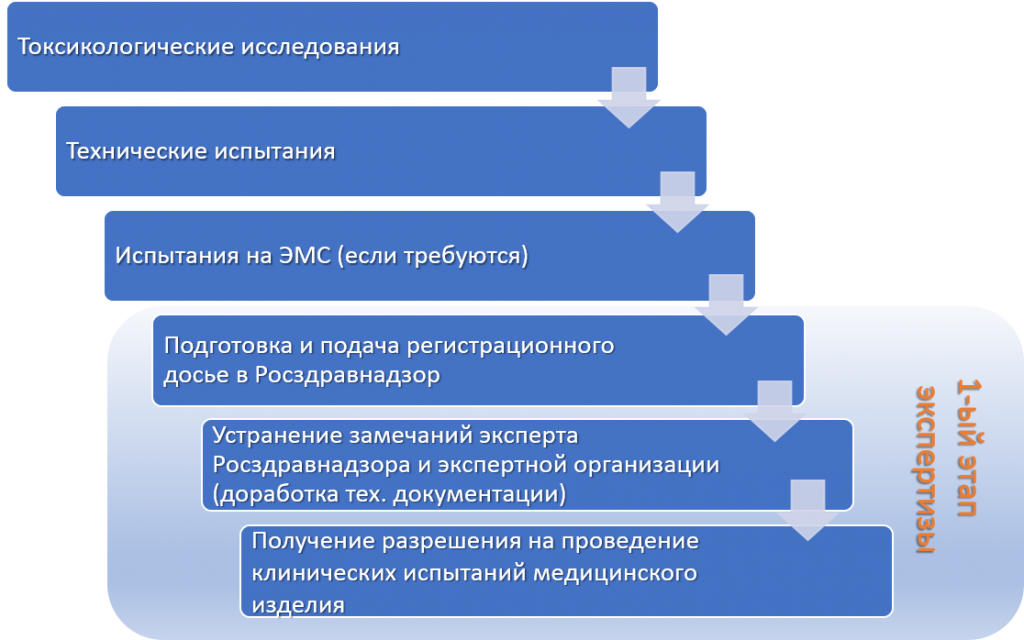
Организация проведения медицинских экспериментов
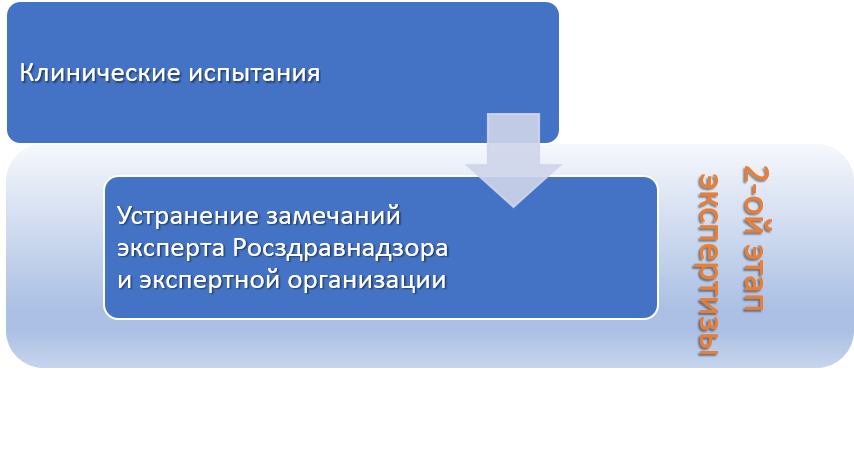
Получение подлинной копии документа в Российском языке
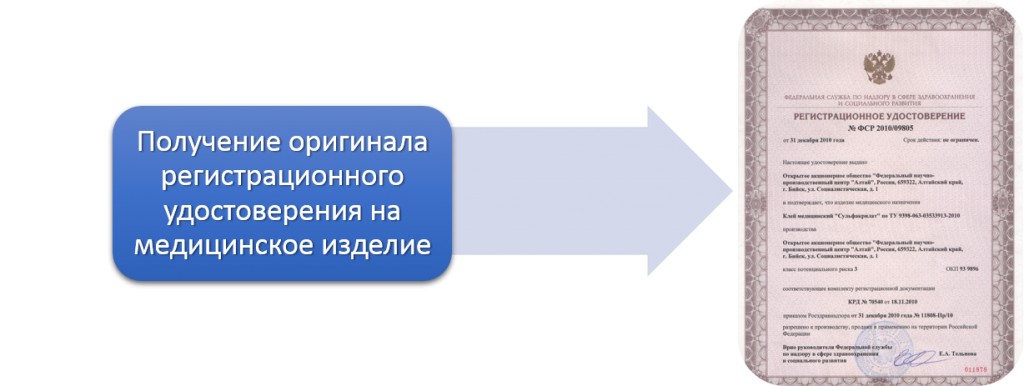
Список документов, необходимых для оформления разрешительной документации для иностранных компаний
- Сертификат о регистрации изготовителя
- Документы, которые подтверждают условия производства медицинских изделий (сертификат/декларация соответствия требованиям Европейской директивы СЕ 93/42, СЕ 98/79; ISO 13485 сертификат стандартов) и соответствие изделий стандартам и требованиям безопасности и качества (национальные сертификаты контроля качества продукции; сертификат свободной продажи; декларация/сертификат соответствия медицинским изделиям с классами риска 1 и 2a, либо 2b и 3)
- Доверенность на имя российского заявителя
- Руководство по эксплуатации
- Технический файл или техническая спецификация
Обратная связь
Новости
Актуальный список ОКПД 2
Пояснения от Министерства здравоохранения о процедуре подтверждения товарного знака при регистрации медицинских изделий
Нужна ли медицинской отрасли Евразийской экономической комиссии такая процедура?
Одним из распространенных заблуждений является то, что для регистрации медицинской техники достаточно иметь только технический паспорт и сертификат качества. На самом деле, процедура регистрации требует предоставления более широкого спектра документов, включая разрешительные документы и документацию о прохождении испытаний и проверок.
Еще одним заблуждением является то, что можно пропустить этап регистрации медицинской техники, если она была приобретена за рубежом. На самом деле, независимо от страны происхождения, все медицинские приборы должны пройти процедуру регистрации в соответствии с законодательством страны, в которой они будут эксплуатироваться.
Также существует заблуждение о том, что регистрация медицинской техники является формальностью, необходимой только для получения лицензии на медицинскую практику. На самом деле, регистрация оборудования не только обязательна, но также гарантирует его соответствие стандартам безопасности и качества, что является важным аспектом в области здравоохранения.
Необходимые документы для регистрации медицинской аппаратуры
Полное сопровождение — быстро и профессионально

Предоставление полной помощи при регистрации медицинских изделий
Регуляторный отдел, специализирующийся в данной области, занимается процессами регистрации медицинских изделий. Профессиональные специалисты контролируют все этапы, включая подготовку необходимых документов и сотрудничество с экспертами. Сегодня, этим отделом было получено и переоформлено более 350 авторизаций на территории РФ и СНГ.
Первый этап

Оформление запроса на технический файл, создание доклада о технических условиях, составление пакета документов для регистрации
Фаза 2

Проведение технических, токсикологических и клинических тестов
Третий этап

Осуществление экспертизы Росздравнадзора с помощью ФГУП ВНИИМТ или ФГУП ЦИМКЭ
Четвертый этап

Прохождение экспертизы успешно завершено
Оплата за регистрацию медицинских изделий и их экспертизу, предназначенных для продажи на рынке России по Правилам Регистрации Медицинских Изделий №1416:
Оплата за получение регистрационного удостоверения медицинского изделия
Оплата за выдачу дубликата регистрационного удостоверения медицинского изделия (ссылка на Пошлина дубликат РУ)
Оплата за внесение изменений в документы, содержащиеся в регистрационном досье медицинского изделия, которые не требуют проведения экспертизы его безопасности, качества и эффективности
Оплата за проведение экспертизы безопасности, качества и эффективности медицинского изделия при его регистрации связана с его потенциальным риском:
Класс 1 — 72 000 руб.;
Класс 2а — 104 000 руб.;
Класс 2б — 136 000 руб.;
Класс 3 медицинского изделия обойдется в 184 000 рублей;
При изменении документов, содержащихся в регистрационном досье медицинского изделия, для проведения экспертизы безопасности, качества и эффективности (в зависимости от класса потенциального риска его применения), стоимость составит:
Класс 1 — 32 000 рублей;
Класс 2а — 48 000 рублей;
Класс 2б — 64 000 рублей;
Класс 3 — 104 000 рублей;
Перечень необходимых документов для регистрации медицинских изделий, производимых в России
| 1 | Копии учредительных и регистрационных документов юридического лица или индивидуального предпринимателя |
| 2 | Технические условия и файл менеджмента риска |
| 3 | Фотографии изделия размером 18х24 (цветные, как в упаковке, так и без, со всеми принадлежностями) |
| 4 | Доверенность на представителя производителя ИМН при регистрации продукции (отечественная компания, занимающаяся регистрацией медицинских изделий) |
| 5 | Руководство по эксплуатации изделия медицинского назначения (ИМН) |
| 6 | Сведения о нормативной документации |
| 7 | Акт квалификационных испытаний |
| 8 | Информация о применении аналогичных медицинских изделий на территории РФ (ссылки в Интернете, брошюры и другие материалы) |
| 9 | Протоколы технических и токсикологических испытаний |
| 10 | Протоколы валидации и верификации программного обеспечения (при необходимости) |
| 11 | Протокол валидации стерилизации (при необходимости) |
| 12 | Отчет о стабильности (при необходимости) |
| 13 | Сертификат ИСО 13485 (при необходимости) |
- Технический файл
- Отчет о испытаниях
- Отчет об испытаниях на электромагнитную совместимость
- Анализ рисков
- Клинический отчет
- Оперативная документация
Документы должны быть заверены печатью, подписью и нотариальным заверением (и апостилем) в стране производителя.
| 1 | Копия документа, подтверждающего полномочия уполномоченного представителя производителя (изготовителя) |
| 2 | Сведения о нормативной документации на медицинское изделие |
| 3 | Техническая документация производителя (изготовителя) на медицинское изделие |
| 4 | Эксплуатационная документация производителя (изготовителя) на медицинское изделие, включая инструкцию по применению или руководство по эксплуатации медицинского изделия |
| 5 | Фотографии медицинского изделия с принадлежностями, необходимыми для его использования (размером не менее 18 x 24 сантиметра) |
| 6 | Документы, подтверждающие результаты технических испытаний медицинского изделия |
| 7 | Документы, подтверждающие результаты токсикологических исследований медицинского изделия, предполагающего контакт с организмом человека |
| 8 | Документы, подтверждающие результаты испытаний медицинского изделия в целях утверждения типа средств измерений |
| 9 | Сертификат системы менеджмента качества ИСО:13485 (требуется нотариальное заверение и апостиль) |
| 10 | Сертификат системы менеджмента качества ИСО:9001 (требуется нотариальное заверение и апостиль) |
| 11 | СЕ сертификат или сертификат свободной торговли или другие (требуется нотариальное заверение и апостиль) |
| 12 | Сведения, подтверждающие клиническую эффективность и безопасность медицинского изделия (при наличии) |
| 13 | Проект программы клинических испытаний медицинского изделия и обосновывающие материалы (при наличии) |
| 14 | Опись документов |
Соблюдение требований России или ЕАЭС при регистрации?
В настоящее время процедура государственной регистрации медицинских изделий разных классов с выдачей специальных разрешительных документов для заявителей находится в переходном режиме и претерпевает изменения. С момента окончания этого периода, с 31 декабря 2021 года, будут действовать правила регистрации ЕАЭС. Кроме того, уже наблюдается внесение изменений в действующий порядок.
Важно знать, что если на 31 декабря 2021 года медицинское изделие будет на стадии одной из национальных процедур регистрации, заявителю будет отказано в проведении государственной регистрации и изменении статуса продукта, из-за изменения правил с переходом на правила ЕАЭС вместо правил России.
Поэтому, если у вас есть нужда в регистрации медицинских изделий и получении соответствующих разрешительных документов в качестве юридического или физического лица, то рекомендуем не откладывать процесс. Необходимо выполнить все необходимые действия своевременно.
Для этого вам потребуется собрать пакет документов (досье) на медицинские изделия и подать его вместе с заявлением. Может потребоваться внести изменения в представленную документацию и/или в процессе обращения (производство, продажа) медицинскими изделиями. Важно учесть возможные неожиданности и сбои заранее.
Не забывайте об оплате пошлины и времени, необходимом на проверку, оценку, утверждение и выдачу разрешительных документов. Это позволит выполнить поставленную цель без риска в полном объеме и соблюсти отведенные сроки!
Свяжитесь с нами по указанным на нашем сайте номерам телефонов или воспользуйтесь другим удобным для вас способом связи. Мы готовы взять на себя все ваши обязательства по регистрации медицинских изделий, быстро и качественно выполнив работу в течение нескольких рабочих дней, а также значительно сэкономив ваше время и деньги.
Я рекомендую ООО "ФармМедПолис РТ" в качестве надежного подрядчика для всех, кто нуждается в помощи в процессе получения регистрационного удостоверения. Компания работает на высоком уровне.
Осведомлённость ООО "ФармМедПолис РТ" о регуляторных процессах помогла нам получить регистрационные документы в оговоренные сроки и в полном соответствии с требованиями. Мы рады, что выбрали именно эту компанию в качестве нашего партнера.
Е.А. Слепчук
Генеральный директор ООО "ЛЕО-Медикал Продакшин"
Компания «ФармМедПолис РТ» оказала помощь в регистрации медицинских изделий и решила все возникшие в процессе работы вопросы, а также помогла найти поставщиков сырья. Особо хочется выделить профессионализм экспертов, которые всегда были на связи и ответили на все возникающие вопросы, а также клиентоориентированность компании.
В.В. Дюкин
Генеральный директор ООО «СИГМА ХЕЛСКЭР»
Э.В. Хуснутдинов
Директор ООО «Айрон Индастри Компани»
Часто задаваемые вопросы:
Какие документы необходимы для регистрации медицинских изделий?
Какие изделия относятся к медицинским?
В соответствии с Федеральным законом от 21.11.2011 N 323-ФЗ (ред. от 25.06.2012) "Об основах охраны здоровья граждан в Российской Федерации", любые материалы, оборудование, приборы, аппараты, инструменты и другие изделия, применяемые в медицинских целях отдельно или в комбинации друг с другом, а также с принадлежностями, необходимыми для их использования, являются медицинскими изделиями.
Какие медицинские изделия допустимы к использованию на территории Российской Федерации?
Согласно статье 38 Федерального закона от 21.11.2011 N 323-ФЗ (ред. от 25.06.2012) "Об основах охраны здоровья граждан в Российской Федерации", медицинские изделия, зарегистрированные в соответствии с установленным Правительством Российской Федерации порядком, можно использовать на территории Российской Федерации. Уполномоченный федеральный орган исполнительной власти также имеет право на их использование.
Какие документы требуется предоставить при государственной регистрации медицинских изделий для подтверждения их качества, если они содержат лекарственные средства?
Согласно постановлению Правительства Российской Федерации от 31.05.2018 № 633 "О внесении изменений в Правила государственной регистрации медицинских изделий", при государственной регистрации медицинского изделия заявитель должен предоставить копии документов, подтверждающих качество лекарственного препарата, фармацевтической субстанции, биологического материала и других веществ, которые используются или входят в состав медицинского изделия и предназначены для его применения в соответствии с назначением, указанным производителем, и выданных в соответствии с законодательством страны происхождения указанных веществ.
Какие сборы нужно уплатить при регистрации медицинских изделий в государственных органах?
Для успешного получения регистрационного удостоверения необходимо заплатить государственную пошлину в размере семи тысяч рублей и оплатить экспертизу качества и безопасности медицинского изделия. Стоимость экспертизы зависит от класса потенциального риска и составляет 45000 рублей для 1 класса, 65000 рублей для 2а класса, 85000 рублей для 2б класса и 115000 рублей для 3 класса.
Как подать документы для государственной регистрации медицинских изделий?
В соответствии с Правилами государственной регистрации медицинских изделий, документы можно предоставить лично по адресу: 109074, город Москва, Славянская площадь, дом 4, строение 1, либо отправить по почте на тот же адрес.
Кто имеет право подавать заявление на регистрацию медицинских изделий перед государством?
В соответствии с пунктом 8 Правил государственной регистрации медицинских изделий, утвержденных постановлением Правительства Российской Федерации от 27.12.2012 г. N 1416, заявитель для регистрации может быть разработчик, производитель медицинского изделия, или уполномоченный представитель производителя.
Какие медицинские изделия не относятся к товарам, подлежащим государственной регистрации?
Согласно пункту 2 Правил государственной регистрации медицинских изделий, утвержденных постановлением Правительства РФ от 27.12.2012г. №1416, медицинские изделия, изготовленные заказчиками с особыми требованиями по назначению медицинских работников и предназначенные исключительно для личного использования, регистрации у государства не подлежат. Пожалуйста, уточните, какой срок потребуется для государственной регистрации медицинского изделия при сотрудничестве с нами?
В среднем регистрация медицинских изделий классов потенциального риска применения 2а, 2б и 3 занимает от 8 до 12 месяцев, в то время как для 1-го класса риска этот срок составляет от 4 до 8 месяцев. Если медицинское изделие предназначено для диагностики in vitro, то срок регистрации увеличивается на примерно 2 месяца из-за загруженности лабораторий, аккредитованных на такие изделия. Кроме того, время регистрации зависит от скорости предоставления заказчиком запрашиваемой информации.
Недавно был добавлен упрощенный порядок государственной регистрации, включающий следующие шаги:
1. Росздравнадзор в течение трех рабочих дней проверяет предоставленный комплект документов на достаточность, правильность оформления, полноту и достоверность содержащейся в нем информации. Если в какой-то момент выявляются недостатки или несоответствия, заявителю сообщают об этом.
В течение 5 рабочих дней заявитель может устранить ошибки, которые возникли при заполнении регистрационного комплекта, без необходимости подачи новой заявки. Если же заявитель не исправил ошибки в указанный срок или предоставил неполный пакет документов, то ведомство вернет ему предоставленный комплект. В таком случае заявитель будет вынужден подавать новую заявку, но он сможет воспользоваться упрощенной процедурой только еще один раз.
Когда проверка комплекта документов завершена, ведомство выдает заявителю регистрационное удостоверение. После получения этого документа продажа товара становится возможной. Необходимо учесть, что срок действия данного удостоверения ограничен и составляет 150 рабочих дней.
Заявитель обязан в течение 150 рабочих дней выполнить всю оставшуюся работу по регистрации медицинского товара. В процесс входит не только проведение технических и токсикологических испытаний конкретного продукта в ФГБУ "ВНИИМТ" Росздравнадзора, но также необходимость организации клинических испытаний в официально аккредитированных медицинских учреждениях. После выполнения каждого испытания составляют окончательный отчет, который будет включен в комплект документов, подаваемый в Росздравнадзор. После предоставления документов ведомство осуществляет проверку на полноту и корректность оформления комплекта, а также проверку достоверности содержащихся в нем данных. Срок проведения проверки составляет 5 рабочих дней.
Если в процессе регистрации будут выявлены недостатки, то заявителю будет предоставлено 30 дней на их устранение. Если владелец заявки не сможет исправить допущенные ошибки, то заявка будет отправлена на доработку с возможностью ее повторной подачи, но не более одного раза.
Если проверка пройдена успешно, Росздравнадзор назначает экспертизу действенности, безопасности и качества медицинского продукта. Экспертизу проводит уполномоченная организация, после чего составляется мотивированное заключение о соответствии или несоответствии продукта требованиям. В случае положительного заключения регистрационное удостоверение становится бессрочным, в противном случае он аннулируется и товар больше нельзя продавать на рынке.
Вы обеспечиваете получение регистрационного удостоверения?
Мы гарантируем получение РУ, если будут соблюдены все условия услуг. В случае отказа по нашей вине мы возвращаем полную стоимость услуг.