Ион коагулятор — это устройство, используемое для обеззараживания и очистки воды путем коагуляции загрязнений. Чтобы определить, нужно обратить внимание на его принцип работы и способ установки.
Далее в статье мы подробно рассмотрим, как ион коагулятор работает, как правильно выбрать и установить устройство, и какие преимущества оно может принести вашему водопроводу. Вы узнаете о том, какой эффект дает использование ион коагулятора и как правильно ухаживать за ним. Будем рассматривать различные модели и сравнивать их особенности, чтобы помочь вам сделать правильный выбор.
- Ион коагулятор — это устройство, которое используется для очистки воды от загрязнений и бактерий путем обезвреживания микроорганизмов.
- Для определения ион коагулятора необходимо обратить внимание на его основные характеристики: мощность, производительность, тип использования (для домашнего или профессионального использования).
- Ион коагуляторы могут быть как переносные, так и стационарные. Переносные устройства удобны для использования дома или на даче, а стационарные — для очистки воды в промышленных масштабах.
- Основным критерием выбора ион коагулятора является его эффективность в очистке воды от бактерий и загрязнений. Для этого необходимо обращать внимание на рейтинг производителя, отзывы пользователей и наличие сертификатов качества.
- При выборе ион коагулятора также следует обратить внимание на его стоимость, технические характеристики, гарантии и сервисное обслуживание. Важно выбрать устройство, которое будет соответствовать вашим потребностям и бюджету.
Электролиты и коагуляция гидрозолей. Порог коагуляции
Уже давно известно, что гидрозоли склонны к коагуляции при добавлении небольшого количества электролитов, что привлекло внимание многих исследователей.
Электролит, вызывающий разрушение агрегативной стабильности золи, называется коагулянтом или электролитом-коагулятором.
Коллоидные растворы чрезвычайно чувствительны к наличию посторонних электролитов, и даже небольшое количество может вызвать их коагуляцию. Например, если золь был сформирован в плохо промытой посуде, которая сохраняет следы солей, содержащихся в водопроводной воде, коагуляция происходит почти немедленно после образования золи.
Малые количества электролита-регулятора могут сохранять агрегативную устойчивость коллоидных растворов. Порог коагуляции g — это наименьшая концентрация электролита, при которой происходит явная коагуляция коллоидного раствора. Нахождение этого порога можно осуществить двумя способами: путем постепенного добавления раствора электролита-коагулятора в золю из бюретки или приготовлением серии растворов с равномерной увеличивающейся концентрацией электролита и последующим добавлением одинаковых объемов золя. Визуальное наблюдение или оптические методы помогают определить наступление коагуляции. Порог коагуляции можно вычислить по формуле или, учитывая разбавление, более точно.
В данной формуле аббревиатуры С эк, V эк и V золь соответствуют концентрации, объему раствора электролита-коагулятора и объему коллоидного раствора соответственно.
Обычно, порог коагуляции измеряется в моль/литр или ммоль/литр. Однако, необходимо помнить, что его физический смысл заключается в количестве электролита (в моль или ммоль), необходимое для вызова коагуляции одного литра коллоидного раствора.
Кроме порога коагуляции, в коллоидной химии также применяется коагулирующая способность обратная ему, обозначаемая Р:
Ее размерность составляет литры на моль или литры на ммоль, что означает объем золя, который может быть скоагулирован одним молем (или миллимолем) электролита.
Показатель порога коагуляции и коагуляционная способность являются относительными параметрами, поскольку зависят от множества факторов, включая скорость добавления электролита-коагулятора, способ приготовления золя, метод регистрации, промежуток времени между добавлением электролита и моментом фиксации явной коагуляции, температуру и другие.
Исследования указывают на то, что ионы электролита-коагулятора обладают коагулирующим эффектом, если их заряд противоположен заряду гранул коллоидных мицелл. Коагуляционное действие значительно возрастает с увеличением заряда коагулирующего иона. Это известно как правило Шульце-Гарди, установленное в 1882 и 1900 годах соответственно. Другими словами, катионы вызывают коагуляцию золя с отрицательно заряженными гранулами, а анионы — у золя с положительно заряженными гранулами.
Согласно исследованию, отношение порогов коагуляции коагулирующих ионов, которые имеют одну, две или три зарядности, примерно обратно пропорционально шестой степени их валентности.
Интересно отметить, что приблизительно в 25-30 мВ абсолютной величине z-потенциала, независимо от знака заряда гранулы, наблюдается снижение вблизи порога коагуляции. Это значение является критическим и при дальнейшем снижении величины z-потенциала золь практически теряет устойчивость. Таким образом, главным фактором устойчивости золей является значение электрокинетического потенциала, что установлено благодаря тщательным исследованиям коагулирующего действия различных ионов с одинаковой величиной заряда. Было отмечено, что они формируют ряды, близкие к лиотропным рядам адсорбции.
Если не все факторы устойчивости снимаются, то не каждое столкновение мицелл может закончиться их агрегированием, и для полной коагуляции золя может потребоваться большое количество времени. Такая коагуляция называется медленной. Если же защитный фактор в системе практически отсутствует, то происходит быстрая коагуляция, когда каждое столкновение частиц приводит к их объединению.
Важно отметить, что термины "быстрая" и "медленная коагуляция" относятся к механизму процесса, а не к реальному времени его протекания. Так, при большой концентрации мицелл "медленная" коагуляция может закончится за короткое время из-за частых столкновений, а при малой концентрации мицелл "быстрая" коагуляция может занять достаточно продолжительное время. Тем не менее, в большинстве случаев реальная скорость коагуляции все же определяется механизмом.
Путем проведения экспериментов была исследована кинетика коагуляции. Результаты указывают, что при нулевом или очень маленьком значении z-потенциала происходит быстрая коагуляция. Также было установлено, что медленная коагуляция наблюдается в случае значений, близких к критическому, которые значительно выше тех, которые вызывают быструю коагуляцию.
Морская и океанская вода более прозрачна благодаря коагуляции, которая происходит при воздействии электролитов на дисперсии, включая коллоидные частицы, содержащиеся в речной, озёрной и болотной воде. Эти частицы образуются при выветривании горных пород и размывании глин и глинистых грунтов. В результате вода становится мутной.
Однако, когда реки впадают в моря, электролиты, содержащиеся в морской воде, связываются с этими дисперсиями и вызывают коагуляцию. Это приводит к образованию осадка, который формирует отмели около устьев рек. В результате вода становится более прозрачной за пределами этих отмелей.
Электролитная коагуляция может привести к образованию холестериновых бляшек внутри кровеносных сосудов и отложению солей в суставах при нарушении солевого баланса крови. Также этот механизм позволяет агглютинировать эритроциты при свертывании крови.
В настоящее время нет единой количественной теории коагуляции и агрегативной устойчивости, хотя в коллоидной химии разработано множество теорий, в которых устойчивость гидрофобных золей и коагулирующее действие электролитов связываются с разными параметрами системы. Каждая из этих теорий объясняет некоторые факты, но не может дать полного ответа на все вопросы, так как строится на связи процесса коагуляции с отдельным параметром системы.
Источник: "6.5. Теории коагуляции"
Появление коагуляции объясняется химическими реакциями на границе фаз, приводящими к нейтрализации поверхностного заряда — это высказывание поддерживал химик П. Э. Дюклов. Одновременно Г. Фрейндлих создал адсорбционную теорию, в которой уменьшение заряда частиц объяснялось адсорбцией ионов противоположного знака. Согласно Г. Мюллеру, увеличение концентрации ионов электролита-коагулянта при постоянном заряде на поверхности частиц приводит к снижению их z -потенциала и, следовательно, к уменьшению устойчивости системы, таково объяснение электростатической теории.
Теория А. И. Рабиновича изучает взаимодействие ионного обмена и уменьшение z-потенциала. Роль z-потенциала в коагуляции описывается в пункте 6.4. В теории В. Оствальда коагуляция определена как вытеснение дисперсной фазы межионными силами притяжения, которые действуют в дисперсионной среде. В этой концепции параметр, который определяет коагуляцию, – это коэффициент активности электролита.
По-видимому, все механизмы коагуляции, которые описаны в этих теориях, действуют в какой-то мере. Преобладающее значение какого-либо из них зависит от свойств дисперсной системы и коагулянта, а также от внешних факторов, таких как температура, механическое воздействие и так далее.
В настоящее время широкое распространение получила теория коагуляции, основанная на физическом подходе. Советские ученые Б. В. Дерягин и Л. Д. Ландау разработали эту теорию в период с 1937 по 1941 гг., а голландские ученые Э. Фервей и Й. Овербек представили свой независимый вариант в 1948 году. Таким образом, теория получила название ДЛФО. Однако, как и многие другие теории, она не объясняет весь механизм коагуляции. Тем не менее, это позволяет нам получать количественные зависимости, например, определять пороговые значения для коагуляции различных электролитов.
Основу теории динамики легко диспергируемых фаз (ДЛФО) составляет сравнение межмолекулярных взаимодействий частиц дисперсной фазы в дисперсионной среде, электростатических взаимодействий диффузных ионных слоев и тепловых движений частиц дисперсной фазы.
Эта теория строгоя и количественно обобщила и усовершенствовала представление об электростатической стабильности коллоидных растворов, изложенные в работах Г. Мюллера, А. И. Рабиновича и В. А. Каргина. Как уже было сказано, добавление электролита в коллоидную систему вызывает сжатие двойного электрического слоя и, следовательно, уменьшение расстояния на котором между частицами возникают силы отталкивания. В такой ситуации при броуновском движении твердых оснований частицы (агрегаты) могут приближаться друг к другу на меньшие расстояния. На малых расстояниях межмолекулярные силы притяжения становятся очень значимыми.
В процессе приближения коллоидных частиц наблюдаются два вида взаимодействия — притяжение и отталкивание. Согласно закону Ньютона, силы притяжения уменьшаются обратно пропорционально квадрату расстояния между частицами. Силы отталкивания происходят из электростатического взаимодействия заряженных коллоидных частиц и давления, которое возникает в структурно-механическом слое на поверхности частиц (известное как "расклинивающее давление" в терминах Б. В. Дерягина). Это давление проявляется в перекрывающихся гидратно-адсорбционных слоях при столкновении мицелл и наложение его на кулоновские силы приводит к экспоненциальному уменьшению сил отталкивания при увеличении расстояния между коллоидными частицами.
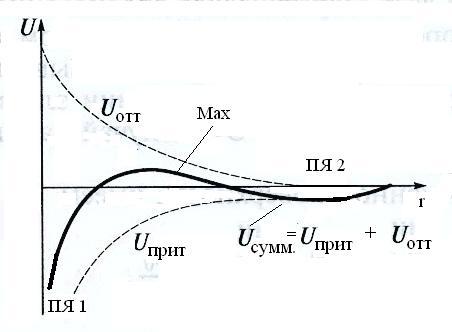
Таким образом, сближение коллоидных частиц друг с другом определяется балансом двух противоположных сил — силы отталкивания и силы притяжения. Их соотношение можно наглядно изобразить на энергетической кривой взаимодействия (см. рис. 6.1). Анализ кривой позволяет выявить наличие двух минимумов и одного максимума, что указывает на преобладание силы притяжения на малых и больших расстояниях между частицами, и силы отталкивания на средних расстояниях.
Рис. 6.1. Зависимость энергии взаимодействия между коллоидными частицами
от расстояния между ними d
- Энергия электростатического отталкивания
- Энергия притяжения
- Результирующая энергия взаимодействия
- Дальний минимум
- Ближний минимум
- Максимум
Притяжение частиц через прослойку среды происходит при достижении минимального расстояния между ними, что приводит к образованию флокул. Однако глубина минимума связана с ослаблением сил притяжения из-за расстояния между частицами и действия расклинивающего давления. Именно поэтому такие флокулы легко разрушаются при введении пептизатора или энергичном перемешивании.
Максимум, расположенный на средних расстояниях между частицами, характеризует потенциальный барьер, который препятствует прямому контакту между ними. Такой барьер образуется из-за наложения адсорбционно-сольватных слоев и электрокинетического потенциала z. Чем выше z-потенциал, тем выше потенциальный барьер, который не позволяет частицам подходить слишком близко друг к другу.
Практический опыт показал, что для достижения агрегативной устойчивости дисперсной системы, необходимо преодолеть барьер, появляющийся при зет-потенциале, равном 20-30 милливольт. По теории диффузно-слоевой модели, электролит-кагулятор играет роль в снижении потенциального барьера за счет электростатической составляющей, которая привязана к зет-потенциалу. Квантифицированные уравнения диффузно-слоевой модели позволяют расчет порогов кагуляции для золей различных электролитов. Согласно этим уравнениям, пороги кагуляции для одно-, двух- и трехзарядных ионов обратно пропорциональны шестой степени зарядности ионов, что соответствует правилу Шульце-Гарди.
Если сила препятствия незначительна и скорость движения входящих частиц достаточно большая, то они могут приблизиться к минимальному расстоянию min 2. В результате этого сближения гидратные оболочки могут быть вытеснены, и частицы могут вступить в непосредственный контакт. В случае твердых частиц это приведет к образованию очень прочных связей, которые, в свою очередь, приведут к необратимой коагуляции. Если же частицы жидкости или газа сближаются, то происходит коалесценция — их слияние.
Однако, теория ДЛФО имеет приближенный характер, так как она не учитывает много факторов, таких как природа ионов с одинаковым зарядом, которая выражается через лиотропные ряды коагуляции, специфическую адсорбцию ионов и другие.
6.6. Кинетика коагуляции.
В начале ХХ века М. Смолуховский заложил основы учения о kinetike коагуляции, то есть ее процессе во времени. Данное учение было далее развито другими исследователями, такими как Г. Мюллер и Н. А. Фукс.
Теория Смолуховского основана на представлении, что при потере агрегативной устойчивости происходит слияние только двух частиц, так как вероятность встретить более трех частиц в пространстве крайне мала. Механизм коагуляции можно рассматривать как бимолекулярную химическую реакцию, где двойная частица возникает при столкновении двух одиночных, тройная — при столкновении двойной и одиночной, четверная — из двух двойных и т.д. Скорость коагуляции зависит от концентрации частиц в системе, скорости их диффузии, вязкости среды и температуры. С помощью теории было выведено уравнение, связывающее количественные характеристики частиц в момент их образования и их изначальной концентрации.
Константа скорости коагуляции, обозначаемая как К, является параметром, который трудно определить экспериментально или вычислить. Однако можно использовать уравнение, которое включает в себя время половинной коагуляции – t 12, за которое число частиц уменьшается вдвое. Согласно уравнению (6.1), можно получить следующее выражение:
n 0/2 = 1 + Kn 0 t 1/2
Чтобы вычислить время половинной коагуляции, можно воспользоваться уравнениями Фика для скорости диффузии и Эйнштейна для коэффициента диффузии. Для этого нужно использовать уравнение:
тут уравнение
Правила электролитной коагуляции
1. Коагуляцию коллоидного раствора может вызвать любой сильный электролит при определенной концентрации.
2. Согласно правилу знака заряда, коагуляция золя происходит под действием иона-коагулятора, заряд которого противоположен заряду коллоидной частицы.
Электролит, содержащий ион-коагулятор, называется коагулирующим электролитом.
3. Каждый электролит имеет свой порог коагуляции по отношению к коллоидному раствору.
Порог коагуляции (γ, С кр) — это минимальная концентрация коагулирующего электролита, которая вызывает коагуляцию золя:
где γ — порог коагуляции (моль/л), V — объем используемого электролита (мл), C — концентрация электролита (моль/л), W — объем золя (мл).
Сила коагулирующего электролита (P) обратно пропорциональна его порогу коагуляции:
4. Воздействие заряда иона коагулятора на коагуляцию (правило Шульце-Гарди). Чем больше валентность иона коагулятора, тем выше его способность к коагуляции.
Здесь валентность (заряд) иона коагулятора равна n=2-6.
5. Коагулирующая сила ионов-коагуляторов с одинаковой валентностью увеличивается с ростом их радиуса (лиотропные ряды).
Например, для получения золя гидроксида цинка были смешаны растворы ZnCl2 и NaOH. Если пороги коагуляции растворов электролитов являются:
| Электролит | Na2SO4 | Mg(NO3)2 | Na3PO4 | NaCl |
| γ, моль/л | 0.05 | 3.0 | 0.004 | 3.0 |
то нужно определить знак заряда коллоидных частиц и записать формулу мицеллы.
Для определения знака заряда коллоидной частицы золя необходимо рассмотреть коагуляцию золя. Однако, катионы электролитов-коагуляторов имеют разные пороги коагуляции, что не соответствует правилу Шульце – Гарди. Следовательно, анионы электролитов вызывают коагуляцию золя. В соответствии с правилом Шульце – Гарди, высокий заряд аниона приводит к меньшему порогу коагуляции. Следовательно, заряд коллоидной частицы положительный. Потенциалопределяющие ионы – Zn 2+ , противоионы – Сl – .
Рассмотрим строение мицеллы и запишем его формулу.
В качестве примера рассмотрим получение золя иодида серебра из растворов KI и AgNO3. Исходя из известных порогов коагуляции растворов электролитов, определим знак заряда коллоидной частицы и запишем формулу мицеллы.
| Электролит | NaCl | NaNO3 | Ca(NO3)2 | Ce(NO3)3 |
| γ, моль/л | 3,2 | 3,1 | 0,05 | 0,006 |
Для определения знака заряда частиц золя необходимо рассмотреть их коагуляцию. Изучив разные электролиты-коагуляторы, можно прийти к выводу, что это не анионы, а катионы вызывают коагуляцию. Одновалентность всех анионов указывает на то, что правило Шульце-Гарди не выполняется. Следовательно, заряд коллоидной частицы отрицательный, что подтверждает "правило знака заряда". Потенциалопределяющие ионы в данном случае — I-, противоионы — Na+.
Согласно полученным результатам, строение мицеллы записывается следующим образом:
В данном примере был получен золь гидроксида алюминия путем слияния растворов AlCl3 и NaOH. Необходимо определить знак заряда коллоидных частиц и написать формулу мицеллы, учитывая, что пороги коагуляции электролитов имеют следующие значения:
| Электролит | Na2SO4 | Mg(NO3)2 | Na3PO4 | NaCl |
| γ, моль/л | 0,011 | 0,70 | 0,001 | 0,70 |
Для начала необходимо определить знак заряда частиц золя. Из таблицы можно заметить, что у Mg(NO3)2 и NaCl пороги коагуляции одинаковы, что значит, что у них одинаковый анион, но разный катион. Следовательно, анионы электролитов вызывают коагуляцию золя.
В данной ситуации становится очевидным, что чем выше заряд аниона, тем менее вероятна коагуляция (правило Шульце-Гарди). Следовательно, коллоидная частица имеет положительный заряд и потенциалопределяющими ионами являются Al3+, а противоионами — Cl- согласно "правилу знака заряда".
Рассмотрим структуру мицеллы:
5.3. Теория устойчивости лиофобных дисперсных систем ДЛФО
В ходе развития коллоидной химии было предложено множество теорий, которые пытались объяснить стойкость гидрофобных коллоидных частиц, включая эффект коагуляции, через различные параметры системы и явления, возникающие при взаимодействии дисперсной фазы с дисперсионной средой.
Каждая из теорий, таких как химическая, адсорбционная, электростатическая и другие, не могла полностью объяснить множество факторов, связанных с процессом коагуляции, так как они были ограничены в своей односторонней природе и соотносились только с определенным параметром системы.
Однако в современной физической теории устойчивости, созданной Б.В. Дерягиным совместно с Л.Д. Ландау в 1937-1941 гг., были представлены результаты исследований, которые были аналогичным образом описаны независимыми исследователями Е. Фервеем и Дж. Овербеком.
Сегодня эта теория известна как теория ДЛФО (DLFO) и представляет собой понимание устойчивости системы коагуляции, основанное на фундаментальных физических законах.
В современной теории устойчивости дисперсных систем процесс коагуляции рассматривается как последствие действия двух видов сил – притяжения Ван-дер-Ваальса и отталкивания электростатических сил между частицами. В зависимости от уравновешенности этих сил в тонком слое жидкости между сближающимися частицами появляется «расталкивающее давление».
Вам понравилась статья? Сохраните ее в закладки (CTRL+D) и поделитесь с друзьями:
Ион коагулятор — это устройство, используемое для удаления загрязнений из воды путем ионизации частиц и их сгущения в флокулянты, которые затем можно легко удалить. Определить ион коагулятор можно по нескольким характеристикам, таким как эффективность удаления загрязнений, скорость обработки воды, степень автоматизации процесса и т.д.
Для определения подходящего ион коагулятора необходимо провести анализ качества воды, определить тип и количество загрязнений, которые необходимо удалить, а также учесть объем и поток воды, который будет подвергаться обработке. Также важно обратить внимание на энергопотребление, рабочее давление, размер и вес устройства.
Для выбора оптимального ион коагулятора рекомендуется обратиться к специалистам, провести консультацию с производителями и изучить отзывы пользователей. При выборе устройства необходимо также учитывать бюджетные ограничения и технические характеристики самого предприятия.
Коагуляция. Применение электролитов для изменения агрегативной устойчивости
Коагуляция – процесс соединения частиц, который приводит к формированию более крупных агрегатов и нарушению седиментационной и фазовой устойчивости, в итоге происходит разрушение дисперсных систем. Агрегативная устойчивость характеризует способность системы сохранять дисперсность и индивидуальность частиц дисперсного фазы.
При потере аграрной устойчивости коагуляция вызывает образование осадков в виде плотных, хлопьевидных, волокнистых или кристаллоподобных образований. При увеличении концентрации сильных электролитов до критического значения порога коагуляции происходит их коагуляция. Исследования скорости коагуляции показывают, что при малой концентрации скорость равна нулю, а при дальнейшем увеличении концентрации скорость растет до определенного значения и затем перестает изменяться. Устойчивость, медленная и быстрая коагуляция являются тремя четко разграниченными зонами.
2. Закон сохранения электрического заряда
В 1900 году Шульц и Гарди провели исследование, из которого следует, что коагуляцию вызывают все электролиты в определенной концентрации, но это свойство не присуще всем ионам в составе электролита. Тот ион, который несет заряд, противоположный знаку заряда коллоидных частиц, называется ион-коагулятором. Следовательно, для систем с отрицательно заряженными частицами, катионы являются ионами-коагуляторами, а для систем с положительно заряженными частицами – анионы.
Существуют пары коагуляции, каждый электролит имеет свой порог коагуляции по отношению к золю. Порог коагуляции γ – это наименьшее количество электролита, которое необходимо для вызова явной коагуляции. Начало коагуляции можно заметить по возникновению мутности в системе. Порог коагуляции γ вычисляется по формуле: γ = V*C/W, где V – объем электролита, C – его концентрация, W – объем золя.
Коэффициент, обратный порогу коагуляции, называется коагулирующей силой электролита: p = 1/3. Правило валентности, известное также как правило Шульце-Гарди, было установлено Шульцем и Гарди. Они доказали, что коагулирующая сила иона-коагулятора возрастает с повышением его заряда. Было определено, что эмпирические пороги коагуляции взаимосвязаны с зарядом иона-коагулятора по формуле: p = K/Z^6, где Z — заряд иона-коагулятора; K — константа.
В некоторых случаях порог коагуляции определяется эмпирическим правилом Эйлерса-Корфа, в котором показатель степени при Z уменьшается до 2: p = K/Z^2. Иногда экспериментальные данные не соответствуют ни правилу Шульце-Гарди, ни правилу Эйлерса-Корфа, а зависимость порога коагуляции от заряда иона коагуляции оказывается промежуточной.
Исследования коагуляции доказали, что порог коагуляции у ионов одинакового заряда понижается по мере увеличения их радиуса. Согласно образовавшемуся лиотропному ряду, ионы Li +, Na +, K +, Rb +, Cs + убывают в порядке возрастания радиуса и увеличения коагулирующей способности, что связано с понижением порога коагуляции.
Принципы коагуляции электролитами
Если в систему добавить некоторое количество электролита, который химически не реагирует с дисперсной фазой, то возникает явление, называемое коагуляцией. Ученый Г. Шульце зафиксировал, что вызвать коагуляцию может только один из ионов электролита, который называют ионом-коагулятором.
Коагулирующая способность этого иона возрастает в геометрической прогрессии при соотношении 1:100:1000 с увеличением заряда иона. Этот закон называется правилом значности или правилом Шульце. Открытие, сделанное Ландау и Дерягиным, показало, что коагулирующая способность изменяется в соответствии с 6-ой степенью заряда ионов: 1 6 :2 6 :3 6 = 1:64:729. Позже исследования М. Гарди показали, что заряд коагулирующего иона всегда противоположен заряду гранулы мицеллы — это правило Гарди. Следовательно, отрицательная гранула коагулирует под влиянием положительно заряженных ионов, а положительно заряженная гранула — под действием анионов добавляемого электролита.
Было выявлено, что закономерности, открытые Шульце и Гарди, могут быть объединены в одно правило, названное правилом Шульце-Гарди. Согласно данному правилу, ион электролита, имеющий противоположный заряд гранулы, обладает коагулирующим действием. Кроме того, чем выше заряд иона-коагулятора, тем сильнее его коагулирующее действие.
Чтобы сравнить различные электролиты и оценить их свойства, используется понятие «порог коагуляции». Это минимальная концентрация добавляемого электролита, при которой наблюдается начало коагуляции.
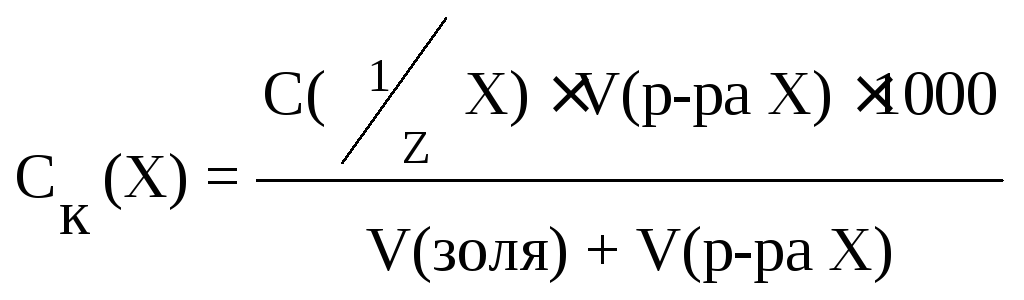
Порог коагуляции может различаться в зависимости от многих факторов, включая время измерения после добавления электролита, метод наблюдения, концентрацию раствора и концентрацию добавленного электролита. Определение порога коагуляции может происходить через измерение светорассеяния или процесс титрования коллоидного раствора добавлением электролита, до тех пор, пока не начнется прямого зрительного наблюдения явной коагуляции.

Коагуляционная способность — это показатель, обратный порогу коагуляции. Он отражает объем зольного раствора, который скоагулирован при воздействии 1 ммоль иона-коагулятора. Чем выше указанный показатель, тем меньше электролита необходимо для вызова коагуляции.
Значение коагуляционной способности зависит от атомной массы и зарядов ионов — то есть от плотности их зарядов. С увеличением атомной массы плотность заряда уменьшается, что связано с уменьшением поляризуемости ионов. Затем также происходит разрушение сольватной оболочки ионов. Из-за этого крупные ионы проще проникают в адсорбционный слой мицелл, нейтрализуя заряд частицы и вызывая коагуляцию золя.
Теории коагуляции электролитами
Для примера, при использовании золя иодида серебра с составом xK+ и индифферентными электролитами, коагуляторами являются ионы K+, Na+, Ca2+, Al3+, Th4+ а соединениями, которые их замещают KNO3, NaNO3, Ca(NO3)2, Al(NO3)3, Th(NO3)4. Изучение коагуляции связано с тремя основными вопросами: 1) почему наступает коагуляция при определенной концентрации электролита-коагулятора; 2) как происходит коагуляция и 3) какова зависимость порога блокировки от свойств электролита-коагулятора.
Какова роль концентрации иона, противоположного заряду гранулы, в данном случае, и почему она является основной?
Почему воздействие заряда иона-коагулятора подчиняется правилу Шульце-Гарди?
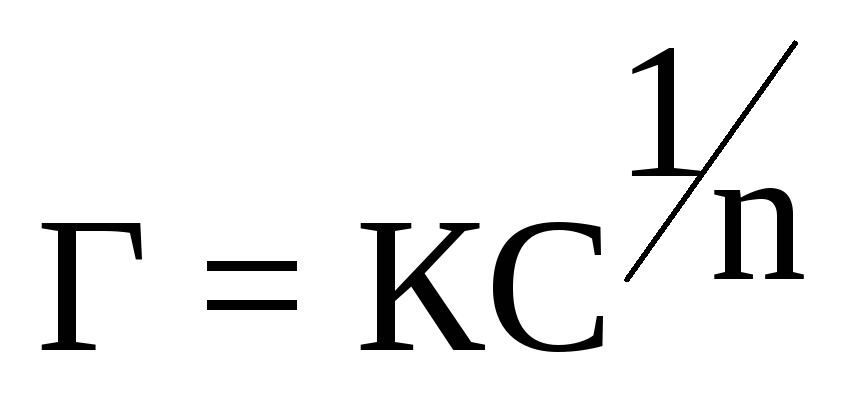
Теория Фрейндлиха объясняет адсорбцию коагуляторов на поверхности частиц посредством изотермы адсорбции. Процесс коагуляции происходит при постепенном уменьшении дзета-потенциала за счет адсорбции различных ионов. Нейтрализация уменьшает число зарядов, что понижает z-потенциал до критического значения.
Однако, теория имеет ограничения, поскольку не всегда можно зафиксировать эквивалентную адсорбцию и разные ионы имеют различные изотермы адсорбции. Кроме того, иногда коагуляция затрагивает только диффузный слой.
Существует теория Мюллера об электростатике, согласно которой введение электролита не влияет на общий заряд в растворе коллоидных частиц, а просто уменьшает толщину диффузионного слоя, вытесняя противоионы в адсорбционный слой. Это, в свою очередь, снижает z-потенциал и уменьшает стабильность коллоидных частиц.
Однако данная теория не учитывает адсорбцию введенных ионов и их влияние на коллоидные частицы.
Обе теории, как Мюллера, так и другая, верны и применимы при коагуляции, но на разных стадиях процесса. Однако они не могут быть использованы для объяснения других типов коагуляции из-за их ограничений.
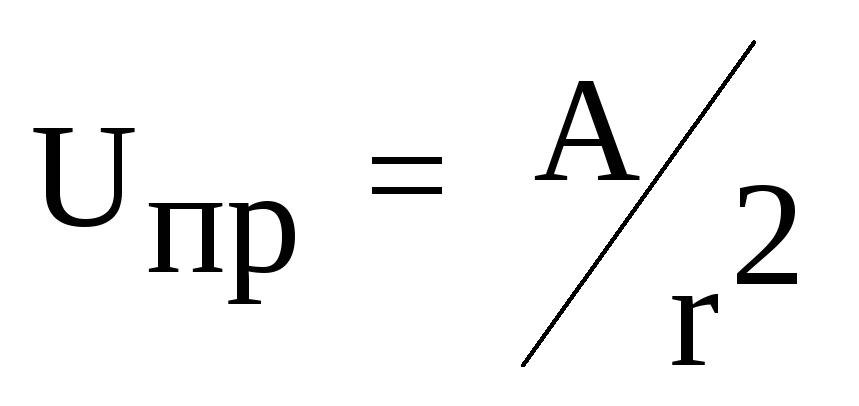
Дерягин, Ландау, Фервей и Овербек в 1941 году создали теорию взаимодействия дисперсных систем, которая носит название ДЛФО в соответствии с первыми буквами фамилий авторов. Она учитывает потенциальную энергию частиц и равновесие электростатических сил, действующих между ними. При приближении частиц возникают электростатические силы притяжения и отталкивания, которые определяют состояние системы.
Если силы отталкивания преобладают, то система остается устойчивой. В случае, когда энергия притяжения становится сильнее, то происходит коагуляция. Энергия притяжения обусловлена силами Ван-дер-Ваальса и обратно пропорциональна квадрату расстояния между частицами. Данные силы действуют только на очень малых расстояниях (1 . 10 − 10 – 1 . 10 − 11 м, т.е. 1 /10 части размера коллоидных частиц).
Коагуляция возникает лишь в том случае, если частицы находятся на необходимом расстоянии. Такое сближение происходит за счет теплового движения частиц. Поэтому, чтобы облегчить процесс коагуляции, необходимо увеличить скорость движения частиц и количество столкновений, что можно достичь при помощи соответствующих воздействий (это подробно описано в разделе "факторы, вызывающие коагуляцию").
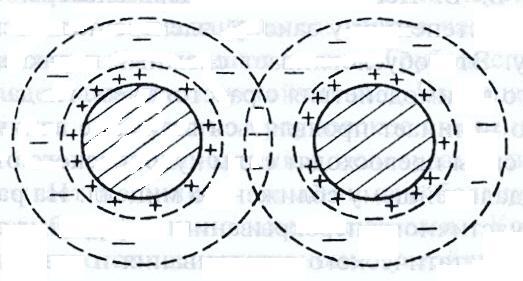
Изображено на Рис.1: пересечение ионных атмосфер коллоидных частиц.
При приближении частиц, возрастают силы электростатического отталкивания, однако сольватная оболочка препятствует соприкосновению частиц. По общему правилу, электростатические силы проявляются при формировании диффузных слоев (ионных сфер) одноименно заряженных частиц. Энергия отталкивания уменьшается при увеличении расстояния между частицами.
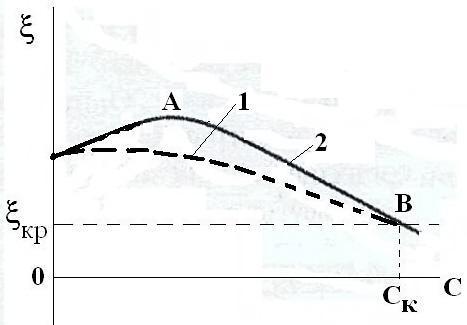
Фигура 2: График потенциальной кривой коагуляции
Для определения состояния системы производится вычисление общей энергии, что позволяет построить график потенциальной кривой коагуляции. В ней имеется несколько зон: в области небольших расстояний присутствует глубокий первичный минимум (потенциальная яма 1), в области больших расстояний — менее глубокий вторичный минимум (потенциальная яма 2). Это указывает на значительный преобладающий потенциал притяжения, следовательно, Uпр >> Uотт.
Предельно стабильная система характеризуется максимумом в зоне средних расстояний. Если он расположен выше горизонтальной оси, то существуют отталкивающие силы между частицами, обеспечивая агрегативную устойчивость системы. При этом Uотт >> Uпр. Увеличение высоты максимума усиливает устойчивость системы.
Для того, чтобы началась коагуляция, необходимо, чтобы заряд частиц был предварительно нейтрализован до определенного значения, а также чтобы была разрушена сольватная оболочка. Для этого вводится электролит или удаляется стабилизирующий электролит. Есть минимальное значение заряда частиц, при котором начинается коагуляция, это называется критическим z-потенциалом (примерно 0,03 В). Если дзета-потенциал достигает критического значения, то кинетическая энергия движения частиц будет достаточной для преодоления остаточных электростатических сил отталкивания (Uпр ~ Uотт), что приведет к объединению мелких частиц в крупные агрегаты.
Существуют два механизма быстрой коагуляции электролитами в соответствии с теорией ДЛФО – концентрационная коагуляция и нейтрализационная (адсорбционная) коагуляция.
В ходе концентрационной коагуляции при добавлении индифферентных ионов не происходит изменения -потенциала. Сама коагуляция происходит в результате сжатия диффузного слоя, вызванного вытеснением противоионов из раствора в адсорбционный слой или в силу увеличения ионной силы.
В случае адсорбционной коагуляции наблюдается уменьшение -потенциала. При этом виде коагуляции электролиты, обладающие зарядом, приводят к изменению заряда на поверхности частиц. Внедрившись в адсорбционный слой, они уравновешивают потенциалопределяющие ионы и, таким образом, уменьшают -потенциал.
Если поверхностные центры микрокристаллов свободны, то происходит достройка кристаллической решетки. Например, если добавить к золю KI, произойдет коагуляция за счет адсорбции ионов иода. Вначале, потенциалы Φ и Ψ увеличиваются, пока центры полностью не будут насыщены адсорбцией. Дальнейшее увеличение концентрации KI приводит к сокращению потенциала Ψ за счет сжатия диффузного слоя и вытеснения ионов калия в адсорбционный слой. Выходит, когда концентрация достигнет определенного уровня, золь начнет коагулировать.
Если на поверхности отсутствуют свободные центры, то происходит сжатие диффузного слоя, но не наблюдается адсорбции и -потенциал не увеличивается.
При добавлении AgNO3 реагенты становятся неиндифферентными, агентами, которые не равнодушны к процессу, — это ионы серебра Ag+. Поскольку иодид-ионы являются потенциалопределяющими ионами, добавление ионов серебра приводит к образованию труднорастворимого соединения AgI. В результате этого число потенциалопределяющих ионов постепенно уменьшается, что приводит к уменьшению - и -потенциалов. Когда -потенциал достигает критического значения, золь коагулирует по адсорбционному механизму. Добавление AgNO3 приводит к перезарядке гранулы за счет избирательной адсорбции ионов серебра, что увеличивает положительный заряд гранулы и формируется новый ДЭС: 3 ─ >х NO3 ─. При дальнейшем добавлении AgNO3 золь коагулирует по концентрационному механизму под действием нитрат-ионов.
Существует заблуждение, что ион коагулятор можно определить по цвету или запаху. Однако, на самом деле для определения иона коагулятора необходимо использовать специальные аналитические методы.
Другое распространенное заблуждение заключается в том, что ион коагулятор можно определить путем визуального осмотра вещества. Это неверно, так как ионы коагулятора не видны невооруженным глазом и требуют специальных методов анализа.
Некоторые также считают, что можно определить ион коагулятора по его вкусу. Однако, это опасное заблуждение, так как некоторые ионы могут быть ядовитыми и недопустимо проводить такие эксперименты без соответствующего оборудования и знаний.
Поэтому для определения иона коагулятора необходимо провести специальные химические анализы с использованием соответствующих реагентов и оборудования. Не следует полагаться на собственные чувства или интуицию при попытке определить ион коагулятора, это может привести к непредсказуемым и опасным последствиям.
Задание 1. Определение порога коагуляции и вычисление коагулирующей силы при коагуляции гидрофобных коллоидов
Процесс коагуляции гидрофобных коллоидов возможен с помощью растворов КС1, K2SO4, СаС12, где все растворы имеют концентрацию 1 М.
Для изучения коагулирующего действия указанных растворов требуется определить пороги коагуляции коллоидов с помощью этих электролитов. Уменьшение порога коагуляции служит показанием увеличения коагулирующей силы иона, который вызывает коагуляцию данного коллоида в соответствии с правилом значимости и валентности.
Для проведения эксперимента необходимо взять пробирки, укрепив их на штативе, за исключением двух. В каждую пробирку добавляют по 1 мл испытуемого золя в соответствии с заданием преподавателя. Для подготовки контрольного раствора добавляют 1 мл дистиллированной воды в первую пробирку с испытуемым золем.
Затем, из колбы с раствором КС1 берут объем 1 мл с помощью пипетки и добавляют его в следующую пробирку с гидрозолем. Сравнив содержимое пробирки с контрольным раствором, можно установить, что хлористый калий данной концентрации приводит к коагуляции коллоида. Наличие коагуляции в пробирке отмечается в таблице 23 символом «+». Далее, можно разбавить раствор КС1 и продолжить определение порога коагуляции гидрофобных золей.
Результаты измерений порога коагуляции гидрофобных золей заносятся в таблицу:
| № п/п | концентрация электролита С, ммоль/л | номер испытуемого золя |
| КС1 | K2SO4 | СаС12 |
| и так далее |
Необходимое оборудование:
— пробирки
— пипетки
— дистиллированная вода
— 1 М КС1
— воздушный насос
— золь
Шаги:
1) Возьмите две пробирки, помойте их и опустите каждую по пипетке на 1 мл.
2) Налейте произвольное количество дистиллированной воды в одну из пробирок, она потребуется для разбавления электролита.
3) Во вторую пробирку налейте 1 мл 1 М КС1 и добавьте 1 мл дистиллированной воды из первой пробирки.
4) Размешайте содержимое пробирки 2 продуванием воздуха через пипетку и отберите 1 мл раствора КС1.
5) Перенесите отобранный раствор в пробирку с золем. При этом не опускайте пипетку в золь, а сливайте электролит по стенке пробирки.
Необходимо аккуратно перемешать содержимое пробирки и проверить, помутнел ли раствор (сравнить с контрольным раствором). Если наблюдается коагуляция, то ее необходимо отметить знаком «+» в специальной таблице. В случае ее отсутствия следует ставить знак «-». Далее необходимо провести разведение электролита аналогично.
Добавляя его маленькими порциями (по 1 мл) к следующим пробиркам с золем, необходимо найти ту концентрацию, при которой коагуляция перестанет наблюдаться. Полученные значения концентраций разведенных растворов электролитов следует записывать в специальную таблицу (в графу С) в виде дроби соответствующей степени. Например: 1), 2), 3) и так далее.
Как упоминалось ранее, порогом коагуляции для каждого электролита считается минимальная концентрация, при которой наблюдается коагуляция золя. Эту величину определяют для каждого электролита и заносят в специальную таблицу №24 (порог коагуляции для КСl, СаС12 и K2SO4 рассчитывается одинаково). По значению порогов коагуляции можно установить ионы-коагуляторы. Затем, чтобы определить коагулирующую силу иона-коагулятора, нужно условно принять коагулирующую силу одновалентного иона за 1. Коагулирующую силу двухвалентного иона (S) можно вычислить по формуле: S = .
Например, если С1 = , а С2 = , то S = =2 5 =32. После выполнения расчетов коагулирующей силы, можно определить результаты коагуляции испытуемого золя.
| Электролиты | Испытуемый золь | |
| Ионы-коагуляторы | Порог коагуляции | Коагулирующая сила |
| КС1 | ||
| СаС12 | ||
| K2SO4 |
Полученные результаты свидетельствуют о том, что коагулирующая сила ионов двухвалентных элементов значительно превосходит коагулирующую силу иих одновалентных коллег. В данном эксперименте разница составила 32 раза.
Базируясь на этой информации, можно определить знак заряда коллоидных частиц исследуемого золя и сделать вывод.
Вторая часть эксперимента касается коагуляции гидрофильных коллоидов действием дегидратирующих веществ, а также исследование обратимости и необратимости коллоидов.
Возьмите две пробирки объемом по 2 мл каждая и наполните их раствором сернистой сурьмы. В первую пробирку добавьте также 2 мл дистиллированной воды — этот раствор использовать как контрольный. Во вторую пробирку из бюретки с добавлением капель насыщенного раствора сульфата аммония, доведите количество раствора до появления хлопьев. Сравните полученный результат с контрольным раствором, отметьте количество мл раствора сульфата аммония, которое вызвало коагуляцию и запишите его в таблицу под номером 25. Затем в эту же пробирку добавьте 5 мл дистиллированной воды и убедитесь в необратимости коагуляции гидрофобного золя.
Перейдите к трём новым пробиркам объемом по 2 мл каждая и налейте в них 0,5% раствора желатина. В первую пробирку добавьте 5 мл дистиллированной воды — это будет контрольный раствор.
Вторую пробирку наполняют из бюретки этиловым спиртом, не прекращая добавлять, пока не появятся маленькие хлопья или муть (по сравнению с контрольной пробиркой). Результат записывают в таблицу №25, указав количество добаленного реагента. Затем к этой же пробирке добавляют из бюретки дистиллированную воду, пока хлопья не исчезнут (по сравнению с контрольной пробиркой). Количество воды и результат также записывают в таблицу.
В третью пробирку добавляют из бюретки насыщенный раствор сульфата аммония с гидрозолем желатина, не останавливаясь, пока не появятся хлопья. Количество добавленного реагента отмечается в тетради. Затем к содержимому пробирки добавляют по 0,5 мл дистиллированной воды, пока хлопья не исчезнут. Количество воды также отмечают.
После проведенных опытов делают выводы об обратимости и коагуляции гидрофильных и гидрофобных золей.
Определение обратимости коллоидов после их коагуляции в зависимости от гидрофильных и гидрофобных золей
| название коллоида | используемый реагент | использованное количество реагента (мл) при коагуляции | использованное количество воды (мл) при пептид-зации | вывод об обратимости коллоидов |
| гидрофильный коллоид в виде 0,5% раствора желатина | этанол, сульфат аммония ((NH4)2SO4) | |||
| гидрофобный коллоид в виде золя сернистой сурьмы | сульфат аммония ((NH4)2SO4) |
Ионы
Согласно исследованиям, электролиты оказывают влияние на состояние гидрофобных золей, при этом коагуляционное действие зависит от заряда ионов. Резкое улучшение скорости коагуляции наблюдается при превышении критической концентрации электролита, таким образом определяется порог коагуляции. Для расчета этой величины необходимо знать концентрацию коагулятора (электролита) — С, объем добавляемого электролита — V, а также общий объем золя — V30 (обычно это 10 мг). Коагулирующая способность электролита равна противоположной величине порога коагуляции, и чем ниже порог, тем выше способность электролита к коагуляции.
Но не все электролиты участвуют в этом процессе, и главную роль играет только тот ион, который имеет такой же заряд, как ион-противник (а заряд иона, который вызывает коагуляцию, всегда противоположен заряду коллоидной частицы). Этот ион называется ионом-коагулянтом.
Чем выше заряд этого иона, тем выше его коагуляционная способность, согласно правилу Шульце-Гарди. Теория Дерягина-Ландау описывает связь между ионом-коагулянтом и порогом коагуляции. Правила электролитной коагуляции включают правило значимости, которое определяет соотношение порогов коагуляции для одно-, двух- и трехзарядных ионов. Y1 : Y2 : Y3 = 729 :11 : 1. Это означает, что трехзарядный ион способен коагулировать на 729 раз быстрее, чем однозарядный.
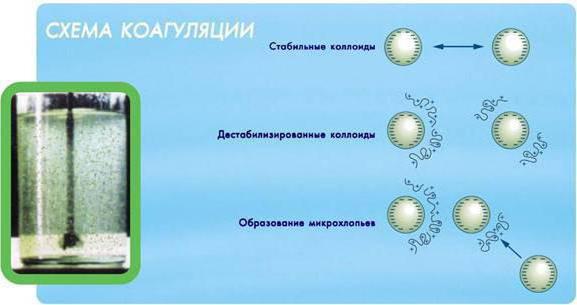
Изменения
Со временем и развитием коллоидной химии в науке были выявлены некоторые отклонения от правила значимости. Кроме заряда, порог коагуляции также зависит от радиуса иона-коагулянта, его способности к гидратации и абсорбции, а также от природы иона, который сопутствует коагулянту. Многозарядность иона приводит к эффекту перезарядки частиц, поэтому изменение знака заряда приводит к изменению потенциала коллоидной частицы.
Добавляемые ионы взаимодействуют с противоположно заряженными ионами, заменяя их в адсорбционном и диффузионном слоях. Когда добавленный ион имеет множественный заряд и является небольшим, как, к примеру, Al 3+, Th 4+ и прочие, происходит сверхэквивалентная адсорбция. В этом случае такой ион замещает указанное количество значительно меньших ионов на поверхности частиц, которые не соответствуют ему по заряду. А именно, вместо одного или нескольких ионов К + появляется ион Th 4+. Именно эта ситуация демонстрирует изменение зарядового потенциала.

Изучение процесса электролитной коагуляции
Цель нашего исследования — раскрыть методы коагуляции и изучить влияние концентрации и характера электролита на данный процесс.
Теоретические аспекты
Коллоидные системы имеют термодинамическую нестабильность. Огромная поверхность диспергированных частиц порождает избыток поверхностной энергии, которая, согласно второму принципу термодинамики, отдает предпочтение минимальному значению. Именно поэтому коллоидные частицы стремятся к склеиванию, т.е. происходит коагуляция. Электролиты и неэлектролиты, изменение температуры, механическое воздействие, свет, электрический ток и другие факторы могут вызвать коагуляцию коллоидных растворов. В частности, электролиты играют ключевую роль в этом процессе.
Заключения, сделанные на основе экспериментов с коагуляцией электролитами, стали основой для выведения правил коагуляции Шульце-Гарди, которые включают в себя следующие пункты:
1) Любой электролит может вызвать коагуляцию при определенной концентрации. Порог коагуляции, то есть минимальная концентрация электролита, при которой наблюдается явная коагуляция, составляет g (моль/л) и сопровождается появлением осадка, помутнения раствора и изменением его цвета;
2) В качестве иона-коагулятора выступает ион, заряд которого противоположен заряду коллоидной частицы;
3) Порог коагуляции уменьшается с увеличением заряда иона-коагулятора.

(1)
Коэффициент "а" характеризует систему, а "z" — заряд иона коагулятора.
Способность иона к гидратации влияет на порог коагуляции для ионов с одинаковым зарядом. При уменьшении этой способности порог коагуляции понижается.
А коагулирующая способность повышается.

Увеличение способности к гидратации
4) Часто начало коагуляции сопровождается снижением  – потенциала до критического уровня. В общем значении,
– потенциала до критического уровня. В общем значении,  – потенциал отражает стабильность системы перед коагуляцией. Большой
– потенциал отражает стабильность системы перед коагуляцией. Большой  – потенциал указывает на большие размеры двойного ионного слоя.
– потенциал указывает на большие размеры двойного ионного слоя.
Добавление электролита приводит к сокращению двойного ионного слоя, и частицы могут приближаться друг к другу больше.
Вышеприведенные соображения могут быть полностью применимы только в отношении лиофобных золей (или, в определенных случаях, гидрофобных), то есть золи, которые не связывают молекулы среды и не смачиваются растворителем. В отличие от этого, лиофильные золи хорошо смачиваются средой и имеют прочную оболочку из молекул среды, что является важным фактором устойчивости. Для коагуляции лиофильного (гидрофильного) золя необходимо предварительно разрушить оболочку из молекул среды вокруг его частиц, что затем сделает возможным процесс электролитной коагуляции. Таким образом, лиофильные золи в целом более устойчивы, чем лиофобные золи, и требуют более сложного способа коагуляции.
Что касается практической части, приведенной ниже, можно провести коагуляцию золя гидроксида железа (III) с использованием электролитов.
Нагрейте 100 мл дистиллированной воды до кипения, а затем добавьте 5-10 мл 2%-го раствора FeCl3 по каплям в кипящую воду. Таким образом, вы получите коллоидный раствор гидроксида железа (III) красно-коричневого цвета. Разлейте полученный золь Fe(OH)3 в три конические колбы пипеткой по 20 мл. Затем в каждую из них по каплям добавляйте растворы электролитов, приведенных в таблице 10.1, до тех пор, пока не появятся первые признаки коагуляции.
Далее, перенесите полученные результаты на график. Откладывайте на оси абсцисс (x) значения заряда ионов коагуляторов, а на оси ординат (y) — логарифм числа миллилитров 0,001 н. растворов. Из хода кривой можно определить, какой из электролитов наиболее эффективен в качестве коагулятора.
В таблице 10.1 представлены результаты коагуляции Fe(OH)3 различными электролитами.
| Номер колбы | Электролит | Концентрация раствора | Объем электролита (мл), необходимый для коагуляции | Объем электролита (мл), необходимый для коагуляции при концентрации 0,001 н. |
| 1. | KCl | 2н. | ||
| 2. | K2S04 | 0,01 н. | ||
| 3. | K3[Fe(CN)6] | 0,001 н. |
В данном случае коллоидные частицы будут иметь положительный заряд, а мицелла будет иметь следующую структуру:

В процессе кипячения раствора происходят следующие реакции:
FeOCl ⇆ FeO + + Cl — , а ионы FeO + адсорбируются на поверхности частиц гидроксида железа (III). Это заряжает коллоидные частицы положительно, поэтому для золя Fe(OH)3 отрицательными ионами-коагуляторами будут анионы.
2. Взаимная коагуляция двух коллоидов
Любая реакция, приводящая к образованию нерастворимого вещества, может в определенных условиях привести к образованию коллоидного раствора.
Реакция образования нерастворимого AgI можно записать следующим образом:
Ag + + I — ⇆ AgI (↓)
Если в растворе присутствует избыток AgNO3, то образовывается коллоидная частица с положительным зарядом, так как ион Ag + адсорбируется.

Если в избытке добавить калий йодид, то возникнет коллоидная частица, обладающая отрицательным зарядом:

При соединении двух коллоидов с противоположными зарядами возможно коагуляция при условии, что суммарное количество зарядов одного коллоида выравнивает суммарное количество противоположных зарядов другого коллоида. Результатом может быть оседание AgI без заряда.
Для получения отрицательно заряженного золя следует аккуратно смешать 40 мл 0,01 н. раствора KI и плавно добавить 32 мл 0,01 н. раствора AgNO3 из бюретки в коническую колбу. А для получения положительно заряженного золя, необходимо налить 40 мл 0,01 н. раствора AgNO3 в другую коническую колбу и медленно добавить при перемешивании 32 мл 0,01 н. раствора KI из бюретки.
Чтобы провести опыт, необходимо взять 11 чистых пробирок и налить в них коллоидный раствор AgI с отрицательно заряженными частицами следующим образом: в первую пробирку – 1 мл, во вторую – 2 мл и т.д., согласно таблице 10.2. В десятую пробирку наливается 10 мл раствора, а одиннадцатая остается пустой. Далее необходимо добавить в каждую пробирку коллоидный раствор AgI, частицы которого заряжены положительно, чтобы общий объем раствора в каждой пробирке был равен 10 мл, как показано в таблице 10.2. Таким образом, будет выполнена взаимная коагуляция двух коллоидов.
Таблица 10.2 — Результаты взаимной коагуляции двух коллоидов
| Номер пробирки | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 |
| Объем (мл) золя [mAgJ] — | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 0 |
| Объем (мл) золя [mAgJ] + | 9 | 8 | 7 | 6 | 5 | 4 | 3 | 2 | 1 | 0 | 10 |
Таким образом, в 10-й и 11-й пробирках происходит процесс коагуляции, в то время как в остальных пробирках отсутствует. По результатам таблицы 10.2 делается вывод об эффективности опыта.
Контрольные пробирки имеют номера 10 и 11.
1. Коагуляция – это процесс слипания молекул, вызываемый различными факторами, например, изменением температуры или добавлением определенных химических веществ.
2. Как электролит природы влияет на процесс коагуляции и что такое порог коагуляции?
3. В чем разница между тем, как происходит коагуляция лиофобных и лиофильных золей?
4. Как влияет заряд иона-коагулятора на порог коагуляции?
5. Какой тип коллоидного раствора может вызвать коагуляцию исследуемого раствора: тот, у которого частицы имеют одинаковый заряд, или тот, у которого частицы имеют противоположный заряд?
6. Какой электролит является наиболее эффективным коагулирующим для золи, полученной в результате реакции 2 H3AsO3 + 3 H2S (изб.) = As2S3 + 6 H2O?
7. Для коагуляции 70 мл золи йодида необходимо 0,45 мл раствора нитрата бария с концентрацией 0,05 моль/л. Каков порог коагуляции?
8. Какие процессы связанны с коагуляцией и какие примеры можно привести?
Лабораторная работа №11
Дата добавления: 2018-04-05; количество просмотров: 917; Мы поможем в написании вашего исследования!
Теория электролитной коагуляции и ее ключевое правило: Шульце-Гарди
Электролитная коагуляция дисперсных систем может быть вызвана различными факторами, такими как: механическое воздействие (например, ультразвук), сильное разбавление, концентрирование, замораживание, нагревание и введение электролитов. Однако, для коагуляции необходимо минимальное количество электролита-коагулятора, которое называется порогом коагуляции данной системы. Обычно этого достаточно небольшое количество. Иногда используют обратную величину, которую называют коагулярующей способностью.
В зависимости от природы электролитов, существуют два возможных механизма их действия. Принцип Шульце-Гарди утверждает, что эффективность действия электролита на коагуляцию зависит от его валентности и молекулярного веса. Следовательно, электролиты с высокой валентностью и молекулярным весом будут эффективнее на коагуляцию, чем электролиты с низкой валентностью и молекулярным весом.
Концентрационная коагуляция вызывается индифферентными электролитами, которые увеличивают ионную силу и уменьшают толщину диффузного слоя противоионов. Это приводит к переходу противоионов из диффузного слоя в плотный, что уменьшает ж-потенциал.
Нейтрализационная (адсорбционная) коагуляция вызывается неиндифферентными электролитами, когда заряд частиц невелик. Происходит непосредственная адсорбция коагулирующих ионов на поверхности частиц. Может быть специфическая адсорбция по правилу Панета-Фаянса, когда ионы достраивают кристаллическую структуру твердой фазы частиц, или замещение в плотном (адсорбционном) слое одних противоионов другими с более высокой плотностью заряда.
В обоих случаях происходит нейтрализация и уменьшение заряда частиц.
Возникновение коагуляции происходит при использовании любых электролитов. В ряду органических ионов, возрастает коагулирующее действие с ростом адсорбционной способности. В ряду неорганических ионов с одинаковым зарядом, коагулирующая активность увеличивается с уменьшением гидратации.
Для коагулирующего действия электролитов используется правило Шульце-Гарди. Коагулирующим действием обладает ион с противоположным зарядом частицы. Сила коагулирующего действия увеличивается с ростом заряда иона.
Определяющим для коагуляции является понятие порога коагуляции. Правило записывается с использованием следующих значений порога коагуляции: г1: г2 : г3 = 500:25:1 для 1, 2 и 3-х зарядных ионов.
Зависимость порога коагуляции от заряда была установлена при помощи теории ДЛФО.

Заряд иона коагулятора z обратно пропорционален порогу коагуляции в шестой степени. Данный коэффициент имеет соотношение г1 : г2 : г3 = 73~0:11:1.
Использование концепции порога коагуляции позволяет оценить коллоидную защиту белков и иных ВМС. Увеличение концентрации электролитов уменьшает устойчивость ДС, но добавление белка повышает ее устойчивость и такую защиту можно характеризовать числом -min концентрацией белка, необходимой для предотвращения коагуляции частиц при наличии пороговой концентрации электролита.
Получение, свойства и применение пен
Плёнками ДС разделены газом заполненные пены, состоящие из ячеек, характерной фигурой которых является пентагональный додекаэдр, имеющий 30 рёбер и 20 вершин. В реальных пенах количество плёнок, окружающих ячейку, близко к 14, что отличается от идеализированной фигуры.
Каналы Гиббса-Плато являются ребрами пенной ячейки и заполнены дисперсионной средой. Каждый канал может сходимся только на три пленки, образующие угол в 120^. Форма поверхности канала имеет сложную вогнутую форму, описываемую условием постоянства сумм двух главных кривизн. Капиллярное давление под вогнутой поверхностью приводит к пониженному давлению в канале Гиббса-Плато.
Основная часть дисперсной системы находится в каналах пены с кратностью от 100 до 1000, которая зависит от толщины и дисперсности пленок. Небольшое количество системы находится в пленках. В ячейках с очень низкой кратностью (около трех) содержание жидкости наибольшее.
В реальных пенах у ячеек различная форма из-за многокомпонентности. Однако, все же, правила Плато работают во всех случаях, то есть три пленки формируют канал, а четыре канала — вершину. Дисперсность пены характеризуется ее удельной поверхностью. Больше всего употребляются некоторые средние значения геометрических параметров ячейки, к примеру, среднее число ячеек в единицу объема или средний эквивалентный радиус.
Использование пен широко распространено в различных областях современной техники: при тушении пожаров, во флотации, в производстве хлебопекарных и кондитерских изделий (например, хлеб с отвержденной пеной), теплоизоляционных материалов (пенобетон, пенопласты, микропористые резины) и т.д. Пену получают путем диспергирования воздуха (иногда другого газа) в жидкости, содержащей какой-либо пенообразователь. Иногда вводятся добавки стабилизаторов пены, также являющихся пенообразователями, которые усиливают действие пенообразователя.
Разбрызгивание газа возможно, используя метод барботажных пен через слой жидкости или с помощью мешалок в жидкости. Существуют различные типы пеногенераторов, часто с изображением на сетке. Регулируя расход воздуха и пенообразующего раствора, можно создавать пену нужной плотности. Для достижения необходимой дисперсности пенного потока, устанавливают ряд сеток, на которых происходит распыление ячеек пены. Такие пеногенераторы могут эффективно и быстро использоваться при тушении пожаров, особенно горевших топлив и других органических жидкостей.
Пены, в которых происходит отверждение ДС (например, хлеб, пеноматериалы), образуются путем конденсации газа, чаще всего С02, в результате химической реакции или биохимического процесса.
Разрушение пены происходит за счет изменения параметров, которые связаны с ее структурой во времени. Этот процесс связан с утоньшением и прорывом пленок, перегонкой газа из мелких ячеек в более крупные, а также с синерезисом — вытеканием дисперсной системы из каналов Гиббса-Плато под воздействием силы тяжести.
Утоньшение пленок может привести к их разрыву или созданию метастабильного равновесного состояния, когда расклинивающее давление в пленке равно капиллярному давлению, которое определяется кривизной поверхности мениска, окружающего пленку. Эту величину можно изменить, отсасывая жидкость из канала Гиббса-Плато.
Изменение пены во времени может быть вызвано переносом газа через пленки или их разрывом. Дисперсность пены и ее изменения во времени измеряются подсчетом числа ячеек, контактирующих со стенкой сосуда, где расположена пена, с помощью микрофотографий.
Изотермический перенос газа значительно влияет на малые ячейки с высоким давлением воздуха, перенося их в крупные ячейки, где давление воздуха ниже. Это особенно важно для высокодисперсных полидисперсных пен на начальных стадиях разрушения. Толщина пленок пен остается неизменной в состоянии, близком к метастабильному равновесию, и кинетика роста ячеек пен происходит при изотермическом переносе газа. Разрыв пленок в пенах является случайным, и вероятность прорыва пленок и объединения соседних ячеек пропорциональна числу пленок в данный момент времени.
Изменение структуры пены со временем связано с вытеканием дисперсионной среды по системе каналов Гиббса-Плато за счет силы тяжести (синерезис). Для достижения гидростатического равновесия противодействует капиллярное давление в каналах Гиббса-Плато.
В высокократных и высокодисперсных пенах начальное значение кратности может превышать допустимую величину. Уменьшение дисперсности пены приводит к уменьшению количества жидкости, которую можно содержать в пене, и начинается вытекание дисперсионной среды, что приводит к увеличению кратности пены.
Участие времени в изменении числа пузырьков полностью зависит от снижения дисперсности пены: когда пленка из пузырька лопается, количество зазоров в единице объема пены уменьшается, а размер каналов остается неизменным. В пенах с маленьким количеством пузырьков происходит обратное: сначала присутствует быстрое распространение дисперсной среды и множество пузырьков увеличивается до того времени, пока не достигнет сосотояния, близкого к гидростатическому равновесию. Позже изменение количества пузырьков происходит так же, как и в пенах с большим количеством пузырьков. Простой способ определения числа пузырьков в пене — измерение ее электрической проводимости (число пузырьков обратно пропорционально ее электрической проводимости).
В пожарной случае особое значение имеют высокоустойчивые пены, содержащие стабилизированные ПАВ третьей и четвертой групп. Они широко применяются при тушении пожаров, возникших на нефтепродуктах и жидких топливах. При этом важными параметрами пен являются скорость распространения по поверхности горящей жидкости и их способность изолировать ее от окружающей среды, задерживая выход паров. При изготовлении таких пен используют сложные составы, включающие помимо основного компонента, другие ПАВ, устойчивые к разрушению. Однако, новые возможности открываются применением фторзамещенных соединений.
На многих производствах важным моментом является уничтожение или предотвращение образования пены. К примеру, в микробиологическом производстве может возникнуть излишняя пена, мешающая нормальному процессу. Пена может образовываться при химических процессах, где происходит выделение газов или при контакте газов с жидкостью. Слишком большое пенообразование может затруднять работу стиральных машин, из-за чего стиральные порошки для машин содержат меньшее количество алкилсульфатов, а больше неионогенных ПАВ. В сравнении с алкилсульфатами, неионогенные ПАВ являются менее активными пенообразователями, особенно при повышенных температурах.




