Введение регистрационных удостоверений на медицинское оборудование помогает обеспечить безопасность пациентов и качество предоставляемых услуг. Это позволяет контролировать качество и соответствие медицинского оборудования стандартам и требованиям.
Далее в статье мы рассмотрим, какие именно медицинские устройства подлежат обязательной регистрации, как процесс регистрации проходит, а также какие организации отвечают за выдачу удостоверений. Узнаете, какие могут быть последствия при использовании нерегистрированного оборудования, и какие меры предпринимаются для борьбы с нелегальным медицинским оборудованием.
- В 2018 году в России было принято постановление о введении регистрационных удостоверений на медицинское оборудование.
- Данное решение было принято с целью повышения качества и безопасности медицинского оборудования на рынке.
- Регистрационные удостоверения позволяют контролировать процесс производства, хранения и эксплуатации медицинского оборудования.
- Только оборудование, прошедшее процедуру регистрации, может быть использовано в медицинских учреждениях.
- Это позволяет защитить пациентов от некачественного и опасного оборудования, а также повысить ответственность производителей.
Как получить регистрационное удостоверение на медицинские изделия
Регистрационное удостоверение на медицинское изделие является официальным документом, подтверждающим его соответствие стандартам качества и безопасности для здоровья, а также разрешает его продажу на территории России.
Федеральным законом от 21.11.2011 № 323-ФЗ установлено обязательное требование государственной регистрации всех медицинских изделий на территории России. Регистрационные удостоверения на медицинские изделия выдаются Росздравнадзором, независимо от класса изделия. Исключение составляет только индивидуальное оборудование, которое изготавливается специально для каждого пациента и предназначено исключительно для его личного пользования.
Если Вы хотите зарегистрировать свое медицинское изделие, то необходимо обратиться в Росздравнадзор и подать соответствующую заявку в соответствии с требованиями закона.
Если товар предназначен для здоровья и его планируют продавать, то необходимо его зарегистрировать. Если регистрации нет, то продажа товара запрещена. Специальное удостоверение выдается на оборудование после прохождения государственной регистрации, которая подтверждает выполнение необходимых процедур. Регистрационное удостоверение для медицинского изделия неограниченного действия.
Назначение регистрации
Один из способов обеспечения качества товаров для здоровья и защиты людей от потенциальной опасности заключается в регистрации оборудования. В процессе регистрации проводится оценка как документов, предоставленных заявителем, так и самого товара и его свойств, что дает возможность подтвердить безопасность и пригодность к использованию медицинских изделий.
Государственные органы, которые покупают товары для здоровья, должны потребовать у потенциальных поставщиков документы о регистрации. Эти документы помогают установить, зарегистрировано ли медицинское изделие или нет, а также указать его производителя, место производства и класс риска. Чтобы гарантировать качество поставляемых товаров, заказчики должны затребовать копии соответствующих документов у участников торгов, а не только узнавать их реквизиты из заявок на участие. Тем не менее, в настоящее время существует база зарегистрированных медицинских изделий и препаратов, где можно легко проверить оригинальность документов по их реквизитам.
В некоторых областях комиссии УФАС считают, что если участник тендера указывает реквизиты документов, подтверждающих его заявку, это достаточно и ее нужно рассмотреть. Однако, судебные прецеденты показывают, что предоставление копий документов является обязательным, если такое требование прописано в документации заказчика. Если в заявке отсутствует свидетельство о регистрации, это является достаточным основанием для отклонения. Такую позицию поддерживает кассационное Постановление АС Московского от 13.06.2019 по делу № А40-185526/2018.
Введение регистрационных удостоверений на медицинское оборудование является важным шагом для обеспечения безопасности и качества медицинских изделий. Регистрация позволяет контролировать процесс производства, обеспечивать соответствие стандартам качества и безопасности, а также отслеживать медицинское оборудование на всем его жизненном цикле.
Этот механизм регистрации позволяет предотвратить появление подделок, контрафактного оборудования и медицинских изделий низкого качества на рынке. Благодаря регистрационным удостоверениям врачи и пациенты могут быть уверены в том, что используемое оборудование прошло все необходимые проверки и соответствует высоким стандартам безопасности.
Кроме того, регистрация медицинского оборудования способствует улучшению мониторинга и контроля за его использованием. Такой подход позволяет своевременно выявлять возможные проблемы с оборудованием, предотвращать несчастные случаи и обеспечивать безопасность как персоналу медицинских учреждений, так и пациентам.
Уровни риска
В Постановлении правительства РФ №1416 установлены разные процедуры госрегистрации для разных типов товаров в зависимости от класса потенциального риска их использования, то есть от возможного вреда, который они могут причинить здоровью пациента, даже если использованы по назначению производителем. Приказ Минтруда от 6 июня 2012 года №4н определяет методику определения степени риска и делит все медицинские изделия на 4 класса:
- 1 – с низкой степенью риска;
- – со средней степенью;
- – с повышенной степенью;
- 3 – с высокой степенью.
Процедуры госрегистрации
Правила постановки на учет для товаров, относящихся к классам 2а, 2б и 3, имеют базовый характер. Сокращенный ориентир алгоритма регистрации действует для продуктов 1 класса риска и товаров в категории in vitro. Согласно постановлению № 1416, для получения регистрационного удостоверения по стандартной процедуре заявитель должен пройти следующие этапы.
Товары 1 класса риска и изделия категории in vitro не нуждаются в проведении клинических испытаний на этапе государственной регистрации и выдачи регистрационного досье. Клинические испытания проводятся на этапе подготовки документации.
Выдача регистрационных удостоверений для медицинского оборудования

Где можно найти регистрационные удостоверения для медицинского оборудования?
Что делать, если нет регламента удостоверения или оно устарело, но оборудование используется?
Существует ли у всех видов медицинского оборудования срок годности или же есть исключения?
На эти вопросы можно получить ответы в данной статье.
Место хранения регистрационных удостоверений не регулируется законодательством и может быть определено руководителем самостоятельно.
Для получения образца договора аренды медицинского оборудования можно скачать/открыть его по ссылке >>
Надо ли закупать медицинское оборудование в соответствии с законом № 44-ФЗ или 223-ФЗ? Об этом также можно узнать, скачав/открыв соответствующий материал по ссылке >>
Организации имеют право использовать медицинские изделия, приобретенные в период действия соответствующих регистрационных удостоверений и сертификатов соответствия, на протяжении сроков службы или годности данного оборудования. Производитель указывает срок службы в технической и эксплуатационной документации (см. письмо Минздрава от 08.09.2015 г. № 2071895/25-3).
Некоторые медицинские изделия, такие как инструменты, приборы и аппараты, относятся к товару длительного пользования и могут стать опасными для жизни, здоровья, имущества или окружающей среды после определенного периода использования. Изготовитель в таких случаях обязан установить срок службы (см. постановление Правительства от 16.06.1997 г. № 720).
Руководители медицинских организаций могут принять участие в бесплатных вебинарах с баллами НМО.
В 2024 году инспекторы обратят внимание на новые аспекты контроля. Например, 16 мая 2024 года руководители организаций должны будут обратить особое внимание на точки риска в своей деятельности. А на 11 июня 2024 года главврачи должны будут знать об изменениях в маркировке лекарств и медицинских изделий, чтобы успешно пройти контроль. А еще, 10 июля 2024 года врачам представятся новые возможности при прохождении аттестации на квалификационную категорию.
Кроме того, производители обязаны устанавливать срок службы долговечных товаров и комплектующих изделий, которые могут стать опасными для жизни, здоровья или окружающей среды. Срок службы идет со дня изготовления товара, а продажа товара после истечения срока годности запрещена. Это основано на законе № 2300-1 "О защите прав потребителей".
Поставщик медицинских изделий разрабатывает соответствующую техническую или эксплуатационную документацию, которая используется для производства, изготовления, хранения, транспортировки, монтажа, наладки, применения, эксплуатации, а также технического обслуживания, ремонта, утилизации или уничтожения медицинского оборудования (согласно статье 38, части 3 Федерального закона от 21.11.2011 №323-ФЗ «Об основах охраны здоровья граждан в Российской Федерации»).
Жизненный цикл оборудования в медицинской организации

За приобретение, установку, прием на баланс, обслуживание, использование и утилизацию медицинской техники отвечает руководитель медицинского учреждения. Как эффективно контролировать каждую из этих стадий, вы найдете в специализированном журнале "Здравоохранение". По интересующим вопросам также доступны таблицы с информацией о временных затратах руководителя на ремонт медицинской техники, а также анализе рисков выхода такого оборудования из строя.
Для установления требований к технической и эксплуатационной документации, относящейся к медицинским изделиям, предусмотренным для использования в медицинских учреждениях, необходимым является уполномоченный федеральный орган исполнительной власти. На данный момент таковых требований не установлено. Следовательно, порядок утилизации медицинской техники определяется на основе соответствующей технической или эксплуатационной документации.
Открыть таблицу
Комиссия по поступлению и выбытию активов осуществляет списание нефинансовых активов в соответствии с актом по форме 0504104 (утвержденным приказом Минфина от 30.03.2015 №52н), за исключением транспортных средств. Однако, при списании изделий медицинской и другой техники, а также узлов и деталей, содержащих драгоценные металлы, следует соблюдать Инструкцию о порядке учета и хранения драгоценных металлов, драгоценных камней, продукции из них и ведения отчетности при их производстве, использовании и обращении (утвержденную приказом Минфина РФ от 29.08.2001 №68н).
Согласно постановлению Главного государственного санитарного врача РФ от 07.07.2011 №91, при утилизации медицинского оборудования, содержащего источники ионизирующего излучения, необходимо соблюдать требования СанПиН 2.6.1.2891-11 «Требования радиационной безопасности при производстве, эксплуатации и выводе из эксплуатации (утилизации) медицинской техники, содержащей источники ионизирующего излучения».
![]()
У вас возникла ситуация, когда инструмент для проведения обследования приобретен, но нет информации о его обработке, утилизации и прочем на русском языке? Не беда! Все необходимые данные указаны на маркировке и в инструкции по применению на русском языке. Кроме того, в законодательстве государств-членов на государственном языке содержатся требования к маркировке и эксплуатационной документации медицинских изделий. Будьте внимательны, символы на медицинском изделии могут быть установлены международными стандартами, но используйте их только если эта информация не повлияет на безопасность использования изделия.
В соответствии с пунктом 11 общих требований безопасности и эффективности медицинских изделий, а также требованиями к их маркировке и эксплуатационной документации, утвержденными решением Совета Евразийской экономической комиссии от 12 февраля 2016 года № 27, поставщик обязан предоставить инструкцию на русском языке.
Эксперты журнала "Здравоохранение" рассказывают о главных ошибках в процессе лицензирования. Вместе с Росздравнадзором и медицинскими юристами были подобраны примеры нарушений, связанных с новым руководством по лицензированию, и составлен чек-лист для внутреннего аудита медицинских организаций. Руководители ведущих клиник поделились мерами профилактики наиболее рискованных нарушений, связанных с лицензионными требованиями.
Как контролировать нарушения в правилах аренды: советы, основанные на новом руководстве Росздравнадзора. В статье вы найдете алгоритм, который поможет вам контролировать аренду помещений — одно из самых рискованных лицензионных требований, отмеченных Росздравнадзором в новом руководстве.
Как предотвратить приостановку работы клиники на 90 дней из-за технических недочетов? В статье вы найдете советы от коллег о том, как контролировать техобслуживание медицинского оборудования и предотвратить нарушения лицензионных требований, которые могут привести к мораторию на работу. Образцы для снижения рисков прилагаются >>
Категории продукции, требующие регистрационное удостоверение
Пересекая российскую границу или выходя на территорию России в первый раз, все медицинские инструменты, оборудование и лекарства должны быть сертифицированы на безопасность и зарегистрированы в Государственном реестре, после чего выдается Регистрационное удостоверение МинЗдрава. Многие изделия медицинского назначения производятся в различных отраслях промышленности, таких как медицина, авиация, оборона, химия, приборостроение, текстиль и металлургия.
В Российской Федерации доля отечественных медицинских изделий на рынке составляет около 35%, а остальные 65% представлены импортными товарами. В большинстве развитых стран применяется контроль качества медицинских изделий. Например, в европейских странах любой медицинский продукт должен быть сертифицирован и иметь маркировку "CE", подтверждающую его соответствие требованиям Европейского Союза. В России же для применения медицинских изделий по назначению обязательно наличие Регистрационного удостоверения Минздрава. Если изделие содержится в списке обязательных для прохождения государственной регистрации, его использование без соответствующих документов незаконно. Список включает следующие категории изделий:
- материалы и инструменты;
- специализированное медицинское оборудование;
- программно-аппаратные решения для диагностики, лечения и управления;
- инные изделия, предназначенные для медицинских целей.
Одним из распространенных заблуждений на тему введения регистрационных удостоверений на медицинское оборудование является то, что это новое требование, которое было внедрено недавно. Однако фактически регистрация медицинского оборудования является стандартной практикой уже многие годы как в России, так и во многих других странах.
Другим распространенным мифом является утверждение о том, что регистрация удостоверений на медицинское оборудование создает дополнительные бюрократические препятствия для производителей и поставщиков. Однако это не так, так как регистрационные удостоверения помогают обеспечить безопасность и качество медицинского оборудования на рынке.
Также часто ошибочно считается, что регистрация удостоверений на медицинское оборудование приводит к увеличению стоимости продукции. На самом деле, регистрационная процедура предназначена для защиты пациентов и потребителей, поэтому она не должна влиять на цену продукции существенно.
Важно понимать, что регистрационные удостоверения на медицинское оборудование необходимы для обеспечения безопасности и эффективности продукции. Это стандартная практика, которая помогает защитить пациентов и потребителей от некачественного или опасного оборудования.
История данного документа
Впервые сертификация медицинских изделий была введена в России в 1992 году. Процедуры подтверждения соответствия таких изделий определены в документе "Правила по сертификации", который был утвержден в ноябре 2001 года на расширенном заседании коллегии Госстандарта РФ. В 2006 году Министерство здравоохранения и социального развития РФ выпустило Административный регламент, который способствует реализации функции, предписанной российским законодательством Росздравнадзору – проведение государственной фиксации аппаратов и приборов медицинского назначения, которые будут использоваться на территории России (Приказ МинЗдрава № 735). Данное требование распространяется как на отечественную медицинскую продукцию, так и на импортируемые поставки. В настоящее время на территории России действуют три различные формы одного и того же разрешительного документа — Регистрационного удостоверения МинЗдрава. Вид документа определяется датой официальной регистрации медицинского изделия:
- До 2014 года было возможно получить Регистрационное удостоверение от МинЗдрава, действительное в течение 10 лет со дня начала действия, указанного в документе.
- С 2005 по 2006 годы выдавалось Регистрационное удостоверение от Росздравнадзора, которое получило свое название после переименования МинЗдрава. Однако, в связи с вступлением в силу Административного регламента министерства, данный формат удостоверений перестал выдаваться. Максимальный срок действия таких удостоверений также составляет 10 лет.
Выдача Регистрационного удостоверения МинЗдрава
- После начала действия Административного регламента, Регистрационное удостоверение МинЗдрава будет выдано в новой форме и в соответствии с новым порядком. Данный документ может быть выдан на неопределенное время, если информация об изделии медицинского назначения и получателе удостоверения остаются неизменными.


С 1 января 2022 года медицинские изделия могут быть зарегистрированы на территории Российской Федерации только через процедуру Евразийского экономического союза. Подтверждением регистрации определенного медицинского устройства является регистрационное удостоверение, включенное в Государственный реестр медицинских изделий и техники. Этот документ гарантирует легальность использования данного продукта в медицинских целях на территории России. Вы можете проверить наличие такого удостоверения на сайте Федеральной службы по надзору в сфере здравоохранения (прямая ссылка на реестр).
Регистрационное удостоверение обязательно выдается для медицинских изделий, независимо от того, на какую компанию оформлено удостоверение — отечественную или иностранную, зарегистрированную в России по законодательству. Если у медицинского изделия нет Регистрационного удостоверения, его нельзя использовать или продавать на территории Российской Федерации. В народе Регистрационное удостоверение иногда называют Минздравом, потому что раньше Росздравнадзор был частью Министерства здравоохранения РФ.
Что нужно знать при получении Регистрационного Удостоверения
Для того чтобы корректно заполнить Регистрационное удостоверение, необходимо следовать установленным правилам, описанным в Приказе Министерства здравоохранения Российской Федерации от 14 октября 2013 года № 737н «Об утверждении Административного регламента Федеральной службы по надзору в сфере здравоохранения по предоставлению государственной услуги по государственной регистрации медицинских изделий». Классификация медицинских изделий определена на основе оценки степени потенциального риска (каждому изделию присваивается только один класс). Низкий уровень риска соответствует Классу риска «1».
Введено Постановлением Правительства № 299 от 18 марта 2020 года упрощенное оформление процедуры для масок, халатов, перчаток, бахил и других изделий. Классификация риска подразделяется на три категории. Класс риска «2а» включает лабораторную технику, спирометры, аудиометры и другие изделия со средним уровнем риска. Изделия повышенной степени риска, такие как дефибрилляторы, кардиоанализаторы и АВЛ – аппарат искусственной вентиляции легких, принадлежат к классу риска «2б». Эндопротезы, имплантаторы и другое оборудование, например, литотриптор – аппарат для дробления камня в мочевом пузыре, относятся к классу риска «3» со значительной степенью риска.
Для иностранных производителей необходима легализованная доверенность на уполномоченного представителя (текст и образец доверенности для РФ).
- Документ, подтверждающий право уполномоченного представителя.
1. Необходимо предоставить документы, подтверждающие регистрацию фирмы-производителя (например, выписку из торгово-промышленной палаты или аналогичный документ).
2. Для медицинского оборудования требуется сертификат СЕ, соответствующий Директиве 93/42/EEC, а для медицинских изделий для диагностики in vitro — Директиве 98/79/EEC.
3. Необходимо предоставить декларацию о соответствии самого изделия с Директивой 93/42/EEC или 98/79/EEC, либо сертификат свободной продажи.
4. Требуется сертификат ИСО 13485:2003 или ИСО 9001:2000.
5. Необходимо предоставить техническую и эксплуатационную документацию, а также тест-репорты в электронном виде.
6. Требуется клинический обзор.
Для российского производителя необходимо соблюдать все вышеперечисленные требования.
- Для российского производителя необходимо составление Технических условий в соответствии с ГОСТ Р 1.3-2018, которые определяют общие требования к содержанию, оформлению, обозначению и обновлению продукции.
- Создание эксплуатационной документации обязательно и должно соответствовать стандартам, установленным Приказом Минздрава РФ от 19 января 2017 года № 11н "Об утверждении требований к содержанию технической и эксплуатационной документации для производителя (изготовителя) медицинского изделия".
- Необходимо предоставить информацию о нормативных документах, которые регулируют производство и эксплуатацию медицинских изделий.
Становится важным учитывать, что при составлении компонентов медицинского изделия может понадобиться предоставление дополнительных документов. Если в медицинской технике используются измерительные приборы, такие как датчики и термометры, необходимо получить свидетельство об утверждении типа средств измерений для получения РУ. Также, для выполнения испытаний, потребуются образцы, количество которых зависит от сложности продукции и потребностей в ее тестировании.
Товары, исключенные из обязательного учета
Существуют товары, на которые государство не требует регистрации. Такие товары предназначены для использования только конкретными больными, по рекомендации врача. Так как регистрация не проводится на этих товарах, их стоимость устанавливается индивидуально, в зависимости от многих факторов.
Большинство медицинских изделий требуют прохождения государственной регистрации. Она обязательна для следующих категорий товаров:
- специализированное оборудование, аппаратура, техника и программы, используемые в медицинских целях, включая программное обеспечение;
- медицинские приборы и инструменты, а также комплекты таких изделий;
- Комплектующие для выполнения перевязок, стежков и прочих манипуляций, включая специальные материалы, необходимые расходные материалы и реагенты;
- Защитные изделия из резины и полимеров, используемые в медицинских целях для защиты персонала и выполнения медицинских манипуляций;
- Примеры материалов и изделий для контроля качества.
Это предложение легко регистрировать медицинские изделия, когда они используются вместе с другими аксессуарами, приборами и приспособлениями, необходимыми для их полноценного применения.
Основание для регистрации: Постановление Правительства № 1416 "О регистрации медицинских изделий"
Уже целых десять лет Российская Федерация является полноправным участником Евразийского экономического союза, и, соответственно, подчиняется всем установленным правилам и нормам, которые имеют силу на всей территории данного союзного образования. В эти дни создаётся единая процедура контроля качества медицинских товаров, которые реализуются на рынке в рамках этого союза. Но сформировать процедуру и установить необходимые правила, постановления и другие документы является весьма трудоёмким и длительным процессом.
В странах-членах ЕАЭС уже были приняты законы и различные постановления, устанавливающие правила для регистрации медицинских товаров в соответствии с правилами экономического союза. Основой являются Договор о Евразийском экономическом союзе от 29 мая 2014 года и Соглашение от 23 декабря 2014 года, которые определяют общие правила деятельности для контрагентов в этом секторе. Конкретные нормы и правила регистрации были зафиксированы в Решении Совета Евразийской экономической комиссии от 12 февраля 2016 года № 46, которое обсуждает правила регистрации медицинских товаров в ЕАЭС и устанавливает временные рамки для реализации соответствующих мероприятий.
О замене документов удостоверяющих личность до 1 января 2021 года

В нашей компании нередко поступают запросы по поводу действия регистрационных удостоверений, выданных до 1 января 2013 года, но не замененных на новую форму. Проблема заключается в том, что в соответствии с Правилами государственной регистрации медицинских изделий, утвержденными приказом Правительства РФ от 27 декабря 2012 года № 1416, регистрационные удостоверения на медицинские изделия и технику, выданные до вступления этого постановления в силу, являются бессрочными и должны быть заменены на новые формы до 1 января 2021 года, которые утверждаются Федеральной службой по надзору в сфере здравоохранения.
До 1 января 2013 года были выдаваемы регистрационные удостоверения старого образца, которые обязательно необходимо заменить на бланки нового образца. Замена проводится без процедуры государственной регистрации медицинских изделий на основании заявления, представленного заявителем в Федеральную службу по надзору в сфере здравоохранения, с указанием необходимых сведений.
Хотя данная процедура не требует особой сложности, некоторые заявители, к сожалению, не знают или забывают о ней. В результате регистрационные удостоверения с формулировкой "аннулирование" теряют свою силу.
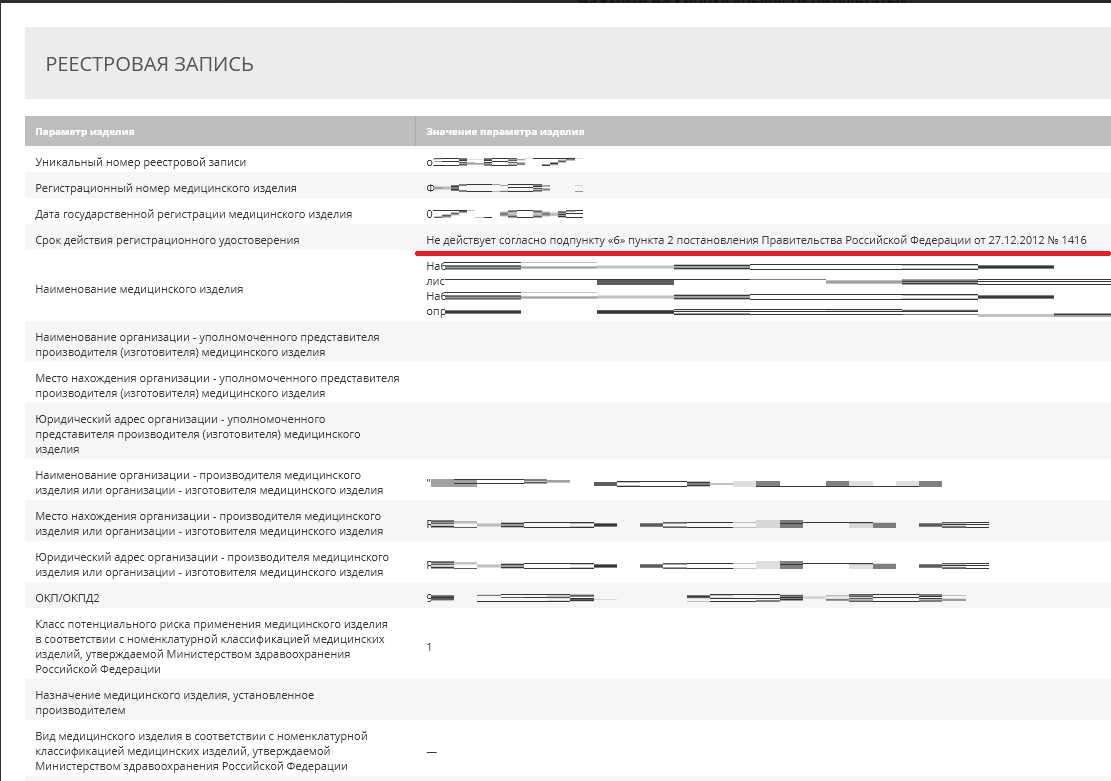
Согласно пункту 2 постановления Правительства Российской Федерации от 27.12.2012 № 1416, подпункт "б" не имеет юридической силы.
Распространенной проблемой является отсутствие возможности использования регистрационных удостоверений, которые не прошли процедуру замены бланка. На сайте Росздравнадзора представлено множество вопросов, которые наиболее часто возникают. Например, есть ли способы восстановить действие регистрационного удостоверения, действует ли оно в конце 2022 года или есть ли упрощенные механизмы для подобных случаев. Однако, на данный момент никаких механизмов, которые бы помогли облегчить процесс регистрации, не существует
Платежи за услуги
В 2015 году были внесены изменения в размер пошлин за некоторые действия, связанные с получением Регистрационного удостоверения:
- За государственную регистрацию медицинского оборудования теперь нужно заплатить 7000 рублей;
- За внесение изменений в документацию придется заплатить 1500 рублей;
- За дубликат Регистрационного удостоверения нужно заплатить 1500 рублей.
Изменение стоимости экспертизы качества РУ
Также были изменены цены на экспертизу качества Регистрационного удостоверения, которые зависят от категории опасности изделия:
- Категория «1»: 45000 рублей;
- Категория «2а»: 65000 рублей;
- Категория «2б»: 85000 рублей;
- Категория «3»: 115000 рублей.




